为实现“碳中和”目标,我国科学家做出了卓越贡献,最新科研成果之一为:在含铂高效催化剂作用下把二氧化碳高效转化清洁液态燃料——甲醇 。
。
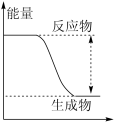
(1)转化过程的能量变化如图所示,可知 转化为
转化为 的反应为
的反应为___________ 反应(填“吸热”或“放热”)。
(2) 转化为
转化为 的总反应为
的总反应为 。下列描述能说明该反应已经达到限度的是___________。
。下列描述能说明该反应已经达到限度的是___________。
(3)科学家提出有关甲醇 的碳循环如图所示。
的碳循环如图所示。
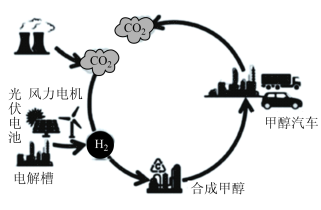
①碳循环过程中的能量转化方式有___________ (答出两种即可)。
②甲醇合成原理为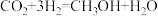 ,若合成甲醇
,若合成甲醇 ,则理论上可吸收工厂排放的
,则理论上可吸收工厂排放的
___________ L(标准状况);电解槽中发生电解反应 ,制备所需的
,制备所需的 转移的电子数为
转移的电子数为___________ (用 表示阿伏加德罗常数)。
表示阿伏加德罗常数)。
 。
。(1)转化过程的能量变化如图所示,可知
 转化为
转化为 的反应为
的反应为
(2)
 转化为
转化为 的总反应为
的总反应为 。下列描述能说明该反应已经达到限度的是___________。
。下列描述能说明该反应已经达到限度的是___________。A. 的生成速率与 的生成速率与 的生成速率相等时 的生成速率相等时 |
| B.恒温恒容时,容器内气体的总压强不再随时间而改变时 |
| C.容器内气体的总质量不再改变时 |
D.恒容时, 、 、 、 、 、 、 的浓度相等时 的浓度相等时 |
 的碳循环如图所示。
的碳循环如图所示。
①碳循环过程中的能量转化方式有
②甲醇合成原理为
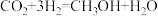 ,若合成甲醇
,若合成甲醇 ,则理论上可吸收工厂排放的
,则理论上可吸收工厂排放的
 ,制备所需的
,制备所需的 转移的电子数为
转移的电子数为 表示阿伏加德罗常数)。
表示阿伏加德罗常数)。
更新时间:2022-04-13 17:17:29
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】人类利用化学反应不仅可以创造新物质,还可以获取能量或实现不同形式能量之间的转化。如用柴木可以生火取暖和照明,在这个过程中________ 能转化成了_________ 能、__________ 能等;又如,利用电池的化学反应可获取驱动汽车的电能,在该过程中,实现了________ 能与________ 能的相互转化。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】Ⅰ.燃料电池电动汽车是利用氢气、甲醇、天然气(主要成分为甲烷)、汽油等燃料和空气中的氧在催化剂的作用下在燃料电池中经电化学反应产生的电能,并作为主要动力源驱动的汽车。
(1)汽车行驶的过程中,能量的转化形式为_______ 。
Ⅱ.利用下表数据回答下列问题:
(2)表示乙烷燃烧热的热化学方程式为_______ 。
(3)稳定性:正丁烷_______ 异丁烷(填“>”“<”或“=”);原因_______ 。
(4)相同质量的燃料,_______ (填“C”或“H”)的质量分数越大,燃烧放出的热量越多。
(5)二氧化碳是重要的温室气体,从环保角度分析,放出相同的热量时选择_______ (填“乙烷”或“甲醇”)作为燃料产生的CO2较少。
(6)现有氢气和丙烷混合气体3 mol,完全燃烧共产生2791.5 kJ的热量,则氢气和丙烷的物质的量之比为_______ 。
(1)汽车行驶的过程中,能量的转化形式为
Ⅱ.利用下表数据回答下列问题:
| 燃料 | 燃烧热/(kJ·mol-1) | 燃料 | 燃烧热/(kJ·mol-1) |
| 氢气 | 285.8 | 甲醇(CH3OH) | 726.51 |
| 甲烷(CH4) | 890.3 | 正丁烷(CH3CH2CH2CH3) | 2878.0 |
| 乙烷(C2H6) | 1559.8 | 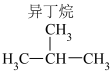 | 2869.6 |
| 丙烷(C3H8) | 2219.9 |
(3)稳定性:正丁烷
(4)相同质量的燃料,
(5)二氧化碳是重要的温室气体,从环保角度分析,放出相同的热量时选择
(6)现有氢气和丙烷混合气体3 mol,完全燃烧共产生2791.5 kJ的热量,则氢气和丙烷的物质的量之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】利用图甲、乙所示装置进行实验,图中两个烧杯里的溶液为同浓度的稀硫酸,乙中G为电流计。请回答下列问题:

(1)以下叙述中,正确的是___________。
(2)变化过程中能量转化的形式主要是:甲为___________ ;乙为___________ 。
(3)乙中锌电极的电极反应式为___________ ;铜电极的电极反应式为___________ ;
(4)乙装置反应过程中有0.4mol电子发生转移,则生成的氢气在标况下的体积为___________
(5)原电池在工作时,下列反应不可能作为原电池工作时发生的反应的是:___________

(1)以下叙述中,正确的是___________。
| A.甲中锌片是负极,乙中铜片是正极 |
| B.两烧杯中铜片表面均有气泡产生 |
C.乙溶液中 向铜片方向移动 向铜片方向移动 |
| D.乙中电流从铜片经导线流向锌片 |
(3)乙中锌电极的电极反应式为
(4)乙装置反应过程中有0.4mol电子发生转移,则生成的氢气在标况下的体积为
(5)原电池在工作时,下列反应不可能作为原电池工作时发生的反应的是:___________
| A.CH4+2O2=CO2+2H2O | B.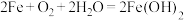 |
C. | D. |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】化学反应伴随有能量的变化,获取反应能量变化有多条途径。
(1)下列反应中,属于放热反应的是___________(填字母)。
(2)①通过化学键的键能计算。
已知几种化学键的键能如下:
计算可得:

___________ 。
②通过反应过程中物质能量的变化计算。由 和NO反应生成
和NO反应生成 和
和 的能量变化如图所示。若生成
的能量变化如图所示。若生成 ,其
,其
___________  。
。

③通过盖斯定律计算。
已知: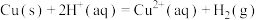

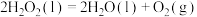

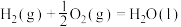

(ⅰ) 的燃烧热
的燃烧热
___________ 。
(ⅱ)在 溶液中Cu与
溶液中Cu与 反应生成
反应生成 和
和 的热化学方程式为
的热化学方程式为___________ 。
(1)下列反应中,属于放热反应的是___________(填字母)。
| A.碳与水蒸气反应 | B.铝和氧化铁反应 |
C. 受热分解 受热分解 | D.锌与盐酸反应 |
已知几种化学键的键能如下:
| 化学键种类 |  | H—H | N—H |
键能 | a | b | c |


②通过反应过程中物质能量的变化计算。由
 和NO反应生成
和NO反应生成 和
和 的能量变化如图所示。若生成
的能量变化如图所示。若生成 ,其
,其
 。
。
③通过盖斯定律计算。
已知:
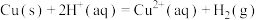

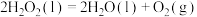

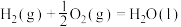

(ⅰ)
 的燃烧热
的燃烧热
(ⅱ)在
 溶液中Cu与
溶液中Cu与 反应生成
反应生成 和
和 的热化学方程式为
的热化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】反应Fe+H2SO4 FeSO4+H2↑的能量变化趋势如图所示:
FeSO4+H2↑的能量变化趋势如图所示:
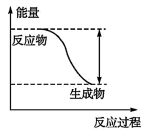
(1)该反应为____ (填“吸热”或“放热”)反应。
(2)若要使该反应的反应速率增大,下列措施可行的是____ (填字母)。
A.改铁片为铁粉 B.改稀硫酸为98%的浓硫酸
C.升高温度 D.减小压强
(3)若将上述反应设计成原电池,铜为原电池某一极材料,则铜为____ (填“正”或“负”)极。铜片上产生的现象为_________ ,该极上发生的电极反应为_______________ ,外电路中电子由____ (填“正”或“负”,下同)极向____ 极移动。
 FeSO4+H2↑的能量变化趋势如图所示:
FeSO4+H2↑的能量变化趋势如图所示:
(1)该反应为
(2)若要使该反应的反应速率增大,下列措施可行的是
A.改铁片为铁粉 B.改稀硫酸为98%的浓硫酸
C.升高温度 D.减小压强
(3)若将上述反应设计成原电池,铜为原电池某一极材料,则铜为
您最近一年使用:0次
【推荐3】工业上海水制氢气的新技术:2H2O 2H2↑+O2↑。试回答下列问题:
2H2↑+O2↑。试回答下列问题:
(1)分解海水的反应属于_______  填“放热”或“吸热”
填“放热”或“吸热” 反应。
反应。
(2)某种氢氧燃料电池是用固体金属化合物陶瓷作电解质,两极上发生的电极反应分别为 极:2H2+2O2--4e-=2H2O,B极:O2+4e-=2O2-,则
极:2H2+2O2--4e-=2H2O,B极:O2+4e-=2O2-,则 极是电池的
极是电池的_______ 极。
(3)氢气的储存比较困难,最近科学家研究出一种环保,安全的储氢方法,其原理可表示为NaHCO3+H2 HCOONa+H2O下列有关说法正确的是_______
HCOONa+H2O下列有关说法正确的是_______ 填序号
填序号 。
。
 2H2↑+O2↑。试回答下列问题:
2H2↑+O2↑。试回答下列问题:(1)分解海水的反应属于
 填“放热”或“吸热”
填“放热”或“吸热” 反应。
反应。(2)某种氢氧燃料电池是用固体金属化合物陶瓷作电解质,两极上发生的电极反应分别为
 极:2H2+2O2--4e-=2H2O,B极:O2+4e-=2O2-,则
极:2H2+2O2--4e-=2H2O,B极:O2+4e-=2O2-,则 极是电池的
极是电池的(3)氢气的储存比较困难,最近科学家研究出一种环保,安全的储氢方法,其原理可表示为NaHCO3+H2
 HCOONa+H2O下列有关说法正确的是_______
HCOONa+H2O下列有关说法正确的是_______ 填序号
填序号 。
。| A.储氢、释氢过程均无能量变化 |
| B.该反应属于可逆反应 |
| C.储氢过程中,NaHCO3被还原 |
| D.释氢过程中,每消耗0.1molH2O放出2.24L的H2 |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】(1)已知断裂1molN≡N键吸收945.6kJ能量,形成1molH-N键放出391kJ的能量。若1molN2和3molH2完全反应:N2+3H2 2NH3,放出的能量为92.4kJ,则断裂lmolH-H键吸收的能量是
2NH3,放出的能量为92.4kJ,则断裂lmolH-H键吸收的能量是___________ kJ。
(2)某温度时在2L容器中发生反应:A(g)+3B(g) mC(g),其中A、C两种气体物质的量(n)随时间(t)变化的曲线如图所示,由图中数据分析:
mC(g),其中A、C两种气体物质的量(n)随时间(t)变化的曲线如图所示,由图中数据分析:

①反应开始到2分钟,A的平均速率为___________ ;
②X点是不是平衡点___________ (填“是"或“否”),此时,v正___________ v逆(填“>”或“<”或“=”);
③m=___________ ;
④下列叙述能说明上述反应达到平衡状态的是___________ 。
A.三种物质的物质的量相等
B.相同时间内消耗amol的A的同时生成3amol的B
C.v(A)正=3v(B)逆
D.n(A)∶n(B)∶n(C)=1∶3∶m
E.混合气体的密度不再变化
 2NH3,放出的能量为92.4kJ,则断裂lmolH-H键吸收的能量是
2NH3,放出的能量为92.4kJ,则断裂lmolH-H键吸收的能量是(2)某温度时在2L容器中发生反应:A(g)+3B(g)
 mC(g),其中A、C两种气体物质的量(n)随时间(t)变化的曲线如图所示,由图中数据分析:
mC(g),其中A、C两种气体物质的量(n)随时间(t)变化的曲线如图所示,由图中数据分析:
①反应开始到2分钟,A的平均速率为
②X点是不是平衡点
③m=
④下列叙述能说明上述反应达到平衡状态的是
A.三种物质的物质的量相等
B.相同时间内消耗amol的A的同时生成3amol的B
C.v(A)正=3v(B)逆
D.n(A)∶n(B)∶n(C)=1∶3∶m
E.混合气体的密度不再变化
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】碘及其化合物在生产生活中有重要作用。
(1)单质碘可与氢气反应生成碘化氢。将物质的量比为 的氢气和碘蒸气放入恒容密闭容器中进行反应:
的氢气和碘蒸气放入恒容密闭容器中进行反应: ,反应经过5分钟后达平衡,测得碘化氢的浓度为0.1mol/L,碘蒸气的浓度为0.05mol/L。
,反应经过5分钟后达平衡,测得碘化氢的浓度为0.1mol/L,碘蒸气的浓度为0.05mol/L。
①前5分钟平均反应速率
___________ , 的初始浓度是
的初始浓度是___________ mol/L。
②反应分别进行至3min和7min时假设容器内气体的密度分别用 和
和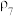 表示,则其大小为关系为
表示,则其大小为关系为
___________ 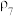 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
③下列能说明反应已达平衡状态的是___________ (填序号)。
a.混合体系总压强保持不变
b.单位时间内断裂的 键数目与断裂的
键数目与断裂的 键数目相等
键数目相等
c.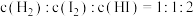
d.
e.反应混合体系的颜色不再发生变化
(2)某小组同学在室温下进行“碘钟实验”:将浓度均为0.01mol/L的 、
、 、
、 、
、 溶液及淀粉混合,一定时间后溶液变为蓝色。
溶液及淀粉混合,一定时间后溶液变为蓝色。
已知:“碘钟实验”的总反应的离子方程式为
反应分两步进行:
反应A:……
反应B:
①反应A的离子方程式是___________ 。对于总反应, 的作用是
的作用是___________ 。
②为探究溶液变蓝快慢的影响因素,进行实验Ⅰ、Ⅱ(溶液浓度均为0.01mol/L)
溶液从混合时的无色变为蓝色的时间:实验Ⅰ是30min、实验Ⅱ是40min。实验Ⅱ中,z所对应的数值是___________ ;对比实验Ⅰ、Ⅱ可得出的实验结论是___________ 。
(1)单质碘可与氢气反应生成碘化氢。将物质的量比为
 的氢气和碘蒸气放入恒容密闭容器中进行反应:
的氢气和碘蒸气放入恒容密闭容器中进行反应: ,反应经过5分钟后达平衡,测得碘化氢的浓度为0.1mol/L,碘蒸气的浓度为0.05mol/L。
,反应经过5分钟后达平衡,测得碘化氢的浓度为0.1mol/L,碘蒸气的浓度为0.05mol/L。①前5分钟平均反应速率

 的初始浓度是
的初始浓度是②反应分别进行至3min和7min时假设容器内气体的密度分别用
 和
和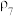 表示,则其大小为关系为
表示,则其大小为关系为
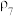 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。③下列能说明反应已达平衡状态的是
a.混合体系总压强保持不变
b.单位时间内断裂的
 键数目与断裂的
键数目与断裂的 键数目相等
键数目相等c.
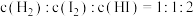
d.

e.反应混合体系的颜色不再发生变化
(2)某小组同学在室温下进行“碘钟实验”:将浓度均为0.01mol/L的
 、
、 、
、 、
、 溶液及淀粉混合,一定时间后溶液变为蓝色。
溶液及淀粉混合,一定时间后溶液变为蓝色。已知:“碘钟实验”的总反应的离子方程式为

反应分两步进行:
反应A:……
反应B:

①反应A的离子方程式是
 的作用是
的作用是②为探究溶液变蓝快慢的影响因素,进行实验Ⅰ、Ⅱ(溶液浓度均为0.01mol/L)
| 用量试剂 |  溶液 溶液 |  溶液 溶液 |  溶液 溶液 |  溶液(含淀粉) 溶液(含淀粉) |  |
| 实验Ⅰ | 5 | 4 | 8 | 3 | 0 |
| 实验Ⅱ | 5 | 2 | x | y | z |
溶液从混合时的无色变为蓝色的时间:实验Ⅰ是30min、实验Ⅱ是40min。实验Ⅱ中,z所对应的数值是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】空气质量与我们的健康息息相关,目前我国通过监测 6 项污染物的质量浓度来计算空气质量指数(AQI),SO2、NO2和 CO 是其中 3 项中的污染物。
(1)一定温度下,向固定体积为 2 L 的密闭容器中充入 SO2和 NO2各 1 mol,发生反应SO2(g)+NO2(g) SO3(g)+NO(g),测得上述反应 5 min 末到达平衡,此时容器中 NO 与 NO2的体积比为 3︰1,则这段时间内 SO2 的反应速率 v(SO2)=
SO3(g)+NO(g),测得上述反应 5 min 末到达平衡,此时容器中 NO 与 NO2的体积比为 3︰1,则这段时间内 SO2 的反应速率 v(SO2)=__________ ,此反应在该温度下的平衡常数 K=__________ 。
(2)甲醇日趋成为重要的有机燃料,通常利用 CO 和 H2合成甲醇,其反应的化学方程式为CO(g)+2H2(g) CH3OH(g)。今在一容积可变的密闭容器中,充有 10 mol CO 和 20 mol H2用于合成甲醇。CO 的平衡转化率(α)与温度(T)、压强(P)的关系如图所示:
CH3OH(g)。今在一容积可变的密闭容器中,充有 10 mol CO 和 20 mol H2用于合成甲醇。CO 的平衡转化率(α)与温度(T)、压强(P)的关系如图所示:
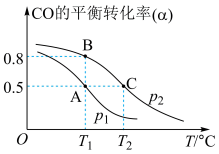
①上述合成甲醇的反应为__________ 反应(填“放热”或“吸热”)。
②A、B、C 三点的平衡常数 KA、KB、KC的大小关系为__________ 。A、B 两点对应的压强大小关系是 PA__________ PB(填“大于”、 “小于”或“等于”)。
(3) 若将达到平衡状态A时生成的甲醇用于构成甲醇一氧气燃料电池,电解质溶液为KOH浓溶液,则该电池工作时正极的电极反应式为____________ ,理论上通过外电路的电子最多为__________ mol。
(1)一定温度下,向固定体积为 2 L 的密闭容器中充入 SO2和 NO2各 1 mol,发生反应SO2(g)+NO2(g)
 SO3(g)+NO(g),测得上述反应 5 min 末到达平衡,此时容器中 NO 与 NO2的体积比为 3︰1,则这段时间内 SO2 的反应速率 v(SO2)=
SO3(g)+NO(g),测得上述反应 5 min 末到达平衡,此时容器中 NO 与 NO2的体积比为 3︰1,则这段时间内 SO2 的反应速率 v(SO2)=(2)甲醇日趋成为重要的有机燃料,通常利用 CO 和 H2合成甲醇,其反应的化学方程式为CO(g)+2H2(g)
 CH3OH(g)。今在一容积可变的密闭容器中,充有 10 mol CO 和 20 mol H2用于合成甲醇。CO 的平衡转化率(α)与温度(T)、压强(P)的关系如图所示:
CH3OH(g)。今在一容积可变的密闭容器中,充有 10 mol CO 和 20 mol H2用于合成甲醇。CO 的平衡转化率(α)与温度(T)、压强(P)的关系如图所示:
①上述合成甲醇的反应为
②A、B、C 三点的平衡常数 KA、KB、KC的大小关系为
(3) 若将达到平衡状态A时生成的甲醇用于构成甲醇一氧气燃料电池,电解质溶液为KOH浓溶液,则该电池工作时正极的电极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】如图所示,E为浸过含酚酞的Na2SO4溶液的滤纸。A、B分别为铂片,压在滤纸两端,R、S为电池的电极。M、N是用多微孔的Ni制成的电极,在碱溶液中可视为惰性电极。G为电流计,K为开关。C、D和电解池中都充满浓KOH溶液。若在滤纸中央滴一滴紫色的KMnO4溶液,将开关K打开,接通电源一段时间后,C、D中有气体产生。回答下列问题:

(1)R为_______ (填“正”或“负”)极。
(2)通电一段时间后,KOH溶液的浓度会_______ (填“变大”、“变小”或“不变”);B附近发生的电极反应式为_______ 。
(3)滤纸上的紫色点向_______ (填“A”或“B”)方向移动。
(4)当C、D中的气体产生到一定量时,切断外电源并接通开关K,经过一段时间后,C、D中的气体逐渐减少,C中的电极为_______ (填“正”或“负”)极,电极反应式为_______ 。
(5)如图,C、D、E、F、X、Y都是惰性电极,A、B为电源。将电源接通后,D电极上有无色气体放出。

①A为电源_______ 极。
②丙装置欲在铁钉上镀铜,则G电极上的反应式为_______ 。
③通电一段时间后,甲中出现浑浊,乙池中蓝色变浅,则甲中发生反应的化学方程式为:_______ ;乙池发生的离子方程式为:_______ ;
④工作一段时间后,丁中X极附近的颜色逐渐变浅,Y极附近的颜色逐渐变深,这说明Fe(OH)3胶粒带_______ 电,在电场作用下向Y极移动。
⑤若工作一段时间后停止通电,此时,乙中E、F两极上都产生2.24L气体(标准状况),欲使溶液恢复到起始状态,可向溶液中加入_______ (填序号)。
A.CuO B.Cu2(OH)2CO3 C.Cu(OH)2 D.CuCO3

(1)R为
(2)通电一段时间后,KOH溶液的浓度会
(3)滤纸上的紫色点向
(4)当C、D中的气体产生到一定量时,切断外电源并接通开关K,经过一段时间后,C、D中的气体逐渐减少,C中的电极为
(5)如图,C、D、E、F、X、Y都是惰性电极,A、B为电源。将电源接通后,D电极上有无色气体放出。

①A为电源
②丙装置欲在铁钉上镀铜,则G电极上的反应式为
③通电一段时间后,甲中出现浑浊,乙池中蓝色变浅,则甲中发生反应的化学方程式为:
④工作一段时间后,丁中X极附近的颜色逐渐变浅,Y极附近的颜色逐渐变深,这说明Fe(OH)3胶粒带
⑤若工作一段时间后停止通电,此时,乙中E、F两极上都产生2.24L气体(标准状况),欲使溶液恢复到起始状态,可向溶液中加入
A.CuO B.Cu2(OH)2CO3 C.Cu(OH)2 D.CuCO3
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】用如图所示的装置进行电解,A中盛有NaCl溶液,B中盛有饱和Na2SO4溶液,通电一会儿,发现湿润的淀粉KI试纸的D端变为蓝色。回答下列问题:

(1)电源的 F端为_______ (填“正”或“负”)极。
(2)A中发生反应的总化学方程式为_______ 。
(3)B中石墨电极上的电极反应式为_______ ;Cu电极观察到的现象是_______ ;一段时间后,B中溶液pH_______ (填“升高”、“降低”或“不变”)
(4)电池工作t min后,B装置中共收集到16.8 L(折算为标准状况下)气体,此时A中溶液的质量减轻了_______ g。
(5)去掉该装置中的电源,改用导线连接,为使湿润的淀粉KI试纸的D端变为蓝色,可将_______ (填“A”或“B”)中的溶液换成_______ (填“稀硫酸”或“浓硝酸”)。

(1)电源的 F端为
(2)A中发生反应的总化学方程式为
(3)B中石墨电极上的电极反应式为
(4)电池工作t min后,B装置中共收集到16.8 L(折算为标准状况下)气体,此时A中溶液的质量减轻了
(5)去掉该装置中的电源,改用导线连接,为使湿润的淀粉KI试纸的D端变为蓝色,可将
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】如图所示,通电5 min,电极5的质量增加2.16 g,请回答下列问题:

(1)a为电源的___ (填“正”或“负”)极,C池是___ 池。电极2的电极反应为________ ,电极3的电极反应为_______ 。
(2)如果B池中共收集到224 mL气体(标准状况)且溶液体积为200 mL(设电解过程中溶液体积不变),则通电前溶液中Cu2+的物质的量浓度为______ 。
(3)如果A池溶液是200 mL足量的食盐水(电解过程溶液体积不变,溶质足量),则通电5 min后,溶液的pH为______ 。

(1)a为电源的
(2)如果B池中共收集到224 mL气体(标准状况)且溶液体积为200 mL(设电解过程中溶液体积不变),则通电前溶液中Cu2+的物质的量浓度为
(3)如果A池溶液是200 mL足量的食盐水(电解过程溶液体积不变,溶质足量),则通电5 min后,溶液的pH为
您最近一年使用:0次



