Ⅰ.燃料电池电动汽车是利用氢气、甲醇、天然气(主要成分为甲烷)、汽油等燃料和空气中的氧在催化剂的作用下在燃料电池中经电化学反应产生的电能,并作为主要动力源驱动的汽车。
(1)汽车行驶的过程中,能量的转化形式为_______ 。
Ⅱ.利用下表数据回答下列问题:
(2)表示乙烷燃烧热的热化学方程式为_______ 。
(3)稳定性:正丁烷_______ 异丁烷(填“>”“<”或“=”);原因_______ 。
(4)相同质量的燃料,_______ (填“C”或“H”)的质量分数越大,燃烧放出的热量越多。
(5)二氧化碳是重要的温室气体,从环保角度分析,放出相同的热量时选择_______ (填“乙烷”或“甲醇”)作为燃料产生的CO2较少。
(6)现有氢气和丙烷混合气体3 mol,完全燃烧共产生2791.5 kJ的热量,则氢气和丙烷的物质的量之比为_______ 。
(1)汽车行驶的过程中,能量的转化形式为
Ⅱ.利用下表数据回答下列问题:
| 燃料 | 燃烧热/(kJ·mol-1) | 燃料 | 燃烧热/(kJ·mol-1) |
| 氢气 | 285.8 | 甲醇(CH3OH) | 726.51 |
| 甲烷(CH4) | 890.3 | 正丁烷(CH3CH2CH2CH3) | 2878.0 |
| 乙烷(C2H6) | 1559.8 | 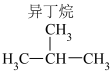 | 2869.6 |
| 丙烷(C3H8) | 2219.9 |
(3)稳定性:正丁烷
(4)相同质量的燃料,
(5)二氧化碳是重要的温室气体,从环保角度分析,放出相同的热量时选择
(6)现有氢气和丙烷混合气体3 mol,完全燃烧共产生2791.5 kJ的热量,则氢气和丙烷的物质的量之比为
23-24高二上·全国·课时练习 查看更多[1]
更新时间:2023-08-14 20:52:00
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】不同的化学反应具有不同的反应热,人们可以通过不同的方法获得反应热数据,可以实验测定,也可以理论推算。
(1)在稀溶液中,强酸与强碱发生中和反应生成1molH2O(1)时释放的热量叫中和热,中和热△H=-57.3kJ·mol-1
①某化学兴趣小组用50mL0.55mol·L-1盐酸、50mL0.50mol·L-1NaOH溶液进行中和热测定,计算结果△H=-58.2kJ·mol-1,其原因可能是:_______ 。
A.盐酸与NaOH溶液混合后立即记录温度
B.分三次将盐酸溶液缓慢倒入NaOH溶液中
C.用量筒量取NaOH溶液时仰视读数
D.使用环形玻璃棒搅拌
②若选用硫酸和氢氧化钡的稀溶液做中和热测定实验(操作无误),测定结果△H_______ 57.3kJ·mol-1(填“>”“=”或“<”)
(2)标准状况下,3.36L仅由C、H两种元素组成的某气体质量为4.5g,在25°C和101kPa下完全燃烧生成CO2(g)和H2O(l)时,放出233.97kJ的热量。
①该气体的分子式为_______ 。
②表示该气体燃烧热的热化学方程式为_______ 。
(3)①2022年北京冬奥会将用绿氢(H2)作为火炬燃料,以太阳能为热源,热化学硫碘循环分解水是一种高效、无污染的制氢方法。其反应过程如下图所示:

反应I:SO2(g)+2H2O(l)+I2(g)=H2SO4(aq)+2HI(aq) △H1=-213kJ·mol-1
反应II:2H2SO4(aq)=2SO2(g)+O2(g)+2H2O(l) △H2=+654kJ·mol-1
反应III:2HI(aq)=H2(g)+I2(g) △H3=+172kJ·mol-1
则反应2H2O(1)=2H2(g)+O2(g) △H=_______ 。
②2008年北京奥运会火炬燃料是丙烷(C3H8),已知丙烷的燃烧热为2220.0kJ·mol-1,室温下将8.96L(已折算为标准状况下体积)H2和C3H8的混合气体完全燃烧,共放307.8kJ热量,则该混合气体中H2和C3H8的体积比为_______ 。
(1)在稀溶液中,强酸与强碱发生中和反应生成1molH2O(1)时释放的热量叫中和热,中和热△H=-57.3kJ·mol-1
①某化学兴趣小组用50mL0.55mol·L-1盐酸、50mL0.50mol·L-1NaOH溶液进行中和热测定,计算结果△H=-58.2kJ·mol-1,其原因可能是:
A.盐酸与NaOH溶液混合后立即记录温度
B.分三次将盐酸溶液缓慢倒入NaOH溶液中
C.用量筒量取NaOH溶液时仰视读数
D.使用环形玻璃棒搅拌
②若选用硫酸和氢氧化钡的稀溶液做中和热测定实验(操作无误),测定结果△H
(2)标准状况下,3.36L仅由C、H两种元素组成的某气体质量为4.5g,在25°C和101kPa下完全燃烧生成CO2(g)和H2O(l)时,放出233.97kJ的热量。
①该气体的分子式为
②表示该气体燃烧热的热化学方程式为
(3)①2022年北京冬奥会将用绿氢(H2)作为火炬燃料,以太阳能为热源,热化学硫碘循环分解水是一种高效、无污染的制氢方法。其反应过程如下图所示:

反应I:SO2(g)+2H2O(l)+I2(g)=H2SO4(aq)+2HI(aq) △H1=-213kJ·mol-1
反应II:2H2SO4(aq)=2SO2(g)+O2(g)+2H2O(l) △H2=+654kJ·mol-1
反应III:2HI(aq)=H2(g)+I2(g) △H3=+172kJ·mol-1
则反应2H2O(1)=2H2(g)+O2(g) △H=
②2008年北京奥运会火炬燃料是丙烷(C3H8),已知丙烷的燃烧热为2220.0kJ·mol-1,室温下将8.96L(已折算为标准状况下体积)H2和C3H8的混合气体完全燃烧,共放307.8kJ热量,则该混合气体中H2和C3H8的体积比为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】按题意要求填空:
(1)已知10g己烷完全燃烧生成液态水放出484kJ的热量,写出表示己烷燃烧热的热化学方程______________ 。
(2)已知在微生物作用的条件下, 经过两步反应被氧化成
经过两步反应被氧化成 。两步反应的能量变化示意图如图:
。两步反应的能量变化示意图如图:

则 全部被氧化成
全部被氧化成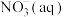 的热化学方程式为:
的热化学方程式为:_____________ 。
(3)化学键的键能是原子间形成(或断裂) 化学键时释放(或吸收)的能量。以下是部分共价键键能数据:H-S:
化学键时释放(或吸收)的能量。以下是部分共价键键能数据:H-S: ;S-S:
;S-S: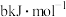 ;S=O:
;S=O: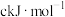 ;H-O:
;H-O: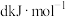 。
。
已知反应:
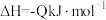 ,其反应产物中的固体
,其反应产物中的固体 实为
实为 ,实际分子是一个8元环状分子(即
,实际分子是一个8元环状分子(即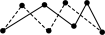 ),试根据这些数据计算已知反应的反应热:则Q=
),试根据这些数据计算已知反应的反应热:则Q=__________ (用a、b、c、d表示)。若已知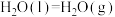
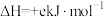 ,试写出
,试写出 和
和 反应生成
反应生成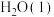 的热化学方程式为:
的热化学方程式为:_______ 。
(4)已知 (金刚石,s)
(金刚石,s)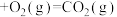
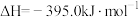
 (石墨,s)
(石墨,s)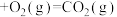
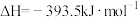
①石墨和金刚石相比,石墨的稳定性_______ 金刚石的稳定性。(填“大于”“小于”或“等于”,下同)
②石墨中 键键能
键键能_______ 金刚石中 键键能
键键能
(1)已知10g己烷完全燃烧生成液态水放出484kJ的热量,写出表示己烷燃烧热的热化学方程
(2)已知在微生物作用的条件下,
 经过两步反应被氧化成
经过两步反应被氧化成 。两步反应的能量变化示意图如图:
。两步反应的能量变化示意图如图:
则
 全部被氧化成
全部被氧化成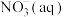 的热化学方程式为:
的热化学方程式为:(3)化学键的键能是原子间形成(或断裂)
 化学键时释放(或吸收)的能量。以下是部分共价键键能数据:H-S:
化学键时释放(或吸收)的能量。以下是部分共价键键能数据:H-S: ;S-S:
;S-S: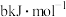 ;S=O:
;S=O: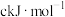 ;H-O:
;H-O: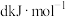 。
。已知反应:

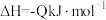 ,其反应产物中的固体
,其反应产物中的固体 实为
实为 ,实际分子是一个8元环状分子(即
,实际分子是一个8元环状分子(即 ),试根据这些数据计算已知反应的反应热:则Q=
),试根据这些数据计算已知反应的反应热:则Q=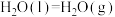
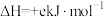 ,试写出
,试写出 和
和 反应生成
反应生成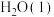 的热化学方程式为:
的热化学方程式为:(4)已知
 (金刚石,s)
(金刚石,s)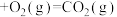
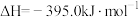
 (石墨,s)
(石墨,s)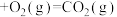
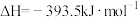
①石墨和金刚石相比,石墨的稳定性
②石墨中
 键键能
键键能 键键能
键键能
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】甲醇(CH3OH)是重要的化工原料及能源物质,如图是甲醇燃料电池工作的示意图,其中A、B、D均为石墨电极,C为铜电极。工作一段时间后,断开K,此时A、B两极上产生的气体体积相同。

(1)图1甲是____ (填“原电池”或“电解池”),通入甲醇这一极的电极反应式为____ 。
(2)该装置刚开始工作时图1乙中总反应的化学方程式为____ 。
(3)丙装置D电极反应式为____ ,溶液中金属阳离子的物质的量与转移电子的物质的量变化关系如图2,则图中②线表示的是____ (填离子符号)的变化。
(4)1g液体甲醇(CH3OH)燃烧生成CO2和液态水时放热23kJ。则表示甲醇燃烧热的热化学方程式为____ 。

(1)图1甲是
(2)该装置刚开始工作时图1乙中总反应的化学方程式为
(3)丙装置D电极反应式为
(4)1g液体甲醇(CH3OH)燃烧生成CO2和液态水时放热23kJ。则表示甲醇燃烧热的热化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】发生化学反应时,物质变化的同时常常伴随有能量变化。
(1)将锌片放入盛有稀硫酸的烧杯中,用温度计测量。随反应进行,温度升高,说明化学能转变为_______ 能。
(2)将 片和
片和 片用导线连接,并串联一个电流表,插入稀硫酸中,如图所示。
片用导线连接,并串联一个电流表,插入稀硫酸中,如图所示。

①证实化学能转化为电能的现象是_______ 。
②解释 片表面产生气泡的原因:
片表面产生气泡的原因:_______ 。
(3)已知:键能是指气态分子中1 化学键解离成气态原子所吸收的能量。
化学键解离成气态原子所吸收的能量。
当 和
和 化合生成2
化合生成2
 时,放出
时,放出_______  的能量。
的能量。
(4)利用 和
和 的反应设计氢氧燃料电池,装置如图所示。
的反应设计氢氧燃料电池,装置如图所示。

①通入 的电极是电池的
的电极是电池的_______ (填“正”或“负”)极。
②通入 的电极反应式是
的电极反应式是_______ 。
(1)将锌片放入盛有稀硫酸的烧杯中,用温度计测量。随反应进行,温度升高,说明化学能转变为
(2)将
 片和
片和 片用导线连接,并串联一个电流表,插入稀硫酸中,如图所示。
片用导线连接,并串联一个电流表,插入稀硫酸中,如图所示。
①证实化学能转化为电能的现象是
②解释
 片表面产生气泡的原因:
片表面产生气泡的原因:(3)已知:键能是指气态分子中1
 化学键解离成气态原子所吸收的能量。
化学键解离成气态原子所吸收的能量。| 化学键 |  |  |  |
| 键能/kJ·mol | 436 | 498 | 463 |
当
 和
和 化合生成2
化合生成2
 时,放出
时,放出 的能量。
的能量。(4)利用
 和
和 的反应设计氢氧燃料电池,装置如图所示。
的反应设计氢氧燃料电池,装置如图所示。
①通入
 的电极是电池的
的电极是电池的②通入
 的电极反应式是
的电极反应式是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】(1)已知1mol石墨转化为1mol金刚石要吸收能量,则1mol石墨的能量比1mol金刚石的能量___ (填“高”或“低”),石墨比金刚石___ (填“稳定”或“不稳定”)。
(2)Ba(OH)2•8H2O和NH4Cl反应的化学方程式是___ ,该反应是 ___ (填“吸热”或“放热”)反应,反应过程能量变化的图象符合___ (填“图1”或“图2”)。
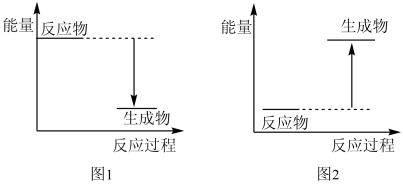
(3)如图3所示,把试管放入盛有饱和澄清石灰水(温度为25℃)的烧杯中,先在试管中放入几小块镁片,再用滴管滴入5mL盐酸。可以观察到烧杯中的石灰水逐渐由澄清变浑浊,出现这种现象的原因是___ 。
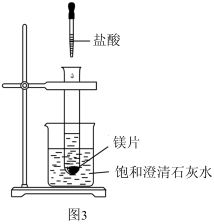
(2)Ba(OH)2•8H2O和NH4Cl反应的化学方程式是

(3)如图3所示,把试管放入盛有饱和澄清石灰水(温度为25℃)的烧杯中,先在试管中放入几小块镁片,再用滴管滴入5mL盐酸。可以观察到烧杯中的石灰水逐渐由澄清变浑浊,出现这种现象的原因是

您最近一年使用:0次
【推荐3】回答下列问题:
(1)在一个小烧杯中加入20g 晶体和10g
晶体和10g  晶体,然后将小烧杯放在事先滴有3~4滴水的玻璃片上,立即用玻璃棒搅拌。实验过程的示意图如下:
晶体,然后将小烧杯放在事先滴有3~4滴水的玻璃片上,立即用玻璃棒搅拌。实验过程的示意图如下:
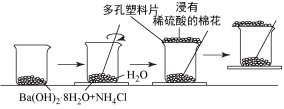
①实验中玻璃棒的作用:_______ 。
②浸有稀硫酸的棉花的作用:_______ 。
③出现结冰现象时,说明该反应为_______ 反应。
(2)沼气是一种廉价能源,农村存在大量的秸秆、杂草等废弃物,它们经微生物发酵之后,便可产生沼气,其主要成分是甲烷,可用来点火做饭。在农村推广建造沼气池,不仅能有效地利用_______ 能,还能为农业生产提供优良的肥料。已知:标准状况下,112.0L 气体完全燃烧生成
气体完全燃烧生成 和液态水时,放出4448kJ的热量。如果上述反应生成的是水蒸气,则反应放出的热量
和液态水时,放出4448kJ的热量。如果上述反应生成的是水蒸气,则反应放出的热量_______ 4448kJ(填“>”“<”或“=”)。
(3)钢铁中因含有碳,容易因构成原电池而发生电化学腐蚀。若在中性环境下,钢铁中少量的碳作为原电池的_______ 极,正极发生的电极反应式:_______ 。
(1)在一个小烧杯中加入20g
 晶体和10g
晶体和10g  晶体,然后将小烧杯放在事先滴有3~4滴水的玻璃片上,立即用玻璃棒搅拌。实验过程的示意图如下:
晶体,然后将小烧杯放在事先滴有3~4滴水的玻璃片上,立即用玻璃棒搅拌。实验过程的示意图如下:
①实验中玻璃棒的作用:
②浸有稀硫酸的棉花的作用:
③出现结冰现象时,说明该反应为
(2)沼气是一种廉价能源,农村存在大量的秸秆、杂草等废弃物,它们经微生物发酵之后,便可产生沼气,其主要成分是甲烷,可用来点火做饭。在农村推广建造沼气池,不仅能有效地利用
 气体完全燃烧生成
气体完全燃烧生成 和液态水时,放出4448kJ的热量。如果上述反应生成的是水蒸气,则反应放出的热量
和液态水时,放出4448kJ的热量。如果上述反应生成的是水蒸气,则反应放出的热量(3)钢铁中因含有碳,容易因构成原电池而发生电化学腐蚀。若在中性环境下,钢铁中少量的碳作为原电池的
您最近一年使用:0次



