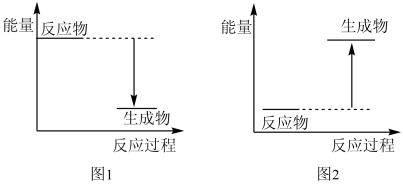
(1)已知1mol石墨转化为1mol金刚石要吸收能量,则1mol石墨的能量比1mol金刚石的能量___ (填“高”或“低”),石墨比金刚石___ (填“稳定”或“不稳定”)。
(2)Ba(OH)2•8H2O和NH4Cl反应的化学方程式是___ ,该反应是 ___ (填“吸热”或“放热”)反应,反应过程能量变化的图象符合___ (填“图1”或“图2”)。
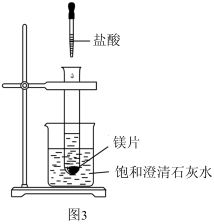
(3)如图3所示,把试管放入盛有饱和澄清石灰水(温度为25℃)的烧杯中,先在试管中放入几小块镁片,再用滴管滴入5mL盐酸。可以观察到烧杯中的石灰水逐渐由澄清变浑浊,出现这种现象的原因是___ 。
(2)Ba(OH)2•8H2O和NH4Cl反应的化学方程式是

(3)如图3所示,把试管放入盛有饱和澄清石灰水(温度为25℃)的烧杯中,先在试管中放入几小块镁片,再用滴管滴入5mL盐酸。可以观察到烧杯中的石灰水逐渐由澄清变浑浊,出现这种现象的原因是

19-20高一·全国·课时练习 查看更多[1]
更新时间:2020-04-19 18:28:47
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】发生化学反应时,物质变化的同时常常伴随有能量变化。
(1)将锌片放入盛有稀硫酸的烧杯中,用温度计测量。随反应进行,温度升高,说明化学能转变为_____ 能。
(2)将Zn片和Cu片用导线连接,并串联一个电流表,插入稀硫酸中,如图所示。

①证实化学能转化为电能的现象是_____ 。
②解释Cu片表面产生气泡的原因:_____ 。
(3)已知:键能是指气态分子中1mol化学键解离成气态原子所吸收的能量。
当H2和O2化合生成2molH2O(g)时,放出_____ kJ的能量。
(4)利用H2与O2的反应设计氢氧燃料电池,装置如图所示。
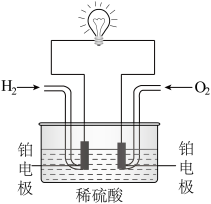
①通入O2的电极是电池的_____ (填“正”或“负”)极。
②通入H2的电极反应式是_____ 。
(1)将锌片放入盛有稀硫酸的烧杯中,用温度计测量。随反应进行,温度升高,说明化学能转变为
(2)将Zn片和Cu片用导线连接,并串联一个电流表,插入稀硫酸中,如图所示。

①证实化学能转化为电能的现象是
②解释Cu片表面产生气泡的原因:
(3)已知:键能是指气态分子中1mol化学键解离成气态原子所吸收的能量。
| 化学键 | H-H | O=O | H-O |
| 键能/kJ•mol-1 | 436 | 498 | 463 |
当H2和O2化合生成2molH2O(g)时,放出
(4)利用H2与O2的反应设计氢氧燃料电池,装置如图所示。

①通入O2的电极是电池的
②通入H2的电极反应式是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】回答下列问题:
(1)①已知断裂或形成1mol化学键所吸收或放出的能量叫做该化学键的键能,单位为 。白磷在氧气中燃烧的化学方程式可用结构式表示如图:
。白磷在氧气中燃烧的化学方程式可用结构式表示如图:
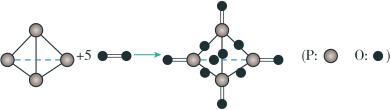
根据下表中数据计算: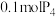 (白磷)在氧气中充分反应
(白磷)在氧气中充分反应_______ (填“吸收”或“放出”)_______ kJ能量,在此过程中能量的转化形式为_______ 。
②白磷在氧气中燃烧的能量变化可用图中的_______ (填字母)表示。

③已知在一定条件下,白磷转化为红磷释放能量,故白磷比红磷的稳定性_______ (填“强”或“弱”)。
(2)下列变化中属于放热反应的是_______ (填字母)
A. 晶体与
晶体与 晶体的反应
晶体的反应
B.镁条与二氧化碳反应
C.干冰升华为气体
D.碳酸钙高温煅烧
E.铝热反应
(3)根据下图所示的转化关系判断,生成 放出
放出_______ kJ能量。

(1)①已知断裂或形成1mol化学键所吸收或放出的能量叫做该化学键的键能,单位为
 。白磷在氧气中燃烧的化学方程式可用结构式表示如图:
。白磷在氧气中燃烧的化学方程式可用结构式表示如图:
根据下表中数据计算:
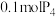 (白磷)在氧气中充分反应
(白磷)在氧气中充分反应| 化学键 |  |  |  | 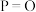 |
键能/ | 198 | 360 | 498 | 585 |

③已知在一定条件下,白磷转化为红磷释放能量,故白磷比红磷的稳定性
(2)下列变化中属于放热反应的是
A.
 晶体与
晶体与 晶体的反应
晶体的反应B.镁条与二氧化碳反应
C.干冰升华为气体
D.碳酸钙高温煅烧
E.铝热反应
(3)根据下图所示的转化关系判断,生成
 放出
放出
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】分别按如图甲、乙所示装置进行实验,图中两个烧杯里的溶液为同浓度的稀硫酸,乙中A为电流表。请回答下列问题:

(1)以下叙述中,正确的是______ (填字母)(双项选择)。
A.甲中锌片是负极,乙中铜片是正极
B.两烧杯中铜片表面均有气泡产生
C.两烧杯中溶液pH均增大
D.产生气泡的速度甲中比乙中慢
E.乙的外电路中电流方向Zn→Cu
F.乙溶液中 向铜片方向移动
向铜片方向移动
(2)变化过程中能量转化的主要形式:甲为_______ ;乙为______ 。
(3)在乙实验中,某同学发现不仅在铜片上有气泡产生,而且在锌片上也产生了气体,分析原因可能是_______ 。
(4)在乙实验中,如果把硫酸换成硫酸铜溶液,请写出铜电极的电极反应方程式及总反应离子方程式:铜电极:________ ,总反应:_________ 。当电路中转移0.2mol电子时,消耗负极材料的质量为______ g(Zn的相对原子质量为65)。

(1)以下叙述中,正确的是
A.甲中锌片是负极,乙中铜片是正极
B.两烧杯中铜片表面均有气泡产生
C.两烧杯中溶液pH均增大
D.产生气泡的速度甲中比乙中慢
E.乙的外电路中电流方向Zn→Cu
F.乙溶液中
 向铜片方向移动
向铜片方向移动(2)变化过程中能量转化的主要形式:甲为
(3)在乙实验中,某同学发现不仅在铜片上有气泡产生,而且在锌片上也产生了气体,分析原因可能是
(4)在乙实验中,如果把硫酸换成硫酸铜溶液,请写出铜电极的电极反应方程式及总反应离子方程式:铜电极:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】I.下列是中学化学中熟悉的物质,请用序号完成下列问题
①O2②Na2O2③NH4Cl ④HCl ⑤NaOH ⑥CaCl2
(1)这些物质中,只含共价键的是__________________ 。
(2)只含离子键的是__________________ 。
(3)既含共价键又含离子键的是__________________ 。
(4)属于离子化合物的是_____________ ,属于共价化合物的是____________ 。
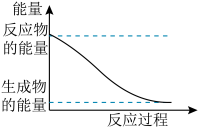
(5)20世纪30年代,Eyring和Pzer在碰撞理论的基础上提出化学反应的过渡态理论:化学反应并不是通过简单的碰撞就能完成的,而是在反应物到生成物的过程中经过一个高能量的过渡态。如图是NO2和CO反应生成CO2和NO过程中的能量变化示意图,说明这个反应是______ 。(填“吸热”或“放热”)反应,NO2和CO的总能量____________ (填“大于”、“小于”或“等于”)CO2和NO的总能量。
(6)下列反应中,属于放热反应的是_____________ ,属于吸热反应的是___________ 。
①物质燃烧;
②酸碱中和反应;
③Ba(OH)2·8H2O与NH4Cl反应;
④二氧化碳通过炽热的碳;
⑤铝与四氧化三铁在高温条件下的反应
①O2②Na2O2③NH4Cl ④HCl ⑤NaOH ⑥CaCl2
(1)这些物质中,只含共价键的是
(2)只含离子键的是
(3)既含共价键又含离子键的是
(4)属于离子化合物的是
(5)20世纪30年代,Eyring和Pzer在碰撞理论的基础上提出化学反应的过渡态理论:化学反应并不是通过简单的碰撞就能完成的,而是在反应物到生成物的过程中经过一个高能量的过渡态。如图是NO2和CO反应生成CO2和NO过程中的能量变化示意图,说明这个反应是

(6)下列反应中,属于放热反应的是
①物质燃烧;
②酸碱中和反应;
③Ba(OH)2·8H2O与NH4Cl反应;
④二氧化碳通过炽热的碳;
⑤铝与四氧化三铁在高温条件下的反应
您最近一年使用:0次
【推荐2】化学上,由稳定单质生成 纯物质的热效应称为生成热,稳定单质的生成热定为0。生成热的相对大小可以判断物质的相对能量。硫及其化合物的生成热如图所示。
纯物质的热效应称为生成热,稳定单质的生成热定为0。生成热的相对大小可以判断物质的相对能量。硫及其化合物的生成热如图所示。
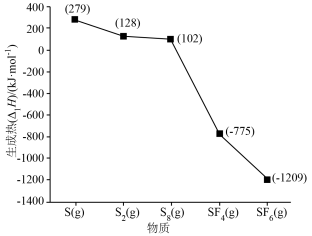
回答下列问题:
(1)图中三种硫单质中,最稳定的是________ (填化学式,下同),最活泼的是__________ 。
(2)已知:i. ;
;
ii. ;
;
iii. 。
。
①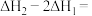
___________  。
。
②
___________ 0(填“>”“<”或“=”),判断依据是___________ 。
(3)根据图像,计算反应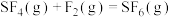 的
的
___________  。
。
 纯物质的热效应称为生成热,稳定单质的生成热定为0。生成热的相对大小可以判断物质的相对能量。硫及其化合物的生成热如图所示。
纯物质的热效应称为生成热,稳定单质的生成热定为0。生成热的相对大小可以判断物质的相对能量。硫及其化合物的生成热如图所示。
回答下列问题:
(1)图中三种硫单质中,最稳定的是
(2)已知:i.
 ;
;ii.
 ;
;iii.
 。
。①
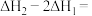
 。
。②

(3)根据图像,计算反应
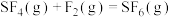 的
的
 。
。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】在2L恒容密闭的绝热容器中,发生反应 ,该反应为放热反应,其中
,该反应为放热反应,其中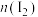 和
和 随时间的变化如下表:
随时间的变化如下表:
(1)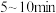 的平均反应速率比
的平均反应速率比 大的原因可能是
大的原因可能是___________ , 之后正反应速率下降的原因可能是
之后正反应速率下降的原因可能是___________ 。
(2) 内
内 的平均反应速率为
的平均反应速率为___________  。该条件下反应达到平衡时,
。该条件下反应达到平衡时, 的浓度为
的浓度为___________ , 的体积分数为
的体积分数为___________ %。
(3)保持其他条件不改变,能说明该反应已经达到平衡状态的是___________ (填标号)。
a.混合气体的密度不变 b.混合气体的颜色保持不变
c.消耗
 的同时生成
的同时生成
 d.
d.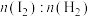 的值保持不变
的值保持不变
(4)保持其他条件不变,第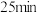 再加入
再加入
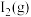 ,反应达到平衡时,下列说法错误的是___________(填标号)。
,反应达到平衡时,下列说法错误的是___________(填标号)。
 ,该反应为放热反应,其中
,该反应为放热反应,其中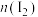 和
和 随时间的变化如下表:
随时间的变化如下表:| 时间/min | 0 | 5 | 10 | 15 | 20 | 25 |
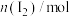 | 2.00 | 1.80 | 1.50 | 1.44 | 1.40 | 1.40 |
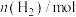 | 1.00 | 0.80 | 0.50 | 0.44 | 0.40 | 0.40 |
(1)
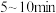 的平均反应速率比
的平均反应速率比 大的原因可能是
大的原因可能是 之后正反应速率下降的原因可能是
之后正反应速率下降的原因可能是(2)
 内
内 的平均反应速率为
的平均反应速率为 。该条件下反应达到平衡时,
。该条件下反应达到平衡时, 的浓度为
的浓度为 的体积分数为
的体积分数为(3)保持其他条件不改变,能说明该反应已经达到平衡状态的是
a.混合气体的密度不变 b.混合气体的颜色保持不变
c.消耗

 的同时生成
的同时生成
 d.
d.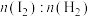 的值保持不变
的值保持不变(4)保持其他条件不变,第
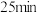 再加入
再加入
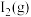 ,反应达到平衡时,下列说法错误的是___________(填标号)。
,反应达到平衡时,下列说法错误的是___________(填标号)。A.反应再次达到平衡时,容器内可能含有 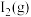 |
B.再加入 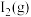 后,正反应速率会加快 后,正反应速率会加快 |
C. 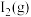 和 和  具有的总能量高于 具有的总能量高于 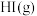 所具有的总能量 所具有的总能量 |
D.再加入 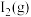 ,平衡时混合气体的颜色比初次投料平衡时的颜色更浅 ,平衡时混合气体的颜色比初次投料平衡时的颜色更浅 |
您最近一年使用:0次



