反应Fe+H2SO4 FeSO4+H2↑的能量变化趋势如图所示:
FeSO4+H2↑的能量变化趋势如图所示:
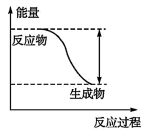
(1)该反应为____ (填“吸热”或“放热”)反应。
(2)若要使该反应的反应速率增大,下列措施可行的是____ (填字母)。
A.改铁片为铁粉 B.改稀硫酸为98%的浓硫酸
C.升高温度 D.减小压强
(3)若将上述反应设计成原电池,铜为原电池某一极材料,则铜为____ (填“正”或“负”)极。铜片上产生的现象为_________ ,该极上发生的电极反应为_______________ ,外电路中电子由____ (填“正”或“负”,下同)极向____ 极移动。
 FeSO4+H2↑的能量变化趋势如图所示:
FeSO4+H2↑的能量变化趋势如图所示:
(1)该反应为
(2)若要使该反应的反应速率增大,下列措施可行的是
A.改铁片为铁粉 B.改稀硫酸为98%的浓硫酸
C.升高温度 D.减小压强
(3)若将上述反应设计成原电池,铜为原电池某一极材料,则铜为
更新时间:2020-05-19 10:29:43
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】用CO2制备甲醇的反应原理为:CO2(g)+3H2(g) CH3OH(g)+H2O(g)。该反应进程可通过如图所示的两步反应实现。
CH3OH(g)+H2O(g)。该反应进程可通过如图所示的两步反应实现。
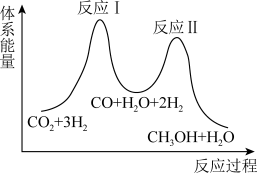
回答下列问题:
(1)反应I的化学方程式是____ 。
(2)由图可知,反应____ (填“I”或“II”)为慢反应。
(3)反应II:CO(g)+2H2(g) CH3OH(g) △H
CH3OH(g) △H____ 0(填“>”“<”或“=”)。
(4)在容积可变的密闭容器中投入0.5molCO和1molH2,发生反应:CO(g)+2H2(g) CH3OH(g),测得平衡时CH3OH的物质的量随温度、压强变化如图所示。
CH3OH(g),测得平衡时CH3OH的物质的量随温度、压强变化如图所示。

①P总1____ P总2(填“>”“<”或“=”),判断理由是____ 。
②若P总1=0.25MPa,则500K时该反应的平衡常数Kp=____ MPa-2。
 CH3OH(g)+H2O(g)。该反应进程可通过如图所示的两步反应实现。
CH3OH(g)+H2O(g)。该反应进程可通过如图所示的两步反应实现。
回答下列问题:
(1)反应I的化学方程式是
(2)由图可知,反应
(3)反应II:CO(g)+2H2(g)
 CH3OH(g) △H
CH3OH(g) △H(4)在容积可变的密闭容器中投入0.5molCO和1molH2,发生反应:CO(g)+2H2(g)
 CH3OH(g),测得平衡时CH3OH的物质的量随温度、压强变化如图所示。
CH3OH(g),测得平衡时CH3OH的物质的量随温度、压强变化如图所示。
①P总1
②若P总1=0.25MPa,则500K时该反应的平衡常数Kp=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】I.填空。
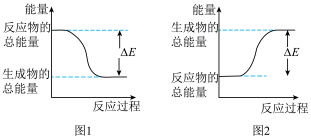
(1)下列反应中,能量变化符合图1的有___________ (填序号,下同),符合图2的有___________ 。
①煅烧石灰石 ②木炭燃烧 ③炸药爆炸 ④酸碱中和 ⑤碳与二氧化碳高温反应
II.如图所示,把试管放入盛有25℃时饱和石灰水的烧杯中,试管中开始放入几小块镁片,再用滴管滴入5mL盐酸于试管中。已知: 的溶解度随温度升高而降低。试回答下列问题:
的溶解度随温度升高而降低。试回答下列问题:
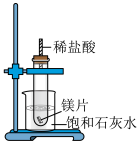
(2)实验中观察到的现象是___________ 。
(3)若将镁和稀盐酸的反应设计成原电池,用稀盐酸作电解质溶液,铜为原电池的某一电极材料,则铜为原电池的___________ (填“正”或“负”,下同)极。电解质溶液中 向
向___________ 极移动。
(4)将铁棒和锌片连接后浸入 溶液里,当电池中有0.2mol电子通过时,正极电极反应式:
溶液里,当电池中有0.2mol电子通过时,正极电极反应式:___________ ,负极质量的变化是减少___________ g。
(1)下列反应中,能量变化符合图1的有
①煅烧石灰石 ②木炭燃烧 ③炸药爆炸 ④酸碱中和 ⑤碳与二氧化碳高温反应

II.如图所示,把试管放入盛有25℃时饱和石灰水的烧杯中,试管中开始放入几小块镁片,再用滴管滴入5mL盐酸于试管中。已知:
 的溶解度随温度升高而降低。试回答下列问题:
的溶解度随温度升高而降低。试回答下列问题:
(2)实验中观察到的现象是
(3)若将镁和稀盐酸的反应设计成原电池,用稀盐酸作电解质溶液,铜为原电池的某一电极材料,则铜为原电池的
 向
向(4)将铁棒和锌片连接后浸入
 溶液里,当电池中有0.2mol电子通过时,正极电极反应式:
溶液里,当电池中有0.2mol电子通过时,正极电极反应式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】已知下列热化学方程式:
①H2(g)+1/2O2(g)===H2O(l) ΔH=-285.8 kJ·mol-1
②H2(g)+1/2O2(g)===H2O(g) ΔH=-241.8 kJ·mol-1
③C(s)+1/2O2(g)===CO(g) ΔH=-110.5 kJ·mol-1
④C(s)+O2(g)===CO2(g) ΔH=-393.5 kJ·mol-1
回答下列各问题:
(1)上述反应中属于放热反应的是_____ 。
(2)燃烧10 g H2生成液态水,放出的热量为__ 。
(3)CO的燃烧热为________________ ;其热化学方程式为______________ 。
①H2(g)+1/2O2(g)===H2O(l) ΔH=-285.8 kJ·mol-1
②H2(g)+1/2O2(g)===H2O(g) ΔH=-241.8 kJ·mol-1
③C(s)+1/2O2(g)===CO(g) ΔH=-110.5 kJ·mol-1
④C(s)+O2(g)===CO2(g) ΔH=-393.5 kJ·mol-1
回答下列各问题:
(1)上述反应中属于放热反应的是
(2)燃烧10 g H2生成液态水,放出的热量为
(3)CO的燃烧热为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】甲烷(CH4)是自然界储量丰富的天然气的主要组分,可用作清洁能源和廉价的化工原料,将甲烷催化转化为具有更高价值的化学物质是一个广受关注的课题.哈尔滨工业大学的科研人员研究了由CO2和CH4转化为高附加值产品CH3COOH的催化反应历程(催化剂是Zn/ZSM-5),共分为甲烷活化、二氧化碳进入和H转移(夺氢)三个阶段。该反应历程的示意图如图:
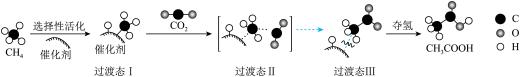
(1)在研究初期,科研人员提出先将CH4转化成CO和H2,再转化成CH3COOH。
已知:
①2CO(g)+O2(g)=2CO2(g) △H1
②2H2(g)+O2(g)=2H2O(l) △H2
③CH3COOH(g)+2O2(g)=2CO2(g)+2H2O(l) △H3
则混合气体CO和H2转化成CH3COOH(g)的热化学方程式为____ 。
(2)催化剂Zn/ZSM-5有以下四种形态:Z1(Zn2+/ZSM-5)、Z2([ZnOZn]2+/ZSM-5)、Z3(Zn2+,[ZnOZn]2+/ZSM-5)、Z4([bi-ZnOZn]2+Zn2+/ZSM-5)。
图甲、图乙分别表示反应CH4(g)+CO2(g) CH3COOH(g) △H4在催化剂Zn/ZSM-5的Z1、Z2形态时的势能变化:
CH3COOH(g) △H4在催化剂Zn/ZSM-5的Z1、Z2形态时的势能变化:
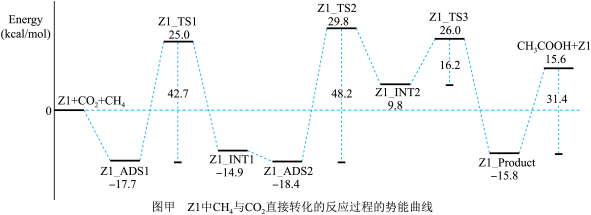

由图甲、图乙可知△H4____ 0(填“>”“<”或“=”);不同形态的Z1、Z2对△H4____ (填“有”或“无”)影响。
(3)从CH4到过渡态I断裂的是____ 键(填“碳氢”“碳碳”“氧氢”或“碳氧”,下同),最后一步“夺氢”过程中有____ 键形成。

(1)在研究初期,科研人员提出先将CH4转化成CO和H2,再转化成CH3COOH。
已知:
①2CO(g)+O2(g)=2CO2(g) △H1
②2H2(g)+O2(g)=2H2O(l) △H2
③CH3COOH(g)+2O2(g)=2CO2(g)+2H2O(l) △H3
则混合气体CO和H2转化成CH3COOH(g)的热化学方程式为
(2)催化剂Zn/ZSM-5有以下四种形态:Z1(Zn2+/ZSM-5)、Z2([ZnOZn]2+/ZSM-5)、Z3(Zn2+,[ZnOZn]2+/ZSM-5)、Z4([bi-ZnOZn]2+Zn2+/ZSM-5)。
图甲、图乙分别表示反应CH4(g)+CO2(g)
 CH3COOH(g) △H4在催化剂Zn/ZSM-5的Z1、Z2形态时的势能变化:
CH3COOH(g) △H4在催化剂Zn/ZSM-5的Z1、Z2形态时的势能变化:

由图甲、图乙可知△H4
(3)从CH4到过渡态I断裂的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】某学生为了探究锌与盐酸反应过程中的速率变化,他在100mL某浓度的稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气,实验记录如下(累计值,体积已换算成标准状态):
(1)2~3min段的反应速率比1~2min段的反应速率__________ (填“块”或“慢”),原因是______ ;
(2)求2~3min段以HCl的浓度变化来表示的平均反应速率(设溶液体积不变)____________ ;
(3)如果反应太激烈,为了减缓反应速率而又不减少产生氢气的量,可以在盐酸中分别加入等体积的下列溶液,你认为可行的是(填编号)____________ 。
A.蒸馏水 B.NaCl溶液 C.Na2CO3溶液 D.CuSO4溶液
| 时间(min) | 0 | 1 | 2 | 3 | 4 | 5 |
| 氢气体积(mL) | 0 | 50 | 120 | 232 | 290 | 310 |
(1)2~3min段的反应速率比1~2min段的反应速率
(2)求2~3min段以HCl的浓度变化来表示的平均反应速率(设溶液体积不变)
(3)如果反应太激烈,为了减缓反应速率而又不减少产生氢气的量,可以在盐酸中分别加入等体积的下列溶液,你认为可行的是(填编号)
A.蒸馏水 B.NaCl溶液 C.Na2CO3溶液 D.CuSO4溶液
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】已知2SO2(g)+O2(g) 2SO3(g) ΔH<0的实验数据如下表:
2SO3(g) ΔH<0的实验数据如下表:
(1)应选择的温度是___________ ,理由是___________ 。
(2)应采用的压强是___________ ,理由是___________ 。
(3)生产中通入过量空气的目的是___________ 。
 2SO3(g) ΔH<0的实验数据如下表:
2SO3(g) ΔH<0的实验数据如下表:| 温度 | 不同压强下SO2的转化率(%) | ||||
| 1×105 Pa | 5×105 Pa | 1×106 Pa | 5×106 Pa | 1×107 Pa | |
| 450 ℃ | 97.5 | 98.9 | 99.2 | 99.6 | 99.7 |
| 550 ℃ | 85.6 | 92.9 | 94.9 | 97.7 | 98.3 |
(2)应采用的压强是
(3)生产中通入过量空气的目的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】如图所示,A、B、C三个装置中的烧杯分别盛有足量的CuCl2溶液。
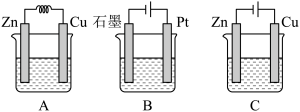
(1)A、B、C三个装置中属于原电池的是____ (填标号,下同),属于电解池的是______ 。
(2)A池中Zn发生___ (填“氧化”或“还原”)反应,Cu电极反应式为__________ 。
(3)B池中石墨是____ 极,Pt极发生的电极反应为_______________ 。
(4)C池中Cu是____ 极,电极反应为__________ ,反应过程中,溶液浓度_____ (填“变大”“变小”或“不变”)。

(1)A、B、C三个装置中属于原电池的是
(2)A池中Zn发生
(3)B池中石墨是
(4)C池中Cu是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】如图所示是原电池的装置图。请回答:
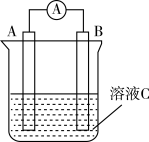
(1)若C为稀H2SO4,电流表指针发生偏转,B电极材料为Fe且作负极,则A电极上发生的电极反应式为________ ;反应进行一段时间后溶液酸性将________ (填“增强”“减弱”或“基本不变”)。
(2)若需将反应:Cu+2Fe3+=Cu2++2Fe2+设计成如图所示的原电池装置,则A(正极)极材料为_______ ,B(负极)极材料为________ ,溶液C为__________ 。
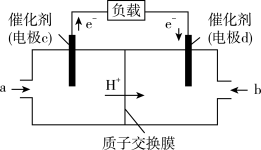
(3)CO与H2反应还可制备CH3OH,CH3OH可作为燃料使用,用CH3OH和O2组合形成的质子交换膜燃料电池的结构示意图如图:电池总反应为2CH3OH+3O2=2CO2+4H2O,则d电极是______ (填“正极”或“负极”)。若线路中转移1mol电子,则上述CH3OH燃料电池消耗的O2在标准状况下的体积为____ L。

(1)若C为稀H2SO4,电流表指针发生偏转,B电极材料为Fe且作负极,则A电极上发生的电极反应式为
(2)若需将反应:Cu+2Fe3+=Cu2++2Fe2+设计成如图所示的原电池装置,则A(正极)极材料为
(3)CO与H2反应还可制备CH3OH,CH3OH可作为燃料使用,用CH3OH和O2组合形成的质子交换膜燃料电池的结构示意图如图:电池总反应为2CH3OH+3O2=2CO2+4H2O,则d电极是

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】
(1)现有如下两个反应:(A)NaOH+HCl=NaCl+H2O;(B)2FeCl3+Cu=2FeCl2+CuCl2,根据两反应本质,判断能设计成原电池的反应是___ (填字母)。
(2)选择适宜的材料和试剂将(1)中你的选择设计为一个原电池______ 。写出电池的正极电极反应式___  。
。
(3)氢氧燃料电池是一种不需要将还原剂和氧化剂全部储藏在电池内部的新型发电装置,是一种具有应用前景的绿色电源。如图为氢氧燃料电池原理示意图,按照此图的提示回答下列问题:
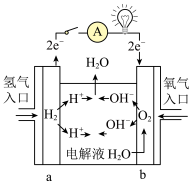
①该燃料电池的负极是___ (填“a”或“b”)。
②___ (填化学式)发生还原反应。
③总反应式是___ 。
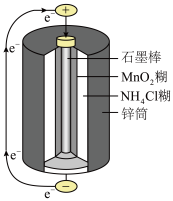
(4)锌锰干电池是最早使用的化学电池,其基本构造如图所示:锌锰干电池的负极是锌(Zn),电路中每通过0.4mole-,负极质量减少___ g;工作时NH 在正极放电产生两种气体,其中一种气体分子是10e-的微粒,正极的电极反应式是
在正极放电产生两种气体,其中一种气体分子是10e-的微粒,正极的电极反应式是___ 。
(1)现有如下两个反应:(A)NaOH+HCl=NaCl+H2O;(B)2FeCl3+Cu=2FeCl2+CuCl2,根据两反应本质,判断能设计成原电池的反应是
(2)选择适宜的材料和试剂将(1)中你的选择设计为一个原电池
 。
。(3)氢氧燃料电池是一种不需要将还原剂和氧化剂全部储藏在电池内部的新型发电装置,是一种具有应用前景的绿色电源。如图为氢氧燃料电池原理示意图,按照此图的提示回答下列问题:

①该燃料电池的负极是
②
③总反应式是
(4)锌锰干电池是最早使用的化学电池,其基本构造如图所示:锌锰干电池的负极是锌(Zn),电路中每通过0.4mole-,负极质量减少
 在正极放电产生两种气体,其中一种气体分子是10e-的微粒,正极的电极反应式是
在正极放电产生两种气体,其中一种气体分子是10e-的微粒,正极的电极反应式是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】从能量的变化和反应的快慢等角度研究反应:2H2+O2=2H2O。
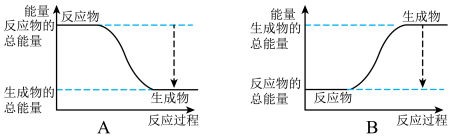
(1)下图能正确表示该反应中能量变化的是________ 。
(2)氢氧燃料电池的总反应方程式为2H2+O2=2H2O。其中,氢气在________ 极发生________ 反应。电路中每转移0.2 mol电子,标准状况下消耗H2的体积是________ L。
(3)理论上讲,任何自发的氧化还原反应都可以设计成原电池,请你利用下列反应“Cu+2Ag+=Cu2++2Ag”设计一个化学电池,并回答下列问题:
①该电池的正极材料是______ ,负极材料是 ______ ,电解质溶液是 ______ 。
②正极上出现的现象是______ ,负极上出现的现象是 ______ 。
(1)下图能正确表示该反应中能量变化的是

(2)氢氧燃料电池的总反应方程式为2H2+O2=2H2O。其中,氢气在
(3)理论上讲,任何自发的氧化还原反应都可以设计成原电池,请你利用下列反应“Cu+2Ag+=Cu2++2Ag”设计一个化学电池,并回答下列问题:
①该电池的正极材料是
②正极上出现的现象是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】人们应用原电池原理制作了多种电池,以满足不同的需要。请根据题中提供的信息,填写空格。
(1)FeCl3溶液常用于腐蚀印刷电路铜板,发生2FeCl3+Cu=2FeCl2+CuCl2,若将此反应设计成原电池,则负极所用电极材料为(填化学式):___________ ;当线路中转移0.4 mol电子时,则被腐蚀铜的质量为:___________ g。
(2)锂锰电池的体积小、性能优良,是常用的一次电池。该电池反应原理如图所示,其中电解质LiClO4,溶于混合有机溶剂中,Li+通过电解质迁移入MnO2晶格中,生成LiMnO2。
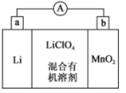
①电子流动方向是由___________ 极流向___________ 极(填字母)。
②电池正极反应式为___________ 。
③是否可用水代替电池中的混合有机溶剂?___________ (填“是”或“否”),原因是___________ 。
(3)近几年开发的甲烷—氧气燃料电池采用铂作电极催化剂,用KOH作为电池中的电解液。则通入CH4的电极为___________ 极(填“正”或“负”),通入O2的电极反应为___________ 。
(1)FeCl3溶液常用于腐蚀印刷电路铜板,发生2FeCl3+Cu=2FeCl2+CuCl2,若将此反应设计成原电池,则负极所用电极材料为(填化学式):
(2)锂锰电池的体积小、性能优良,是常用的一次电池。该电池反应原理如图所示,其中电解质LiClO4,溶于混合有机溶剂中,Li+通过电解质迁移入MnO2晶格中,生成LiMnO2。

①电子流动方向是由
②电池正极反应式为
③是否可用水代替电池中的混合有机溶剂?
(3)近几年开发的甲烷—氧气燃料电池采用铂作电极催化剂,用KOH作为电池中的电解液。则通入CH4的电极为
您最近一年使用:0次

 Na2Sx,正极的电极反应式为
Na2Sx,正极的电极反应式为


