Ⅰ.如下图所示,将2molA气体和1molB气体充入一容积可变的密闭容器中,发生反应:2A(g)+B(g) 2C(g).反应开始时可滑动的活塞的位置如甲图所示,当反应达到平衡时,活塞位置如乙图所示。则当达到平衡时,A的转化率为
2C(g).反应开始时可滑动的活塞的位置如甲图所示,当反应达到平衡时,活塞位置如乙图所示。则当达到平衡时,A的转化率为__________ ;该条件下的反应的平衡常数为_____________ 。

Ⅱ.(1)已知298K时,1molC2H6在氧气中完全燃烧生成二氧化碳和液态水,放出热量1558.3KJ。写出该反应的热化学方程式_____________________________ 。
(2)利用该反应可设计一个燃料电池:用氢氧化钾溶液做电解质溶液,用多孔石墨做电极,在电极上分别充入乙烷和氧气。写出负极的电极反应式_______________ 。
(3)用石墨做阳极,铁棒做阴极,电解硫酸铜溶液,则石墨棒上的电极反应式为________________________ ;如果起始时盛有1000mL PH=5的硫酸铜溶液(25℃)(足量),一段时间后溶液的PH变为1,若要使溶液恢复到起始浓度(忽略溶液体积变化),可向溶液中加入__________ (填物质名称),其质量约为___________ 。
 2C(g).反应开始时可滑动的活塞的位置如甲图所示,当反应达到平衡时,活塞位置如乙图所示。则当达到平衡时,A的转化率为
2C(g).反应开始时可滑动的活塞的位置如甲图所示,当反应达到平衡时,活塞位置如乙图所示。则当达到平衡时,A的转化率为
Ⅱ.(1)已知298K时,1molC2H6在氧气中完全燃烧生成二氧化碳和液态水,放出热量1558.3KJ。写出该反应的热化学方程式
(2)利用该反应可设计一个燃料电池:用氢氧化钾溶液做电解质溶液,用多孔石墨做电极,在电极上分别充入乙烷和氧气。写出负极的电极反应式
(3)用石墨做阳极,铁棒做阴极,电解硫酸铜溶液,则石墨棒上的电极反应式为
2010高二上·辽宁大连·竞赛 查看更多[1]
(已下线)2010届辽宁省大连协作体高二上学期竞赛(理综)化学部分
更新时间:2016-12-09 01:25:35
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】(1)拆开1 mol H-H键、1 mol N-H键、1 mol N≡N键需要的能量分别是436 kJ、391 kJ、946 kJ,则1 mol N2生成NH3的反应热为__________ ,1 mol H2生成NH3的反应热为__________ 。
(2) 写出298 K 101 kPa时,用CO(g)还原1 mol Fe2O3(s),放热24.8 kJ的热化学方程式:________________________________________________________ 。
(3) 已知N2(g)+2O2(g)====2 NO2(g);△H=+67.7 kJ·mol-1,
N2H4(g)+O2(g)=== N2(g)+2H2O (g);△H=-534 kJ·mol-1,根据盖斯定律写出肼与NO2完全反应生成氮气和气态水的热化学方程式_________________________________ 。
(2) 写出298 K 101 kPa时,用CO(g)还原1 mol Fe2O3(s),放热24.8 kJ的热化学方程式:
(3) 已知N2(g)+2O2(g)====2 NO2(g);△H=+67.7 kJ·mol-1,
N2H4(g)+O2(g)=== N2(g)+2H2O (g);△H=-534 kJ·mol-1,根据盖斯定律写出肼与NO2完全反应生成氮气和气态水的热化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】(1)肼(N2H4)是火箭推进器中常用的高能燃料,已知0.4 mol液态肼和足量H2O2反应,生成N2和水蒸气,放出256. 65kJ的热量,请写出该反应的热化学方程式:__________ 。
(2)工业上制氢气的一个重要反应是:CO(g) +H2O(g)=CO2(g)+H2(g)
已知在25℃时:C(石墨)+ O2(g)=CO(g) △H1=-111kJ·mol-1
O2(g)=CO(g) △H1=-111kJ·mol-1
H2(g)+ O2(g)=H2O(g) △H2=-242 kJ·mol-1
O2(g)=H2O(g) △H2=-242 kJ·mol-1
C(石墨)+O2(g)=CO2(g) △H3=-394kJ·mol-1
试计算25℃时一氧化碳与水作用转化为氢气和二氧化碳反应的反应热△H=______ kJ·mol-1
(3)CO2再在自然界循环时可与CaCO3反应,CaCO3是一种难溶物质,其Ksp=2.8×10-9。CaCl2溶液与NaCO3溶液混合可形成CaCO3沉淀,现将等体积的CaCl2溶液与Na2CO3溶液混合,若Na2CO3溶液的浓度为2×10-4mol / L ,则生成沉淀所需CaCl2溶液的最小浓度为__________ 。
(2)工业上制氢气的一个重要反应是:CO(g) +H2O(g)=CO2(g)+H2(g)
已知在25℃时:C(石墨)+
 O2(g)=CO(g) △H1=-111kJ·mol-1
O2(g)=CO(g) △H1=-111kJ·mol-1H2(g)+
 O2(g)=H2O(g) △H2=-242 kJ·mol-1
O2(g)=H2O(g) △H2=-242 kJ·mol-1C(石墨)+O2(g)=CO2(g) △H3=-394kJ·mol-1
试计算25℃时一氧化碳与水作用转化为氢气和二氧化碳反应的反应热△H=
(3)CO2再在自然界循环时可与CaCO3反应,CaCO3是一种难溶物质,其Ksp=2.8×10-9。CaCl2溶液与NaCO3溶液混合可形成CaCO3沉淀,现将等体积的CaCl2溶液与Na2CO3溶液混合,若Na2CO3溶液的浓度为2×10-4mol / L ,则生成沉淀所需CaCl2溶液的最小浓度为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】回答下列问题
(1)为了研究化学反应A+B=C+D的能量变化情况,某同学设计了如图所示装置。当向盛有A的试管中滴加试剂B时,看到U形管中甲处液面下降乙处液面上升。试回答下列问题:
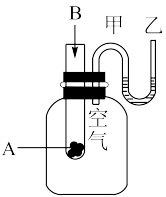
①该反应为___________ 反应(填“放热”或“吸热”)。
②A和B的总能量比C和D的总能量___________ (填“高”或“低”)。
(2)完成下列反应的热化学方程式。
已知:
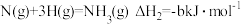
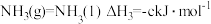
写出 和
和 反应生成液氨的热化学方程式
反应生成液氨的热化学方程式___________ 。
(3)写出 在水溶液中的电离方程式
在水溶液中的电离方程式___________ 。
(4)写出 的水解方程式
的水解方程式___________ 。
(1)为了研究化学反应A+B=C+D的能量变化情况,某同学设计了如图所示装置。当向盛有A的试管中滴加试剂B时,看到U形管中甲处液面下降乙处液面上升。试回答下列问题:

①该反应为
②A和B的总能量比C和D的总能量
(2)完成下列反应的热化学方程式。
已知:

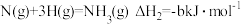
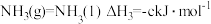
写出
 和
和 反应生成液氨的热化学方程式
反应生成液氨的热化学方程式(3)写出
 在水溶液中的电离方程式
在水溶液中的电离方程式(4)写出
 的水解方程式
的水解方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】氢能是一种极具发展潜力的清洁能源。下列反应是目前大规模制取氢气的方法之一、
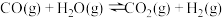
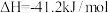
(1)在生产中,欲使CO的转化率提高,同时提高 的产率,可采取哪些措施
的产率,可采取哪些措施___________ ?
(2)在容积不变的密闭容器中,将2.0molCO与8.0mol 混合加热到830℃发生上述反应,达到平衡时CO的转化率是80%。计算该反应的平衡常数
混合加热到830℃发生上述反应,达到平衡时CO的转化率是80%。计算该反应的平衡常数___________ 。
(3)实验发现,其他条件不变,在相同时间内,向上述体系中投入一定量的CaO可以明显提高 的体积分数。对比实验的结果如图所示。
的体积分数。对比实验的结果如图所示。
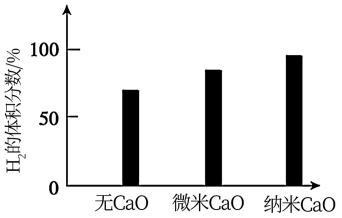
请思考:投入CaO时, 的体积分数为什么会增大
的体积分数为什么会增大___________ ?微米CaO和纳米CaO对平衡的影响为何不同___________ ?
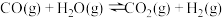
(1)在生产中,欲使CO的转化率提高,同时提高
 的产率,可采取哪些措施
的产率,可采取哪些措施(2)在容积不变的密闭容器中,将2.0molCO与8.0mol
 混合加热到830℃发生上述反应,达到平衡时CO的转化率是80%。计算该反应的平衡常数
混合加热到830℃发生上述反应,达到平衡时CO的转化率是80%。计算该反应的平衡常数(3)实验发现,其他条件不变,在相同时间内,向上述体系中投入一定量的CaO可以明显提高
 的体积分数。对比实验的结果如图所示。
的体积分数。对比实验的结果如图所示。
请思考:投入CaO时,
 的体积分数为什么会增大
的体积分数为什么会增大
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】恒温恒容下,将2 mol A气体和2 mol B气体通入体积为2 L的密闭容器中发生如下反应:2A(g)+B(g) xC(g)+2D(s),2 min时反应达到平衡状态,此时剩余1.2 mol B,并测得C的浓度为1.2 mol·L-1。
xC(g)+2D(s),2 min时反应达到平衡状态,此时剩余1.2 mol B,并测得C的浓度为1.2 mol·L-1。
(1)从开始反应至达到平衡状态,生成C的平均反应速率为_______________ 。
(2)x=________ 。
(3)A的转化率为_____________ 。
(4)下列各项可作为该反应达到平衡状态的标志的是________ 。
A.压强不再变化
B.气体密度不再变化
C.气体的平均相对分子质量不再变化
D.A的消耗速率与B的消耗速率之比为2∶1
 xC(g)+2D(s),2 min时反应达到平衡状态,此时剩余1.2 mol B,并测得C的浓度为1.2 mol·L-1。
xC(g)+2D(s),2 min时反应达到平衡状态,此时剩余1.2 mol B,并测得C的浓度为1.2 mol·L-1。(1)从开始反应至达到平衡状态,生成C的平均反应速率为
(2)x=
(3)A的转化率为
(4)下列各项可作为该反应达到平衡状态的标志的是
A.压强不再变化
B.气体密度不再变化
C.气体的平均相对分子质量不再变化
D.A的消耗速率与B的消耗速率之比为2∶1
您最近一年使用:0次
【推荐3】在一定体积的密闭容器内发生某气体体系反应,根据如图填空。
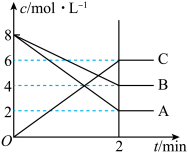
(1)反应物是___ ,生成物是____ 。
(2)在2min内A的平均反应速率为___ mol·L-1·min-1。
(3)该反应的化学方程式是__ 
___ 。
(4)写出此反应的平衡常数表达式___ (用物质A、B、C表示),增大压强,平衡向___ (填“正”或“逆”)反应方向移动,K___ (填“增大”、“减小”或“不变”)。
(5)转化率为已反应的物质的量与初始物质的量比值,B的转化率为___ ,若升高温度,B的转化率增加,则正反应是___ (填“吸热”或“放热”)。
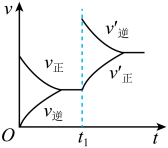
(6)2分钟后的某时刻(t1)改变某一条件使平衡移动,符合如图所示的条件是___ 。

(1)反应物是
(2)在2min内A的平均反应速率为
(3)该反应的化学方程式是

(4)写出此反应的平衡常数表达式
(5)转化率为已反应的物质的量与初始物质的量比值,B的转化率为
(6)2分钟后的某时刻(t1)改变某一条件使平衡移动,符合如图所示的条件是

您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】我国古代青铜器工艺精湛,有很高的艺术价值和历史价值,但出土的青铜器因受到环境腐蚀,欲对其进行修复和防护具有重要意义。图为青铜器在潮湿环境中发生的电化学腐蚀的示意图。
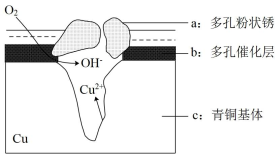
①腐蚀过程中,负极是_____ (填图中字母“a”或“b”或“c”)
②环境中的Clˉ̄扩散到孔口,并与正极反应产物和负极反应产物作用生成多孔铜锈Cu2(OH)3Cl,其离子方程式为_____ ;
③若生成4.29 g Cu2(OH)3Cl,则理论上耗氧体积为_____ L(标准状况)。

①腐蚀过程中,负极是
②环境中的Clˉ̄扩散到孔口,并与正极反应产物和负极反应产物作用生成多孔铜锈Cu2(OH)3Cl,其离子方程式为
③若生成4.29 g Cu2(OH)3Cl,则理论上耗氧体积为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】I.某温度时,在2 L密闭容器中,三种气态物质X、Y、Z的物质的量(n)随时间(t)变化的曲线如图所示,由图中数据分析可得:
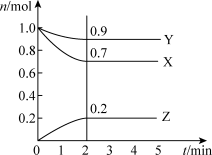
(1)该反应的化学方程式为_______ 。
(2)反应开始至2 min,用Y表示的平均反应速率为_______ 。
II.电化学技术是有效解决 CO、SO2、NOx 等大气污染的重要方法,某兴趣小组以SO2为原料,采用电化学方法制取硫酸,装置如下 :

(3)电解质溶液中 离子向
离子向_______ (填“A极”或“B极” )移动。
(4)请写出负极电极反应式_______ 。
(5)用该原电池做电源,石墨做电极电解2L AgNO3和KNO3混合溶液,通电一段时间,两极均产生2.24 L(标准状况)气体,假设电解前后溶液体积不变,则电解后溶液中H+的浓度为_______ ,析出银的质量_______ g。
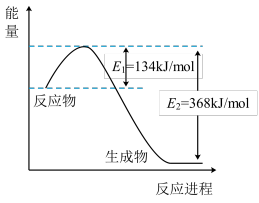
(6)如图是 1 mol NO2(g)和1 mol CO(g)反应生成 1 mol CO2(g)和 1 mol NO(g)过程中能量变化示意图。请写出反应的热化学方程式_______ 。

(1)该反应的化学方程式为
(2)反应开始至2 min,用Y表示的平均反应速率为
II.电化学技术是有效解决 CO、SO2、NOx 等大气污染的重要方法,某兴趣小组以SO2为原料,采用电化学方法制取硫酸,装置如下 :

(3)电解质溶液中
 离子向
离子向(4)请写出负极电极反应式
(5)用该原电池做电源,石墨做电极电解2L AgNO3和KNO3混合溶液,通电一段时间,两极均产生2.24 L(标准状况)气体,假设电解前后溶液体积不变,则电解后溶液中H+的浓度为
(6)如图是 1 mol NO2(g)和1 mol CO(g)反应生成 1 mol CO2(g)和 1 mol NO(g)过程中能量变化示意图。请写出反应的热化学方程式

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】回答下列问题:
(1)科研人员研究出一种方法,可实现水泥生产时CO2的零排放,其基本原理如图1所示;电解反应在温度小于900℃时进行,碳酸钙先分解为CaO和CO2,电解质为熔融碳酸钠,阳极的电极反应式为2CO -4e-=2CO2↑+O2↑,则阴极的电极反应式为
-4e-=2CO2↑+O2↑,则阴极的电极反应式为_____ 。
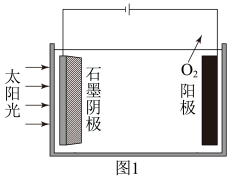
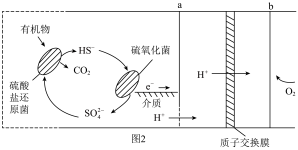
(2)微生物燃料电池是在微生物的作用下将化学能转化为电能的装置。某微生物燃料电池的工作原理如图2所示,其中HS-在硫氧化菌作用下转化为SO 的电极反应式是
的电极反应式是_____ 。
(3)①利用原电池检测CO的原理如图3所示,负极反应式为______ ,正极反应式为_____ ,电池总反应式为______ 。

②废气中NH3的发电原理如图4所示,则负极反应式为______ ,正极反应式为_____ 。电池总反应式为_____ 。

(1)科研人员研究出一种方法,可实现水泥生产时CO2的零排放,其基本原理如图1所示;电解反应在温度小于900℃时进行,碳酸钙先分解为CaO和CO2,电解质为熔融碳酸钠,阳极的电极反应式为2CO
 -4e-=2CO2↑+O2↑,则阴极的电极反应式为
-4e-=2CO2↑+O2↑,则阴极的电极反应式为
(2)微生物燃料电池是在微生物的作用下将化学能转化为电能的装置。某微生物燃料电池的工作原理如图2所示,其中HS-在硫氧化菌作用下转化为SO
 的电极反应式是
的电极反应式是
(3)①利用原电池检测CO的原理如图3所示,负极反应式为

②废气中NH3的发电原理如图4所示,则负极反应式为

您最近一年使用:0次



