燃料电池是一种新能源。利用2CO+O2═2CO2设计燃料电池时,负极发生反应的气体是__ ,正极发生反应的气体是__ 。
更新时间:2020-06-29 01:33:50
|
相似题推荐
填空题
|
容易
(0.94)
名校
【推荐1】Ⅰ.反应Fe+H2SO4=FeSO4+H2↑的能量变化如图所示:
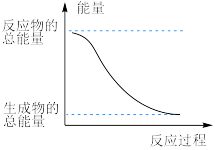
(1)该反应为___________ 反应(填“吸热”或“放热”)。
(2)若将上述反应设计成原电池,铜为原电池某一极材料,则铜为___________ (填“正”或“负”)极;其电极反应式为:___________ ,外电路中电流由___________ 流出。(填电极材料名称)。
(3)若要使该反应的反应速率加快,下列措施可行的是________ ;原因是________ 。
A.增加铁的量 B.改稀硫酸为98%的硫酸
C.增大压强 D.滴加几滴CuSO4溶液
Ⅱ.在一定温度下将2molA气体和4molB气体在2L密闭容器中混合并发生反应:A(g)+2B(g) 3C(g)+D(s)。若经2min后测得C的浓度为0.6mol·L-1,则:
3C(g)+D(s)。若经2min后测得C的浓度为0.6mol·L-1,则:
(4)用物质A表示的反应速率为___________ 。
(5)2min时物质B的浓度为___________ 。

(1)该反应为
(2)若将上述反应设计成原电池,铜为原电池某一极材料,则铜为
(3)若要使该反应的反应速率加快,下列措施可行的是
A.增加铁的量 B.改稀硫酸为98%的硫酸
C.增大压强 D.滴加几滴CuSO4溶液
Ⅱ.在一定温度下将2molA气体和4molB气体在2L密闭容器中混合并发生反应:A(g)+2B(g)
 3C(g)+D(s)。若经2min后测得C的浓度为0.6mol·L-1,则:
3C(g)+D(s)。若经2min后测得C的浓度为0.6mol·L-1,则:(4)用物质A表示的反应速率为
(5)2min时物质B的浓度为
您最近一年使用:0次
填空题
|
容易
(0.94)
【推荐2】以锌片,铜片为电极,稀硫酸为电解质溶液组成原电池。
(1)该原电池的负极为
(2)该原电池的正极为
您最近一年使用:0次
填空题
|
容易
(0.94)
【推荐1】燃料电池
氢氧燃料电池的构造:氢气在___________ 极室通入,氧气在___________ 极室通入。
氢氧燃料电池的构造:氢气在
您最近一年使用:0次
填空题
|
容易
(0.94)
【推荐2】为体现绿色世博、低碳世博、科技世博,上海世博会已经开始使用中国自己生产的燃料电池汽车,该车以氢气和空气中的氧气为燃料,KOH为电解质溶液,真正实现了“零排放”。该电池的负极反应式为________________________ ,从能量角度分析氢气用作燃料电池与直接燃烧相比主要优点______________________________ 。
您最近一年使用:0次
填空题
|
容易
(0.94)
名校
解题方法
【推荐3】科学家预言,燃料电池将是21世纪获得电能的重要途径。近几年开发的甲醇燃料电池是采用铂作电极催化剂,电池中的质子交换膜只允许质子(就是H+)和水分子通过。其工作原理的示意图如下图,请回答下列问题:
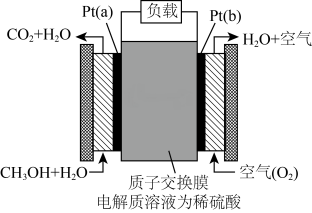
(1)该装置的能量转化形式为__________ 。
(2)Pt(a)电极是电池的_____ (填“正”或“负”)极。
(3)电解液中的H+向_________ (填“a”或“b")极移动。
(4)如果该电池工作时消耗1 mol CH3OH,则电路中通过______ mol电子,其通入空气(O2)一极的电极反应式为_______ 。
(5)比起直接燃烧燃料产生电力,使用燃料电池有许多优点,其中主要有两点:首先是燃料电池的能量转化率高,其次是__________ 。

(1)该装置的能量转化形式为
(2)Pt(a)电极是电池的
(3)电解液中的H+向
(4)如果该电池工作时消耗1 mol CH3OH,则电路中通过
(5)比起直接燃烧燃料产生电力,使用燃料电池有许多优点,其中主要有两点:首先是燃料电池的能量转化率高,其次是
您最近一年使用:0次



