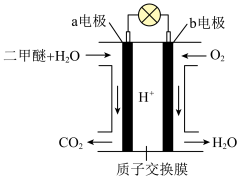
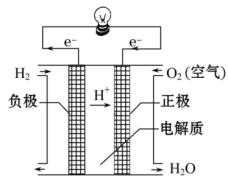
科学家预言,燃料电池将是21世纪获得电能的重要途径。近几年开发的甲醇燃料电池是采用铂作电极催化剂,电池中的质子交换膜只允许质子(就是H+)和水分子通过。其工作原理的示意图如下图,请回答下列问题:
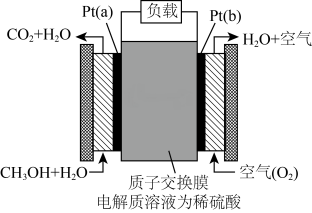
(1)该装置的能量转化形式为__________ 。
(2)Pt(a)电极是电池的_____ (填“正”或“负”)极。
(3)电解液中的H+向_________ (填“a”或“b")极移动。
(4)如果该电池工作时消耗1 mol CH3OH,则电路中通过______ mol电子,其通入空气(O2)一极的电极反应式为_______ 。
(5)比起直接燃烧燃料产生电力,使用燃料电池有许多优点,其中主要有两点:首先是燃料电池的能量转化率高,其次是__________ 。

(1)该装置的能量转化形式为
(2)Pt(a)电极是电池的
(3)电解液中的H+向
(4)如果该电池工作时消耗1 mol CH3OH,则电路中通过
(5)比起直接燃烧燃料产生电力,使用燃料电池有许多优点,其中主要有两点:首先是燃料电池的能量转化率高,其次是
更新时间:2020-08-07 10:58:52
|
相似题推荐
填空题
|
容易
(0.94)
名校
解题方法
【推荐1】依据氧化还原反应:2Ag+(aq) +Cu(s) =Cu2+(aq) +2Ag(s)设计的原电池如图所示。请回答下列问题:
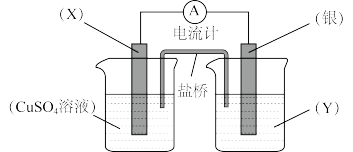
(1)电解质溶液Y是___________ ;
(2)银电极为电池的___________ 极,发生的电极反应为___________
(3)外电路中的电子是从___________ 电极流向___________ 电极。

(1)电解质溶液Y是
(2)银电极为电池的
(3)外电路中的电子是从
您最近一年使用:0次
填空题
|
容易
(0.94)
名校
解题方法
【推荐2】如图是一个原电池装置,请按要求填空。
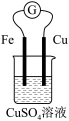
(1)正极材料是___________ ,负极材料是___________ 。
(2)电子的流向是由___________ (填“Fe”或“Cu”,不同)极经外电路流向___________ 极。
(3)写出电极反应式:负极___________ ,正极___________ 。
(4)该原电池中发生的总反应离子方程式为___________ 。

(1)正极材料是
(2)电子的流向是由
(3)写出电极反应式:负极
(4)该原电池中发生的总反应离子方程式为
您最近一年使用:0次
填空题
|
容易
(0.94)
名校
解题方法
【推荐1】燃料电池是一种新能源。利用2CO+O2═2CO2设计燃料电池时,负极发生反应的气体是__ ,正极发生反应的气体是__ 。
您最近一年使用:0次
填空题
|
容易
(0.94)
【推荐2】燃料电池
氢氧燃料电池的构造:氢气在___________ 极室通入,氧气在___________ 极室通入。
氢氧燃料电池的构造:氢气在
您最近一年使用:0次
填空题
|
容易
(0.94)
【推荐3】燃料电池
一种将燃料(如氢气、甲烷、乙醇)和氧化剂(如氧气)的化学能直接转化为电能的电化学反应装置
特点:清洁、安全、高效;能量转化率可以达到80%以上;反应物不是储存在电池内部,而是从外部提供,供电量易于调节。
燃料电池与一般的电池不同的是,反应物不是储存在____ ,而是由外部提供,电池装置起着类似于试管、烧杯等反应容器的作用。
工作原理:利用原电池的工作原理将燃料(如H2)和氧化剂(如O2)分别在两个电极上反应所放出的化学能直接转化为__ 。(实验装置如下)
一种将燃料(如氢气、甲烷、乙醇)和氧化剂(如氧气)的化学能直接转化为电能的电化学反应装置
特点:清洁、安全、高效;能量转化率可以达到80%以上;反应物不是储存在电池内部,而是从外部提供,供电量易于调节。
燃料电池与一般的电池不同的是,反应物不是储存在
工作原理:利用原电池的工作原理将燃料(如H2)和氧化剂(如O2)分别在两个电极上反应所放出的化学能直接转化为

您最近一年使用:0次
填空题
|
容易
(0.94)
【推荐1】2009年10月1日,我国成功举办国庆六十年阅兵活动。其中阅兵仪式上9辆电动车与混合动力车等新能源车辆的亮相,展示了综合国力、国防科技发展水平。同时也说明能源短缺是人类社会面临的重大问题。甲醇是一种可再生能源,具有广泛的开发和应用前景。
(1)工业上一般采用下列两种反应合成甲醇:
反应Ⅰ: CO(g) + 2H2(g) CH3OH(g) ΔH1
CH3OH(g) ΔH1
反应Ⅱ: CO2(g) + 3H2(g) CH3OH(g) + H2O(g) ΔH2
CH3OH(g) + H2O(g) ΔH2
①上述反应符合“原子经济”原则的是 _____(填“Ⅰ”或“Ⅱ”)。
②下表所列数据是反应Ⅰ在不同温度下的化学平衡常数(K)。
由表中数据判断ΔH1 0 (填“>”、“=”或“<”)。
③某温度下,将2 mol CO和6 mol H2充入2L的密闭容器中,充分反应,达到平衡后,测得c(CO)= 0.2 mol/L,则CO的转化率为 ,此时的温度为 (从上表中选择)。
(2)已知在常温常压下:
① 2CH3OH(l) + 3O2(g) = 2CO2(g) + 4H2O(g) ΔH1=-1275.6 kJ/mol
② 2CO (g)+ O2(g) = 2CO2(g) ΔH2=-566.0 kJ/mol
③ H2O(g) = H2O(l) ΔH3=-44.0 kJ/mol
写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式:
(3)某实验小组依据甲醇燃烧的反应原理,
①设计如图所示的电池装置。该电池正极的电极反应为 。
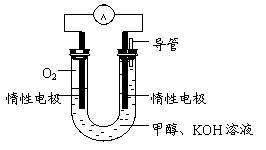
②工作一段时间后,测得溶液的pH减小,该电池总反应的化学方程式为
。
(1)工业上一般采用下列两种反应合成甲醇:
反应Ⅰ: CO(g) + 2H2(g)
 CH3OH(g) ΔH1
CH3OH(g) ΔH1反应Ⅱ: CO2(g) + 3H2(g)
 CH3OH(g) + H2O(g) ΔH2
CH3OH(g) + H2O(g) ΔH2①上述反应符合“原子经济”原则的是 _____(填“Ⅰ”或“Ⅱ”)。
②下表所列数据是反应Ⅰ在不同温度下的化学平衡常数(K)。
| 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |
由表中数据判断ΔH1 0 (填“>”、“=”或“<”)。
③某温度下,将2 mol CO和6 mol H2充入2L的密闭容器中,充分反应,达到平衡后,测得c(CO)= 0.2 mol/L,则CO的转化率为 ,此时的温度为 (从上表中选择)。
(2)已知在常温常压下:
① 2CH3OH(l) + 3O2(g) = 2CO2(g) + 4H2O(g) ΔH1=-1275.6 kJ/mol
② 2CO (g)+ O2(g) = 2CO2(g) ΔH2=-566.0 kJ/mol
③ H2O(g) = H2O(l) ΔH3=-44.0 kJ/mol
写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式:
(3)某实验小组依据甲醇燃烧的反应原理,
①设计如图所示的电池装置。该电池正极的电极反应为 。

②工作一段时间后,测得溶液的pH减小,该电池总反应的化学方程式为
。
您最近一年使用:0次
填空题
|
容易
(0.94)
名校
【推荐2】近年来甲醇用途日益广泛,越来越引起商家的关注,工业上甲醇的合成途径多种多样。现有实验室中模拟甲醇合成反应,在2 L密闭容器内,400 ℃时反应:CO(g)+2H2(g) CH3OH(g) △H<0,体系中n(CO)随时间的变化如表:
CH3OH(g) △H<0,体系中n(CO)随时间的变化如表:
(1)图中表示CH3OH的变化的曲线是_______ 。
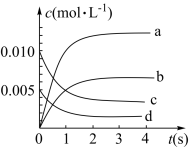
(2)用H2表示从0~2s内该反应的平均速率v(H2)=_______ 。
(3)能说明该反应已达到平衡状态的是_______ 。
a.反应中CO与CH3OH的物质的量之比为1:1
b.容器内压强保持不变
c.2v逆(CO)=v正(H2)
d.单位时间内每消耗1molCO,同时生成1molCH3OH
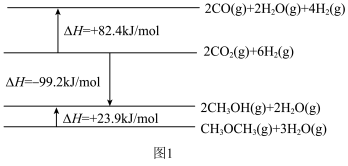
(4)CH3OH与O2的反应可将化学能转化为电能,工作原理如图所示,则CH3OH应从_______ (填A或B)通入,K+移向 _______ (填a、b极) 当电路中累计有2mol电子通过时,消耗的氧气体积为(在标准状况下)_______ L

 CH3OH(g) △H<0,体系中n(CO)随时间的变化如表:
CH3OH(g) △H<0,体系中n(CO)随时间的变化如表:| 时间(s) | 0 | 1 | 2 | 3 | 5 |
| n(CO)(mol) | 0.020 | 0.011 | 0.008 | 0.007 | 0.007 |

(2)用H2表示从0~2s内该反应的平均速率v(H2)=
(3)能说明该反应已达到平衡状态的是
a.反应中CO与CH3OH的物质的量之比为1:1
b.容器内压强保持不变
c.2v逆(CO)=v正(H2)
d.单位时间内每消耗1molCO,同时生成1molCH3OH
(4)CH3OH与O2的反应可将化学能转化为电能,工作原理如图所示,则CH3OH应从

您最近一年使用:0次
填空题
|
容易
(0.94)
名校
解题方法
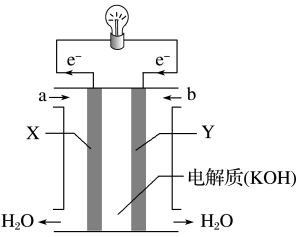
【推荐1】回答下列问题:
(1)如图为氢氧燃料电池的构造示意图,根据电子运动方向,可知氧气从___________ 口通入(填“a”或“b”),X极为电池的___________ (填“正”或“负”)极,Y极的电极方程式为___________ 。
A极:2H2+2O2--4e-=2H2O
B极:O2+4e-=2O2-
则A极是电池的___________ 极;电子从该极___________ (填“流入”或“流出”)。
(3)微型纽扣电池在现代生活中有广泛应用,有一种银锌电池,其电极分别是Ag2O和Zn,电解质溶液为KOH溶液,电极反应为:
Zn+2OH-2e-=ZnO+H2O Ag2O+H2O+2e-=2Ag+2OH-
总反应为Ag2O+Zn=ZnO+2Ag
①Zn是___________ 极,Ag2O发生___________ 反应。
②电子由___________ 极流向___________ 极(填“Zn”或“Ag2O”),当电路通过1 mol电子时,负极消耗物质的质量是___________ g。
③在使用过程中,电解质溶液中KOH的物质的量___________ (填“增大”“减小”或“不变”)。
(1)如图为氢氧燃料电池的构造示意图,根据电子运动方向,可知氧气从
A极:2H2+2O2--4e-=2H2O
B极:O2+4e-=2O2-
则A极是电池的
(3)微型纽扣电池在现代生活中有广泛应用,有一种银锌电池,其电极分别是Ag2O和Zn,电解质溶液为KOH溶液,电极反应为:
Zn+2OH-2e-=ZnO+H2O Ag2O+H2O+2e-=2Ag+2OH-
总反应为Ag2O+Zn=ZnO+2Ag
①Zn是
②电子由
③在使用过程中,电解质溶液中KOH的物质的量
您最近一年使用:0次
填空题
|
容易
(0.94)
解题方法
【推荐2】铅蓄电池的电极分别是PbO2和Pb,电解质溶液为稀H2SO4溶液,工作时原电池的总反应式为PbO2+Pb+2H2SO4=2PbSO4+2H2O据上述变化判断:
①原电池的负极是_______ (填电极材料)。电极反应式_______
②工作时正极反应式为_______
③工作时电解质溶液的c(H+)_______ (填“增大”、“不变”或“减小”)
①原电池的负极是
②工作时正极反应式为
③工作时电解质溶液的c(H+)
您最近一年使用:0次


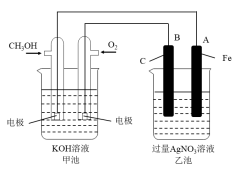
 催化加氢制二甲醚,可以实现
催化加氢制二甲醚,可以实现



 )燃料电池”的工作原理示意图(a、b均为多孔性
)燃料电池”的工作原理示意图(a、b均为多孔性 电极)。负极是
电极)。负极是 氢离子通过质子交换膜,则b电极在标准状况下吸收
氢离子通过质子交换膜,则b电极在标准状况下吸收 氧气。
氧气。