下图是元素周期表的一部分,根据① ~ ⑨在周期表中的位置按题目要求回答:
(1)画出⑩的原子结构示意图_________________________
(2)①与②形成的一种化合物甲,甲在大气含量过高会产生温室效应,写出甲物质的结构式__________________________________ 。
(3)元素③⑤对应的最高价氧化物的水化物,写出它们相互之间能发生反应化学方程式__________________ 。
(4)元素⑦和⑨形成的化合物乙,请用电子式表示物质乙的形成过程__________________ 。
(5)②、⑥分别形成的两种氢化物中,沸点较高的是______ (填化学式),原因是:___________________________________________________ 。
| 族 周期 | IA | 0 | ||||||||
| 1 | ⅡA | …… …… …… | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |||
| 2 | ① | ② | ||||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | |||||
| 4 | ⑧ | ⑨ | ⑩ | |||||||
(1)画出⑩的原子结构示意图
(2)①与②形成的一种化合物甲,甲在大气含量过高会产生温室效应,写出甲物质的结构式
(3)元素③⑤对应的最高价氧化物的水化物,写出它们相互之间能发生反应化学方程式
(4)元素⑦和⑨形成的化合物乙,请用电子式表示物质乙的形成过程
(5)②、⑥分别形成的两种氢化物中,沸点较高的是
19-20高一下·安徽六安·阶段练习 查看更多[2]
更新时间:2020-07-06 18:48:11
|
相似题推荐
解答题-无机推断题
|
较易
(0.85)
名校
【推荐1】下表是元素周期表的一部分,请参照元素①-⑩在表中的位置,回答下列问题。
(1)②的原子结构示意图是_______ 。
(2)化学性质最不活泼的元素是_______ (填元素符号,下同);形成化合物种类最多的元素_______ ,其最高价氧化物分子的空间构型为_______ 。(每空1分)
(3)在③、④、⑤、⑥这些元素形成的最简单离子中,离子半径由大到小的顺序是_______ 。(填离子符号)。
(4)在这些元素的最高价氧化物对应的水化物中,酸性最强的物质与碱性最强的物质在水溶液中发生的化学方程式为_______ ;⑥的单质与上面碱性最强的物质在水溶液中反应的离子方程式为_______ 。
(5)由元素③、⑤、⑨形成的一种常见的杀菌消毒剂中存在的化学键有_______ 。
(6)由元素⑧和⑨形成的某种化合物可表示为X2Y2(其中各原子均满足8电子稳定结构),写出X2Y2的电子式:_______ 。
| 族 周期 | IA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ① | ② | ③ | ④ | ||||
| 三 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
(2)化学性质最不活泼的元素是
(3)在③、④、⑤、⑥这些元素形成的最简单离子中,离子半径由大到小的顺序是
(4)在这些元素的最高价氧化物对应的水化物中,酸性最强的物质与碱性最强的物质在水溶液中发生的化学方程式为
(5)由元素③、⑤、⑨形成的一种常见的杀菌消毒剂中存在的化学键有
(6)由元素⑧和⑨形成的某种化合物可表示为X2Y2(其中各原子均满足8电子稳定结构),写出X2Y2的电子式:
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐2】短周期A、B、C、D 四种元素,原子序数依次增大 ,A原子的最外层上有4个电子;B的阴离子和C的阳离子具有相同的电子层结构,两元素的单质反应,可生成一种原子个数比为1:1的且不溶于水的固体E;D的L层电子数等于K、M两个电子层上电子数之和。
(1)A元素的名称为______________
(2)B原子的阴离子的结构示意图为_________________ 。
(3)C元素位于元素周期表中第________ 周期、第_______ 族。
(4) D的最高价氧化物对应的水化物化学式为:_______________________ 。
(5)写出A、D两元素形成化合物的电子式_____________________________________ 。
(1)A元素的名称为
(2)B原子的阴离子的结构示意图为
(3)C元素位于元素周期表中第
(4) D的最高价氧化物对应的水化物化学式为:
(5)写出A、D两元素形成化合物的电子式
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐3】下表列出了①~⑩号元素在元素周期表中的位置:
回答下列问题:
(1)①~⑩中,元素的化学性质最不活泼的是_______ (填元素符号,下同)。上述10种元素中,属于金属元素的有_______ 。
(2)写出①与④以原子个数比3∶1形成的化合物的电子式:_______ 。
(3)元素④、⑤、⑩分别和①组成的简单化合物中,最稳定的是_______ (填化学式)。
(4)从元素原子得、失电子的角度看,⑤的单质具有_______ (填“氧化性”或“还原性”)。
(5)元素①~⑩半径最大的是(②除外)_______ (填化学式)。
(6)在盛有氢氧化钠溶液的小烧杯中通入元素⑩的单质,发生反应的离子方程式为_______ 。
| 族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 一 | ① | ② | ||||||
| 二 | ③ | ④ | ⑤ | |||||
| 三 | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
(1)①~⑩中,元素的化学性质最不活泼的是
(2)写出①与④以原子个数比3∶1形成的化合物的电子式:
(3)元素④、⑤、⑩分别和①组成的简单化合物中,最稳定的是
(4)从元素原子得、失电子的角度看,⑤的单质具有
(5)元素①~⑩半径最大的是(②除外)
(6)在盛有氢氧化钠溶液的小烧杯中通入元素⑩的单质,发生反应的离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐1】下表是元素周期表的一部分,a~k分别代表10种元素,请按照要求回答:
(1)元素a~k中,其简单氢化物最稳定的是_______ (填元素名称)。
(2)b的简单氢化物的电子式_______ 。
(3)元素h、i的最高价氧化物对应水化物中酸性较强的是_______ (填化学式)。
(4)g的单质与e的最高价氧化物对应的水化物反应的化学方程式是_______ 。
(5)下列说法能证明金属性k强于f的是_______ (填序号)。
A.k的简单阳离子的氧化性更弱
B.k的氢氧化物水溶液的导电性更强
C.k的单质与水反应更剧烈
| a | ||||||||
| b | c | d | ||||||
| e | f | g | h | i | ||||
| k | …… | |||||||
(2)b的简单氢化物的电子式
(3)元素h、i的最高价氧化物对应水化物中酸性较强的是
(4)g的单质与e的最高价氧化物对应的水化物反应的化学方程式是
(5)下列说法能证明金属性k强于f的是
A.k的简单阳离子的氧化性更弱
B.k的氢氧化物水溶液的导电性更强
C.k的单质与水反应更剧烈
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐2】下表是元素周期表的一部分,请按要求回答下列问题:
(1)①元素的元素符号是_____ ;画出②原子结构示意图:____ 。
(2)①②③三种元素对应的简单氢化物中,最稳定的是_____ (填化学式,下同),④⑤两种元素的最高价氧化物对应的水化物中,碱性较强的是_____ 。
(3)⑥元素的最高价氧化物对应的水化物的化学式为____ ,④元素的单质与H2O反应的化学反应方程式_____ 。
(4)用电子式形式表示④⑦两元素化合物的形成过程:______ 。
| 族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 1 | ||||||||
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ |
(2)①②③三种元素对应的简单氢化物中,最稳定的是
(3)⑥元素的最高价氧化物对应的水化物的化学式为
(4)用电子式形式表示④⑦两元素化合物的形成过程:
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐3】下表是元素周期表的一部分,表中所列的字母分别代表某一化学元素。
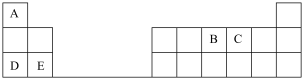
完成下列填空(填元素符号或化学式):
(1)元素C在元素周期表中的位置是__________ ,B、C、E三种元素原子半径从大到小的顺序是__________ ;
(2)D简单离子的结构示意图为______________ ,D的金属性________ E的金属性(填“大于”“小于”“等于”)。D单质在空气中燃烧可生成淡黄色粉末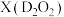 ,
, 的电子式为
的电子式为___________ ,D的最高价氧化物对应的水化物中含有的化学键类型有_________ 。
(3)将 、
、 的固体混合物完全溶于水,配制成溶液,然后向该溶液中逐滴加入
的固体混合物完全溶于水,配制成溶液,然后向该溶液中逐滴加入 的盐酸,所加盐酸的体积与产生
的盐酸,所加盐酸的体积与产生 的体积(标准状况)关系如图所示。
的体积(标准状况)关系如图所示。
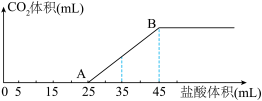
已知:逐滴将盐酸加入碳酸钠溶液中时,盐酸先与碳酸钠反应生成碳酸氢钠。
①AB段发生反应的离子方程式为____________ 。
②原固体混合物中 与
与 的物质的量之比为
的物质的量之比为____________ 。

完成下列填空(填元素符号或化学式):
(1)元素C在元素周期表中的位置是
(2)D简单离子的结构示意图为
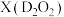 ,
, 的电子式为
的电子式为(3)将
 、
、 的固体混合物完全溶于水,配制成溶液,然后向该溶液中逐滴加入
的固体混合物完全溶于水,配制成溶液,然后向该溶液中逐滴加入 的盐酸,所加盐酸的体积与产生
的盐酸,所加盐酸的体积与产生 的体积(标准状况)关系如图所示。
的体积(标准状况)关系如图所示。
已知:逐滴将盐酸加入碳酸钠溶液中时,盐酸先与碳酸钠反应生成碳酸氢钠。
①AB段发生反应的离子方程式为
②原固体混合物中
 与
与 的物质的量之比为
的物质的量之比为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐1】短周期主族元素A、B、C、D、E、F在元素周期表中的位置如图所示,试回答下列问题:
(1)写出下列元素的元素符号:B___________ ,E___________ 。
(2)写出化合物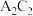 的结构式:
的结构式:___________ 。
(3)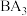 的电子式为
的电子式为___________ 。
(4)写出D的最高价氧化物对应的水化物与 反应的离子方程式:
反应的离子方程式:___________ 。
| A | |||||||
| B | C | ||||||
| D | E | F |
(2)写出化合物
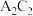 的结构式:
的结构式:(3)
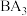 的电子式为
的电子式为(4)写出D的最高价氧化物对应的水化物与
 反应的离子方程式:
反应的离子方程式:
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
【推荐2】下表列出了①~⑧所分别代表的八种元素在周期表中的位置,按要求填写下列问题:
(1)①~⑧八种元素中金属性最强的元素是_______ (填元素符号)。
(2)元素②与①组成的某化合物,其分子为18电子体,分子中两种元素原子个数的最简比为1:2,则该分子的电子式为_______ 。
(3)元素⑧的原子结构示意图为_______ 。
(4)Mg和元素⑤的单质作电极材料,氢氧化钠溶液作电解质溶液,能设计成原电池,则该电池负极反应式为_______ 。
(5)写出碳单质与元素②最高价氧化物对应水化物的浓溶液反应的化学方程式_______ 。
(6)第118号元素与⑥为同族元素,它位于元素周期表第_______ 周期。
周期 族 | IA | 0 | ||||||
1 | ① | lIA | IIIA | IVA | VA | VIA | VIIA | |
2 | ② | ③ | ||||||
3 | ④ | ⑤ | ⑥ | |||||
4 | ⑦ | ⑧ |
(2)元素②与①组成的某化合物,其分子为18电子体,分子中两种元素原子个数的最简比为1:2,则该分子的电子式为
(3)元素⑧的原子结构示意图为
(4)Mg和元素⑤的单质作电极材料,氢氧化钠溶液作电解质溶液,能设计成原电池,则该电池负极反应式为
(5)写出碳单质与元素②最高价氧化物对应水化物的浓溶液反应的化学方程式
(6)第118号元素与⑥为同族元素,它位于元素周期表第
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
【推荐3】下表为元素周期表的一部分,请参照元素①-⑧在表中的位置,回答下列问题:
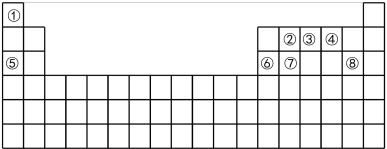
(1)写出元素⑥在周期表中的位置___________ 。
(2)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是___________ (填化学式)。
(3)元素①与④能组成一种质子数为10、电子数也为10的微粒,写出元素⑤的单质和该微粒反应的化学方程式:___________ 。
(4)写出实验室制取元素⑧的单质的化学方程式:___________ 。
(5)碘(Ⅰ)在元素周期表中位于ⅦA族,是人体必需的微量元素之一、下列事实能够用“碘的非金属性比氯的弱”来解释的是___________ (填标号)。
a.Cl2能使淀粉KI试纸变蓝 b.HClO3的酸性强于HIO3
c.Cl2比I2更容易与H2化合 d.HCl比HI更不易分解

(1)写出元素⑥在周期表中的位置
(2)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是
(3)元素①与④能组成一种质子数为10、电子数也为10的微粒,写出元素⑤的单质和该微粒反应的化学方程式:
(4)写出实验室制取元素⑧的单质的化学方程式:
(5)碘(Ⅰ)在元素周期表中位于ⅦA族,是人体必需的微量元素之一、下列事实能够用“碘的非金属性比氯的弱”来解释的是
a.Cl2能使淀粉KI试纸变蓝 b.HClO3的酸性强于HIO3
c.Cl2比I2更容易与H2化合 d.HCl比HI更不易分解
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐1】判断
(1)范德华力存在于任何物质中_____
(2)范德华力比化学键弱得多_____
(3)CH4、C2H6、C3H8的熔点、沸点依次升高_____
(4)HF、HCl、HBr、HI的稳定性依次减弱,是因为分子间作用力依次减弱_____
(5)卤素单质、卤素氢化物、卤素碳化物(即CX4)的熔、沸点均随着相对分子质量的增大而增大_____
(6)加热蒸发氯化钾水溶液的过程中有分子间作用力的破坏_____
(7)CO2溶于水和干冰升华都只有分子间作用力改变_____
(8)石墨转化为金刚石既有共价键的断裂和生成,也有分子间作用力的破坏_____
(1)范德华力存在于任何物质中
(2)范德华力比化学键弱得多
(3)CH4、C2H6、C3H8的熔点、沸点依次升高
(4)HF、HCl、HBr、HI的稳定性依次减弱,是因为分子间作用力依次减弱
(5)卤素单质、卤素氢化物、卤素碳化物(即CX4)的熔、沸点均随着相对分子质量的增大而增大
(6)加热蒸发氯化钾水溶液的过程中有分子间作用力的破坏
(7)CO2溶于水和干冰升华都只有分子间作用力改变
(8)石墨转化为金刚石既有共价键的断裂和生成,也有分子间作用力的破坏
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
【推荐2】(1)下列物质变化过程只与范德华力有关的是___________ (填标号)。
a.干冰熔化 b.乙酸汽化
c.石英熔化 d.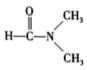 溶于水
溶于水
e.碘溶于四氯化碳
(2) 常温下为固体,熔点为282℃,沸点为315℃,在300℃以上升华,易溶于水,也易溶于乙醚、丙酮等有机溶剂。据此判断
常温下为固体,熔点为282℃,沸点为315℃,在300℃以上升华,易溶于水,也易溶于乙醚、丙酮等有机溶剂。据此判断 的晶体类型为
的晶体类型为___________ 。
(3)某石蕊分子的结构如图所示:
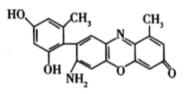
①石蕊分子所含元素中,基态原子2p轨道有两个未成对电子的是___________ (填元素符号);由其中两种元素形成的三角锥形结构的一价阳离子是___________ (填离子符号)。
②该石蕊易溶于水,分析可能的原因是___________ 。
(4)已知:Cu2++2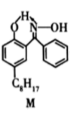 →
→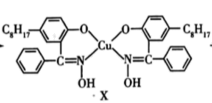 +2H+
+2H+
①基态 的核外电子排布式为
的核外电子排布式为___________ 。
②X难溶于水、易溶于有机溶剂,其晶体类型为___________ 。
③M中所含元素的电负性由大到小的顺序为___________ ,N原子以___________ 轨道与O原子形成 键。
键。
④上述反应中断裂和生成的化学键有___________ (填标号)。
a.离子键 b.配位键 c.金属键 d.范德华力 e.共价键
(5)白磷( )是磷的一种单质,它属于分子晶体,其晶胞结构如图所示。已知该晶体的密度为
)是磷的一种单质,它属于分子晶体,其晶胞结构如图所示。已知该晶体的密度为 ,晶胞的边长为acm,则阿伏加德罗常数为
,晶胞的边长为acm,则阿伏加德罗常数为___________ 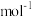 (用含ρ、a的式子表示)。
(用含ρ、a的式子表示)。
a.干冰熔化 b.乙酸汽化
c.石英熔化 d.
 溶于水
溶于水e.碘溶于四氯化碳
(2)
 常温下为固体,熔点为282℃,沸点为315℃,在300℃以上升华,易溶于水,也易溶于乙醚、丙酮等有机溶剂。据此判断
常温下为固体,熔点为282℃,沸点为315℃,在300℃以上升华,易溶于水,也易溶于乙醚、丙酮等有机溶剂。据此判断 的晶体类型为
的晶体类型为(3)某石蕊分子的结构如图所示:

①石蕊分子所含元素中,基态原子2p轨道有两个未成对电子的是
②该石蕊易溶于水,分析可能的原因是
(4)已知:Cu2++2
 →
→ +2H+
+2H+①基态
 的核外电子排布式为
的核外电子排布式为②X难溶于水、易溶于有机溶剂,其晶体类型为
③M中所含元素的电负性由大到小的顺序为
 键。
键。④上述反应中断裂和生成的化学键有
a.离子键 b.配位键 c.金属键 d.范德华力 e.共价键
(5)白磷(
 )是磷的一种单质,它属于分子晶体,其晶胞结构如图所示。已知该晶体的密度为
)是磷的一种单质,它属于分子晶体,其晶胞结构如图所示。已知该晶体的密度为 ,晶胞的边长为acm,则阿伏加德罗常数为
,晶胞的边长为acm,则阿伏加德罗常数为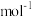 (用含ρ、a的式子表示)。
(用含ρ、a的式子表示)。
您最近一年使用:0次



