钢铁工业是国家工业的基础,钢铁生锈现象却随处可见,为此每年国家损失大量资金。
(1)钢铁腐蚀主要是吸氧腐蚀,该腐蚀过程中的正极电极反应式为:_____________
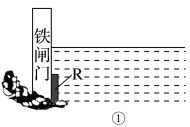
(2)为了降低某水库的铁闸门被腐蚀的速率,可以采用图①所示的方案,其中焊接在铁闸门上的固体材料R可以采用________ 。
A.铜 B.钠 C.锌 D.石墨
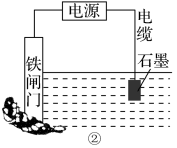
(3)图②所示的方案也可以降低铁闸门的腐蚀速率,其中铁闸门应该连接在直流电源的__________ 极。
(4)钢铁的防护除了用电化学保护方法之外,在钢铁制品表面镀铜也可以有效地防止其腐蚀,电镀的装置如图所示:
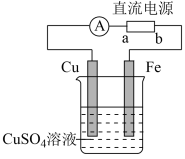
①电镀装置图的“直流电源”中,______  填“a”或“b”
填“a”或“b” 是正极。Fe电极反应式为
是正极。Fe电极反应式为_________ ;
②接通电源前,装置图中的铜、铁两个电极质量相等,电镀完成后,将两个电极取出,用水小心冲洗干净、烘干,然后称量,二者质量之差为5.12g,由此计算电镀过程中电路中通过电子的物质的量为________ 。
③上述铁镀件破损后,铁更容易被腐蚀。请简要说明镀铜铁镀件破损后,铁更容易被腐蚀的原因:______ 。


(1)钢铁腐蚀主要是吸氧腐蚀,该腐蚀过程中的正极电极反应式为:
(2)为了降低某水库的铁闸门被腐蚀的速率,可以采用图①所示的方案,其中焊接在铁闸门上的固体材料R可以采用
A.铜 B.钠 C.锌 D.石墨
(3)图②所示的方案也可以降低铁闸门的腐蚀速率,其中铁闸门应该连接在直流电源的
(4)钢铁的防护除了用电化学保护方法之外,在钢铁制品表面镀铜也可以有效地防止其腐蚀,电镀的装置如图所示:

①电镀装置图的“直流电源”中,
 填“a”或“b”
填“a”或“b”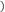 是正极。Fe电极反应式为
是正极。Fe电极反应式为②接通电源前,装置图中的铜、铁两个电极质量相等,电镀完成后,将两个电极取出,用水小心冲洗干净、烘干,然后称量,二者质量之差为5.12g,由此计算电镀过程中电路中通过电子的物质的量为
③上述铁镀件破损后,铁更容易被腐蚀。请简要说明镀铜铁镀件破损后,铁更容易被腐蚀的原因:
2020·河北邯郸·模拟预测 查看更多[2]
更新时间:2020-07-21 22:26:42
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】潜艇的金属外壳浸在海水中,在海水和空气的作用下会被腐蚀:
(1)若海水呈中性,一艘钢制外壳的潜艇在海水中发生腐蚀的电极反应式为:
正极:___________ ,负极:____________________ 。
(2)为有效地保护潜艇。下列措施中最好的是______________ (填序号)
A.采用纯铁制造潜艇外壳 B.采用耐腐蚀的合金制造潜艇外壳
C.在潜艇上涂一层油 D.在潜艇外壳上装一定数量的锌块
(1)若海水呈中性,一艘钢制外壳的潜艇在海水中发生腐蚀的电极反应式为:
正极:
(2)为有效地保护潜艇。下列措施中最好的是
A.采用纯铁制造潜艇外壳 B.采用耐腐蚀的合金制造潜艇外壳
C.在潜艇上涂一层油 D.在潜艇外壳上装一定数量的锌块
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】将1 g琼脂加入250 mL烧杯中,再向其中加入50 mL饱和食盐水和150 mL水。搅拌、加热、煮沸,使琼脂溶解。稍冷后,趁热把琼脂溶液分别倒入两个培养皿中,各滴入5~6滴酚酞溶液和铁氰化钾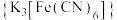 溶液,混合均匀。取两个2~3cm长的铁钉,用砂纸擦光,除去表面氧化物。将裹有锌皮的铁钉放入上述培养皿中,如图1;将缠有铜丝的铁钉放入上述另一个培养皿中,如图2。
溶液,混合均匀。取两个2~3cm长的铁钉,用砂纸擦光,除去表面氧化物。将裹有锌皮的铁钉放入上述培养皿中,如图1;将缠有铜丝的铁钉放入上述另一个培养皿中,如图2。
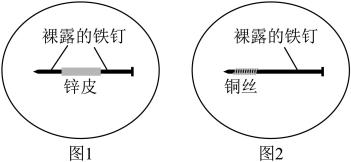
(1)图1中裸露的铁钉作___________ 极,该电极的电极反应式为___________ ,其附近可观察到的颜色变化为___________ 。
(2)图2中,在裸露的铁钉附近看到的颜色变化为___________ ,分析出现该颜色的原因:___________ ,靠近铜丝一端可观察到的颜色变化为___________ 。
(3)另一个同学也进行了上述实验操作,在图1装置中没有看到上述实验现象,其原因可能是___________ (填一条)。
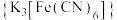 溶液,混合均匀。取两个2~3cm长的铁钉,用砂纸擦光,除去表面氧化物。将裹有锌皮的铁钉放入上述培养皿中,如图1;将缠有铜丝的铁钉放入上述另一个培养皿中,如图2。
溶液,混合均匀。取两个2~3cm长的铁钉,用砂纸擦光,除去表面氧化物。将裹有锌皮的铁钉放入上述培养皿中,如图1;将缠有铜丝的铁钉放入上述另一个培养皿中,如图2。
(1)图1中裸露的铁钉作
(2)图2中,在裸露的铁钉附近看到的颜色变化为
(3)另一个同学也进行了上述实验操作,在图1装置中没有看到上述实验现象,其原因可能是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】I.实验室以K2MnO4为原料,用两种方法制备高锰酸钾。已知:K2MnO4在浓强碱溶液中可稳定存在,溶液呈墨绿色,当溶液碱性减弱时易发生反应:3 +2H2O=2
+2H2O=2 +MnO2↓+4OH-。
+MnO2↓+4OH-。
(1)CO2法:实验装置如图:

①反应一段时间后,用玻璃棒蘸取溶液滴在滤纸上,仅有紫红色而没有绿色痕迹,由此可知_______ 。
②停止通入CO2,过滤除去_______ (填化学式,下同),将滤液蒸发浓缩、冷却结晶,抽滤得到KMnO4粗品。若CO2通入过多,产品中可能混有的杂质是_______ 。
(2)电解法:实验装置如图。

①阳极的电极反应式为_______ ,阴极产生的气体为_______ (填化学式)。
②与CO2法相比,电解法的主要优点是_______ (写一条)。,
(3)如用氨燃料电池电解溶液,已知氨燃料电池使用的电解质溶液是KOH溶液,电池反应为4NH3+3O2=2N2+6H2O。则其负极反应式为_______ 。
(4)若用钢铁(含Fe、C)制品盛装NaClO溶液会发生电化学腐蚀,钢铁制品表面生成红褐色沉淀,溶液会失去漂白、杀菌消毒功效。该电化学腐蚀过程中的正极反应式为_______ 。
 +2H2O=2
+2H2O=2 +MnO2↓+4OH-。
+MnO2↓+4OH-。(1)CO2法:实验装置如图:

①反应一段时间后,用玻璃棒蘸取溶液滴在滤纸上,仅有紫红色而没有绿色痕迹,由此可知
②停止通入CO2,过滤除去
(2)电解法:实验装置如图。

①阳极的电极反应式为
②与CO2法相比,电解法的主要优点是
(3)如用氨燃料电池电解溶液,已知氨燃料电池使用的电解质溶液是KOH溶液,电池反应为4NH3+3O2=2N2+6H2O。则其负极反应式为
(4)若用钢铁(含Fe、C)制品盛装NaClO溶液会发生电化学腐蚀,钢铁制品表面生成红褐色沉淀,溶液会失去漂白、杀菌消毒功效。该电化学腐蚀过程中的正极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】理论上讲,任何自发的氧化还原反应都可以设计成原电池。请你利用下列反应“Cu+2Ag+=2Ag+Cu2+”设计一个化学电池,并回答下列问题:
(1)该电池的正极材料是___________ ,负极材料是___________ ,电解质溶液是___________ 溶液。
(2)在外电路中,电流方向是从___________ 极到___________ 极。(填“正”或“负”)
(3)正极反应是___________ ,负极反应是___________ 。
(4)若有1mol的Ag析出,转移电子的数目为___________ 。
(1)该电池的正极材料是
(2)在外电路中,电流方向是从
(3)正极反应是
(4)若有1mol的Ag析出,转移电子的数目为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】氢氧燃料电池是符合绿色化学理念的新型发电装置。如图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定,请回答:
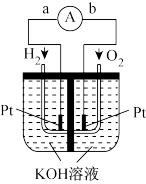
(1)氢氧燃料电池能量转化的主要形式是___________ ,在导线中电子流动方向为________ (用a、b表示)。
(2)负极反应式为___________ 。
(3)该电池工作时,H2和O2连续由外部供给,电池可连续不断提供电能,大量安全储氢是关键技术之一。金属锂是一种重要的储氢材料,吸氢和放氢原理如下:
Ⅰ.2Li+H2===2LiH Ⅱ.LiH+H2O===LiOH+H2↑
①反应Ⅰ中的还原剂是________ ,反应Ⅱ中的氧化剂是________ 。
②金属锂吸收的氢气与放出的氢气的物质的量之比为________ 。

(1)氢氧燃料电池能量转化的主要形式是
(2)负极反应式为
(3)该电池工作时,H2和O2连续由外部供给,电池可连续不断提供电能,大量安全储氢是关键技术之一。金属锂是一种重要的储氢材料,吸氢和放氢原理如下:
Ⅰ.2Li+H2===2LiH Ⅱ.LiH+H2O===LiOH+H2↑
①反应Ⅰ中的还原剂是
②金属锂吸收的氢气与放出的氢气的物质的量之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】化学电池在通讯、交通及日常生活中有着广泛的应用。
(1)下列相关说法正确的是___________ (填序号)。
A.通过某种电池单位质量或单位体积所能输出能量的多少,可以判断该电池的优劣
B.二次电池又称充电电池或蓄电池,这类电池可无限次重复使用
C.除氢气外,甲醇、汽油、氧气等都可用作燃料电池的燃料
D.近年来,废电池必须进行集中处理的问题被提到议事日程,其首要原因是电池外壳的金属材料需要回收
(2)目前常用的镍(Ni)镉(Cd)电池,其电池总反应可表示为:2Ni(OH)2+Cd(OH)2 Cd+2NiO(OH)+2H2O,已知Ni(OH)2和Cd(OH)2均难溶于水,但能溶于酸,以下说法不正确的是
Cd+2NiO(OH)+2H2O,已知Ni(OH)2和Cd(OH)2均难溶于水,但能溶于酸,以下说法不正确的是___________ 。
A.电池放电时Cd作负极
B.反应环境为碱性
C.以上反应是可逆反应
D.该电池是一种二次电池
(3)二甲醚(CH3OCH3)——空气燃料电池的工作原理如图所示。电池工作时,

①a极反应式:___________
②每消耗1molCH3OCH3,有___________ molH+向右侧移动。
(1)下列相关说法正确的是
A.通过某种电池单位质量或单位体积所能输出能量的多少,可以判断该电池的优劣
B.二次电池又称充电电池或蓄电池,这类电池可无限次重复使用
C.除氢气外,甲醇、汽油、氧气等都可用作燃料电池的燃料
D.近年来,废电池必须进行集中处理的问题被提到议事日程,其首要原因是电池外壳的金属材料需要回收
(2)目前常用的镍(Ni)镉(Cd)电池,其电池总反应可表示为:2Ni(OH)2+Cd(OH)2
 Cd+2NiO(OH)+2H2O,已知Ni(OH)2和Cd(OH)2均难溶于水,但能溶于酸,以下说法不正确的是
Cd+2NiO(OH)+2H2O,已知Ni(OH)2和Cd(OH)2均难溶于水,但能溶于酸,以下说法不正确的是A.电池放电时Cd作负极
B.反应环境为碱性
C.以上反应是可逆反应
D.该电池是一种二次电池
(3)二甲醚(CH3OCH3)——空气燃料电池的工作原理如图所示。电池工作时,

①a极反应式:
②每消耗1molCH3OCH3,有
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】离子液体是一种室温熔融盐,为非水体系,由有机阳离子、Al2Cl 和AlCl
和AlCl 组成的离子液体作电解液时,可在钢制品上电镀铝。钢制品应接电源的
组成的离子液体作电解液时,可在钢制品上电镀铝。钢制品应接电源的_______ 极,已知电镀过程中不产生其他离子且有机阳离子不参与电极反应,阴极电极反应式为_______ 。若改用AlCl3水溶液作电解液,则阴极产物为_______ 。
 和AlCl
和AlCl 组成的离子液体作电解液时,可在钢制品上电镀铝。钢制品应接电源的
组成的离子液体作电解液时,可在钢制品上电镀铝。钢制品应接电源的
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】钢铁很容易生锈而被腐蚀,每年因腐蚀而损失的钢铁占世界钢铁年产量的四分之一。请回答钢铁在腐蚀、防护过程中的有关问题。
(1)下列哪个装置可防止铁棒被腐蚀________________ 。
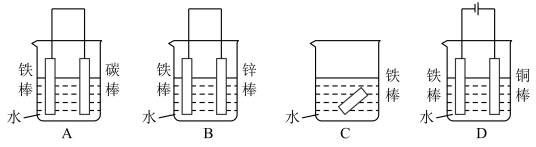
(2)在实际生产中,可在铁件的表面镀铜防止铁被腐蚀。装置示意图如图。请回答:

①铁件应与电源的________ 极相连(写正或负),B电极的电极反应式是______ 。
②若电镀前A、B两金属片质量相同,电镀完成后将它们取出洗净、烘干、称量,二者质量差为10.24 g,则电镀时电路中通过的电子为________ mol。
③电镀结束后CuSO4溶液的浓度______ (填变大,变小,不变)
④镀层破损后,铁不易被腐蚀的是___________ (填序号)。
A 镀铜铁 B 镀锌铁 C 镀锡铁
(1)下列哪个装置可防止铁棒被腐蚀
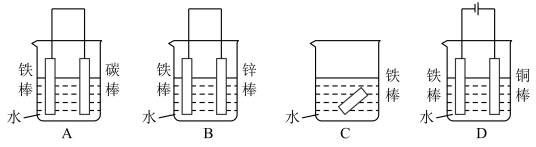
(2)在实际生产中,可在铁件的表面镀铜防止铁被腐蚀。装置示意图如图。请回答:

①铁件应与电源的
②若电镀前A、B两金属片质量相同,电镀完成后将它们取出洗净、烘干、称量,二者质量差为10.24 g,则电镀时电路中通过的电子为
③电镀结束后CuSO4溶液的浓度
④镀层破损后,铁不易被腐蚀的是
A 镀铜铁 B 镀锌铁 C 镀锡铁
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】认真观察下列装置,回答下列问题:
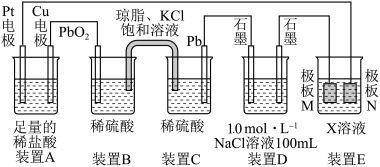
(1)装置B中PbO2上发生的电极反应方程式为________________
(2)装置A中总反应的离子方程式为_____________________________ 。
(3)若装置E中的目的是在Cu材料上镀银,则X为________ ,极板N的材料为________ 。
(4)当装置A中Cu电极质量改变6.4 g时,装置D中产生的气体体积为________ L(标准状况下)。
(5)用NaOH溶液吸收烟气中的SO2,将所得的Na2SO3溶液进行电解,可循环再生NaOH,同时得到H2SO4,其原理如图所示(电极材料为石墨)。
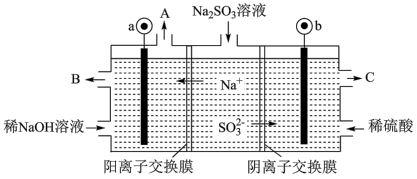
①图中a极连接电源的___________ 极,
②b极电极反应式为____________________________________________

(1)装置B中PbO2上发生的电极反应方程式为
(2)装置A中总反应的离子方程式为
(3)若装置E中的目的是在Cu材料上镀银,则X为
(4)当装置A中Cu电极质量改变6.4 g时,装置D中产生的气体体积为
(5)用NaOH溶液吸收烟气中的SO2,将所得的Na2SO3溶液进行电解,可循环再生NaOH,同时得到H2SO4,其原理如图所示(电极材料为石墨)。

①图中a极连接电源的
②b极电极反应式为
您最近一年使用:0次



