潜艇的金属外壳浸在海水中,在海水和空气的作用下会被腐蚀:
(1)若海水呈中性,一艘钢制外壳的潜艇在海水中发生腐蚀的电极反应式为:
正极:___________ ,负极:____________________ 。
(2)为有效地保护潜艇。下列措施中最好的是______________ (填序号)
A.采用纯铁制造潜艇外壳 B.采用耐腐蚀的合金制造潜艇外壳
C.在潜艇上涂一层油 D.在潜艇外壳上装一定数量的锌块
(1)若海水呈中性,一艘钢制外壳的潜艇在海水中发生腐蚀的电极反应式为:
正极:
(2)为有效地保护潜艇。下列措施中最好的是
A.采用纯铁制造潜艇外壳 B.采用耐腐蚀的合金制造潜艇外壳
C.在潜艇上涂一层油 D.在潜艇外壳上装一定数量的锌块
10-11高一下·辽宁沈阳·阶段练习 查看更多[1]
(已下线)2010-2011学年辽宁省沈阳铁路实验中学高一6月月考化学试题
更新时间:2016-12-09 01:54:15
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】钢铁很容易生锈而被腐蚀,每年因腐蚀而损失的钢铁占世界钢铁年产量的四分之一。钢铁容易生锈的主要原因是因为钢铁在炼制过程中混有少量的碳杂质,在潮湿的空气中容易形成原电池,发生电化学腐蚀。
(1)在空气酸度不大的环境中,其正极反应式为___________________
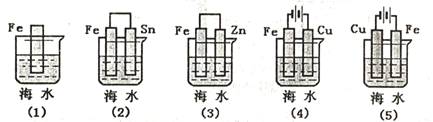
(2)下列各情况,在其中Fe片腐蚀由快到慢的顺序是___________ (用序号表示)。
(3)下图装置的盐桥中盛有饱和NH4NO3琼脂溶液,能够连接两份电解质溶液,形成闭合回路:
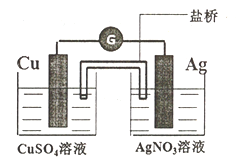
①该装置的能量转化形式为:_________ ,装置工作时,盐桥中的NH4+移向___________ 。(“CuSO4溶液”或“AgNO3溶液”)
②若将盐桥换成铜丝,电路中也有电流通过,则铜丝左端为_________ 极,该极反应式为:___________ 。
(4)运用原电池原理,设计实验验证Cu2+、Fe3+氧化性的强弱,在下图方框内画出实验装置图_____________ (要求:设计一个带盐桥的原电池,标出电极名称及电解质溶液)。该原电池正极反应式__________________ 。
(1)在空气酸度不大的环境中,其正极反应式为
(2)下列各情况,在其中Fe片腐蚀由快到慢的顺序是

(3)下图装置的盐桥中盛有饱和NH4NO3琼脂溶液,能够连接两份电解质溶液,形成闭合回路:

①该装置的能量转化形式为:
②若将盐桥换成铜丝,电路中也有电流通过,则铜丝左端为
(4)运用原电池原理,设计实验验证Cu2+、Fe3+氧化性的强弱,在下图方框内画出实验装置图
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】下表是元素周期表中的一部分。
根据A—J在周期表中的位置,用元素符号、化学式或反应式 回答下列问题:
(1)氧化性最强的单质是___ ,用一个化学反应证明H单质的氧化性强于G单质__________ 。
(2)A分别与F、G、H形成的简单化合物中,稳定性由强到弱的顺序为_________ 。
(3)B、C、G、H离子半径由大到小的顺序是_________ 。
(4)D单质可用来制造D—空气燃料电池,该电池通常以氯化钠或氢氧化钾溶液为电解质溶液,通入空气的电极为正极。若以氯化钠为电解质溶液时,正极的反应式为______ 。若以氢氧化钾溶液为电解质溶液时,电池的总反应式为____ 。
族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 1 | A | |||||||
| 2 | E | F | G | H | J | |||
| 3 | B | C | D | I |
(1)氧化性最强的单质是
(2)A分别与F、G、H形成的简单化合物中,稳定性由强到弱的顺序为
(3)B、C、G、H离子半径由大到小的顺序是
(4)D单质可用来制造D—空气燃料电池,该电池通常以氯化钠或氢氧化钾溶液为电解质溶液,通入空气的电极为正极。若以氯化钠为电解质溶液时,正极的反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】交警检验司机是否酒驾时,通常使用酒精检测仪,学习小组分别对酒精检测仪的原理进行探究性学习。
(1)一种传统的酒精检测仪利用乙醇与酸性 溶液的反应进行检测,甲组同学进行模拟实验,向酸性
溶液的反应进行检测,甲组同学进行模拟实验,向酸性 溶液中加入乙醇,溶液由橙色变绿色,查阅资料发现
溶液中加入乙醇,溶液由橙色变绿色,查阅资料发现 在溶液中显绿色,该实验体现乙醇的
在溶液中显绿色,该实验体现乙醇的_______ (填“氧化性”或者“还原性”)
(2)目前常用的是燃料电池型呼气酒精检测仪,其工作原理如图所示,被测者呼出气体中所含的酒精被输送到电池中反应产生微小电流,该电流经电子放大器放大后在液晶显示屏上显示其酒精含量。
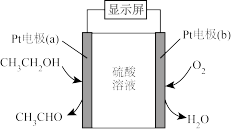
①负极电极反应式为_______ 。
②电池反应为_______ 。
(3)乙组同学设计如下装置(夹持装置省略)进一步探究 催化氧化反应。
催化氧化反应。
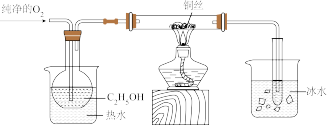
为检验反应产物,该小组同学分别取少量试管中的液体进行了如下实验,回答下列问题:已知:可以用检验葡萄糖的方法检验乙醛。
①热水浴的作用_______ 。
②实验b得出结论依据的现象是_______ 。
③实验a~c中的结论不合理的是_______ (填序号),原因是_______ 。
(1)一种传统的酒精检测仪利用乙醇与酸性
 溶液的反应进行检测,甲组同学进行模拟实验,向酸性
溶液的反应进行检测,甲组同学进行模拟实验,向酸性 溶液中加入乙醇,溶液由橙色变绿色,查阅资料发现
溶液中加入乙醇,溶液由橙色变绿色,查阅资料发现 在溶液中显绿色,该实验体现乙醇的
在溶液中显绿色,该实验体现乙醇的(2)目前常用的是燃料电池型呼气酒精检测仪,其工作原理如图所示,被测者呼出气体中所含的酒精被输送到电池中反应产生微小电流,该电流经电子放大器放大后在液晶显示屏上显示其酒精含量。

①负极电极反应式为
②电池反应为
(3)乙组同学设计如下装置(夹持装置省略)进一步探究
 催化氧化反应。
催化氧化反应。
为检验反应产物,该小组同学分别取少量试管中的液体进行了如下实验,回答下列问题:已知:可以用检验葡萄糖的方法检验乙醛。
| 实验序号 | 检验试剂和反应条件 | 现象 | 结论 |
| a | 酸性 溶液 溶液 | 紫红色褪去 | 产物含有乙醛 |
| b | 新制 悬浊液,加热 悬浊液,加热 | _______ | 产物含有乙醛 |
| c | 浅红色含酚酞的 溶液 溶液 | 浅红色褪去 | 产物可能含有乙酸 |
①热水浴的作用
②实验b得出结论依据的现象是
③实验a~c中的结论不合理的是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】如何防止铁的锈蚀是工业上研究的重点内容。为研究铁的锈蚀,某同学做了探究实验,如下图所示,铁处于①②③三种不同的环境中
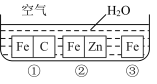
请回答:
(1)金属腐蚀主要分为__________ 腐蚀和_____________ 腐蚀两种。
(2)铁被腐蚀的速率由快到慢的顺序是_________________ (填序号)。
(3)①中正极的电极反应式为_________________________________________________ ,②中负极的电极反应式为_________________________________________ 。
(4)据资料显示,全世界每年因腐蚀而报废的金属材料相当于其年产量的20%以上。为防护金属被腐蚀可采取的措施有__________ (填序号)。
①健身器材刷油漆 ②自行车钢圈镀铬
③将钢管用导线与铜条连接 ④将钢管用导线与碳棒连接

请回答:
(1)金属腐蚀主要分为
(2)铁被腐蚀的速率由快到慢的顺序是
(3)①中正极的电极反应式为
(4)据资料显示,全世界每年因腐蚀而报废的金属材料相当于其年产量的20%以上。为防护金属被腐蚀可采取的措施有
①健身器材刷油漆 ②自行车钢圈镀铬
③将钢管用导线与铜条连接 ④将钢管用导线与碳棒连接
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】电化学在工业生产中具有重要作用。
(1)工业上通过电解饱和食盐水制备氯气,阳极反应历程如图所示:
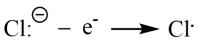
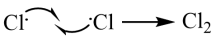
阳极反应历程可描述为:_______ 。
(2)深埋在潮湿土壤中的铁管道,在硫酸盐还原菌作用下,能被硫酸根腐蚀,其电化学腐蚀原理如图所示,此过程中腐蚀电池的正极反应式是_______ 。

(3)工业膜电极法制备的KMnO4常用于氧化还原滴定,该滴定同中和滴定类似(用已知浓度的氧化剂溶液滴定未知浓度的还原剂溶液或反之)。现用0.1000mol·L−1KMnO4标准溶液测定K3[Fe(C2O4)3]样品的纯度。准确称取1.000gK3[Fe(C2O4)3]样品,加入适量水溶解并用稀硫酸酸化,加热至80oC,趁热用KMnO4标准溶液滴定至终点,消耗KMnO4标准溶液20.00mL。反应离子方程式: +C2O
+C2O +H+→CO2↑+Mn2++H2O(未配平)Mr[K3[Fe(C2O4)3]]=437,请完成下列问题:
+H+→CO2↑+Mn2++H2O(未配平)Mr[K3[Fe(C2O4)3]]=437,请完成下列问题:
①实验中配制100mL0.1000mol·L−1KMnO4溶液,所需的玻璃仪器有烧杯、胶头滴管,还须_______ 。
②滴定终点的现象是_______ 。
③计算样品的纯度(写出计算过程):_______ 。
④若滴定时所用的酸性KMnO4溶液因久置而导致浓度变小,则由此测得的待测样品的纯度会_______ (填“偏小”“偏大”或“不变”)。
(1)工业上通过电解饱和食盐水制备氯气,阳极反应历程如图所示:
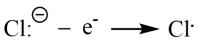
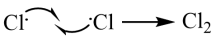
阳极反应历程可描述为:
(2)深埋在潮湿土壤中的铁管道,在硫酸盐还原菌作用下,能被硫酸根腐蚀,其电化学腐蚀原理如图所示,此过程中腐蚀电池的正极反应式是

(3)工业膜电极法制备的KMnO4常用于氧化还原滴定,该滴定同中和滴定类似(用已知浓度的氧化剂溶液滴定未知浓度的还原剂溶液或反之)。现用0.1000mol·L−1KMnO4标准溶液测定K3[Fe(C2O4)3]样品的纯度。准确称取1.000gK3[Fe(C2O4)3]样品,加入适量水溶解并用稀硫酸酸化,加热至80oC,趁热用KMnO4标准溶液滴定至终点,消耗KMnO4标准溶液20.00mL。反应离子方程式:
 +C2O
+C2O +H+→CO2↑+Mn2++H2O(未配平)Mr[K3[Fe(C2O4)3]]=437,请完成下列问题:
+H+→CO2↑+Mn2++H2O(未配平)Mr[K3[Fe(C2O4)3]]=437,请完成下列问题:①实验中配制100mL0.1000mol·L−1KMnO4溶液,所需的玻璃仪器有烧杯、胶头滴管,还须
②滴定终点的现象是
③计算样品的纯度(写出计算过程):
④若滴定时所用的酸性KMnO4溶液因久置而导致浓度变小,则由此测得的待测样品的纯度会
您最近一年使用:0次
【推荐3】能源是现代文明的原动力,随着常规能源的有限性以及环境问题的日益突出,以环保和可再生为特质的新能源越来越得到各国的重视。新能源包括风能、氢能、沼气、酒精、甲醇等,新能源的使用与研究在一定程度上助力中国实现“碳达峰、碳中和”。通过化学方法可以使能量按人们所期望的形式转化,从而开辟新能源和提高能源的利用率。
(1)二氧化碳的资源化利用是目前研究的热点问题之一,西北工业大学团队研究锂-二氧化碳二次电池,取得了重大科研成果。该电池放电的总反应为3CO2+4Li=2Li2CO3+C。下列说法正确的是_______ 。
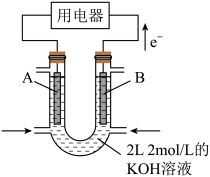
(2)如图所示为CH4燃料电池的装置(A、B为多孔碳棒):______ (填A或B)处电极入口通甲烷,其电极反应式为:_______ ;当消耗甲烷的体积为11.2L(标准状况下)时,消耗KOH的质量为_______ g。
(3)用上述CH4燃料电池连接成如图装置。
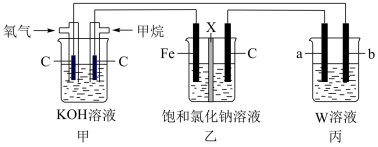
乙池中X为阳离子交换膜,石墨电极(C)作_______ 极,写出乙池总反应的离子方程式_______ 。
(4)若将乙装置中两电极用导线直接相连,则铁发生_______ 腐蚀,写出碳棒的电极反应式:______ 。若将乙装置中两电极连接电源的正负两极,铁连接电源的_______ 极(填“正”或“负”)时,可防止铁腐蚀。
(5)若丙中要实现铁上镀银,b电极材料为_______ 。
(1)二氧化碳的资源化利用是目前研究的热点问题之一,西北工业大学团队研究锂-二氧化碳二次电池,取得了重大科研成果。该电池放电的总反应为3CO2+4Li=2Li2CO3+C。下列说法正确的是
| A.该电池的电解液可以是稀硫酸 |
| B.放电时,若消耗1.5molCO2时,转移2mol电子 |
| C.放电时,电子从锂电极流出,通过电解液流回锂电极,构成闭合回路 |
| D.放电时,锂电极作正极 |

(3)用上述CH4燃料电池连接成如图装置。

乙池中X为阳离子交换膜,石墨电极(C)作
(4)若将乙装置中两电极用导线直接相连,则铁发生
(5)若丙中要实现铁上镀银,b电极材料为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】化学与环境保护、人体健康、建筑材料等息息相关。
(1)天然水中杂质较多.常需加入明矾、ClO2等物质处理后才能饮用。加入ClO2 的作用是__ :加入明矾后,Al3+水解的离子方程式是_________________________ 。
(2)服装面料种类繁多。下列面料中不属于天然纤维的是__________ (填序号)。
a、棉和麻 b、丝和毛 c、涤纶和锦纶
(3)金属腐蚀会造成巨大的经济损失,钢铁在潮湿的空气中更容易腐蚀,主要原因是钢铁里的铁和碳构成许多微小的___________ ,发生电化学腐蚀。
(4)“玉兔”号月球车开创了我国月球表面探索的先河,其制备材料中使用了镁铝合金。镁铝合金的优点是_________ :a.强度大 b.密度大 c.绝缘性好 d.耐腐蚀
(1)天然水中杂质较多.常需加入明矾、ClO2等物质处理后才能饮用。加入ClO2 的作用是
(2)服装面料种类繁多。下列面料中不属于天然纤维的是
a、棉和麻 b、丝和毛 c、涤纶和锦纶
(3)金属腐蚀会造成巨大的经济损失,钢铁在潮湿的空气中更容易腐蚀,主要原因是钢铁里的铁和碳构成许多微小的
(4)“玉兔”号月球车开创了我国月球表面探索的先河,其制备材料中使用了镁铝合金。镁铝合金的优点是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】金属腐蚀的电化学原理可用下图模拟。
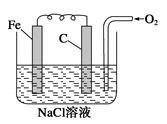
请写出有关电极反应式:
①铁棒上的电极反应式:_______________________
碳棒上的电极反应式:_________________________
(2)该图所表示的是_________________________ (填“析氢”或“吸氧”)腐蚀。
(3)若将O2撤走,并将NaCl溶液改为稀H2SO4溶液,则此图可表示__________ (填“析氢”或“吸氧”)腐蚀原理;若用牺牲阳极法来保护铁棒不被腐蚀溶解,即可将碳棒改为_________ 棒。

请写出有关电极反应式:
①铁棒上的电极反应式:
碳棒上的电极反应式:
(2)该图所表示的是
(3)若将O2撤走,并将NaCl溶液改为稀H2SO4溶液,则此图可表示
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
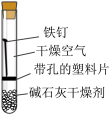
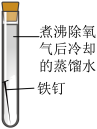
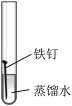
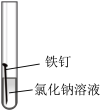
【推荐3】某小组同学对不同条件下铁钉的锈蚀进行了实验。
(1)一周后观察,铁钉被腐蚀程度最大的是___________ (填实验序号)。
(2)实验小组将实验④中氯化钠溶液分别替换为pH=2和pH=4的盐酸溶液。在密闭容器中,分别用压强传感器记录实验过程中的压强变化,如图所示。___________ (填字母,下同)。
a.两容器中负极反应均为Fe-2e⁻=Fe2+
b.曲线a记录的是pH=2的盐酸中压强的变化
c.在弱酸性溶液中,铁钉能发生吸氧腐蚀
d.曲线b记录的容器中正极反应是O2+4e⁻+2H2O=4OH⁻
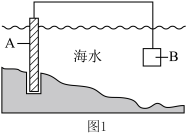
(3)电化学原理在保护海水中钢闸门中有广泛应用。______ 。
a.牺牲阳极法 b.外加电流法
②为了减缓海水对钢闸门A的腐蚀,图1中材料B可以选择______ 。
a.碳棒 b.锌板 c.铜板
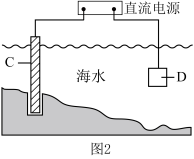
③图2中,钢闸门C应连接直流电源的___________ (填“正”或“负”)极。
| 序号 | ① | ② | ③ | ④ |
| 实验 |
|
|
|
|
(1)一周后观察,铁钉被腐蚀程度最大的是
(2)实验小组将实验④中氯化钠溶液分别替换为pH=2和pH=4的盐酸溶液。在密闭容器中,分别用压强传感器记录实验过程中的压强变化,如图所示。

a.两容器中负极反应均为Fe-2e⁻=Fe2+
b.曲线a记录的是pH=2的盐酸中压强的变化
c.在弱酸性溶液中,铁钉能发生吸氧腐蚀
d.曲线b记录的容器中正极反应是O2+4e⁻+2H2O=4OH⁻
(3)电化学原理在保护海水中钢闸门中有广泛应用。
a.牺牲阳极法 b.外加电流法
②为了减缓海水对钢闸门A的腐蚀,图1中材料B可以选择
a.碳棒 b.锌板 c.铜板
③图2中,钢闸门C应连接直流电源的
您最近一年使用:0次
【推荐1】根据原电池原理和电解原理进行如图回答。请回答:用如图所示装置进行实验(K闭合)。
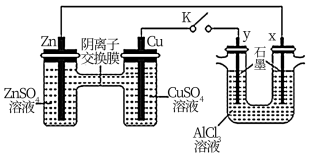
(1)Zn极为___________ 极;实验过程中,SO
____________ (填“从左向右”、“从右向左”或“不”)移动,Cu极的电极反应式为:___________ 。
(2)y极为___________ 极;x的电极反应现象为___________ ;写出右边装置的总反应式:___________ 。
(3)写出生活中对钢闸门的一种电化学保护方法___________ 。
(4)有人设想寻求合适的催化剂和电极材料,以O2、CH4为电极反应物,以NaOH为电解质溶液制取新型燃料电池,请写出该电池的正极反应式___________ 。

(1)Zn极为

(2)y极为
(3)写出生活中对钢闸门的一种电化学保护方法
(4)有人设想寻求合适的催化剂和电极材料,以O2、CH4为电极反应物,以NaOH为电解质溶液制取新型燃料电池,请写出该电池的正极反应式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】钢铁很容易生锈而被腐蚀,每年因腐蚀而损失的钢材占世界钢铁年产量的四分之一。
(1)钢铁腐蚀主要是吸氧腐蚀,该腐蚀过程中的电极反应式为:正极:_____________________________ ;负极:______________________ 。
(2)为了降低某水库铁闸门被腐蚀的速率,可以采用甲图所示的方案,其中焊接在闸 门上的固体材料R可以采用___________ 。
A.铜 B.钠 C.锌 D.石墨
(3)乙图所示的方案也可以降低铁闸门的腐蚀速率,其中铁闸门应该连接在直流电源的___________ 极。

(4)铅蓄电池是化学电源,其电极材料分别为Pb和PbO2,电解质溶液为稀硫酸,放电时电池的总反应为Pb + PbO2 + 2H2SO4== 2PbSO4 + 2H2O。根据上述情况判断:
①铅蓄电池的正极材料是_______ (填“Pb”或“PbO2”),负极的电极反应式为_______________________________________ 。
②铅蓄电池工作时,电解质溶液中SO42﹣移向________ 极(填“负”或“正”),溶液的pH___________ (填“增大”“减小”或“不变”)。
(1)钢铁腐蚀主要是吸氧腐蚀,该腐蚀过程中的电极反应式为:正极:
(2)为了降低某水库铁闸门被腐蚀的速率,可以采用甲图所示的方案,其中焊接在闸 门上的固体材料R可以采用
A.铜 B.钠 C.锌 D.石墨
(3)乙图所示的方案也可以降低铁闸门的腐蚀速率,其中铁闸门应该连接在直流电源的

(4)铅蓄电池是化学电源,其电极材料分别为Pb和PbO2,电解质溶液为稀硫酸,放电时电池的总反应为Pb + PbO2 + 2H2SO4== 2PbSO4 + 2H2O。根据上述情况判断:
①铅蓄电池的正极材料是
②铅蓄电池工作时,电解质溶液中SO42﹣移向
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】(1)化学与生活息息相关。下列叙述正确的是________ (填字母代号,下同)。
A.馒头越嚼越甜 B.鲜榨橙汁遇到碘水会变蓝
C.油脂经水解可变成葡萄糖 D.土豆中的淀粉经水解可变成酒
(2)把新制的Cu(OH)2悬浊液加入到某病人的尿液中并微热,如果观察到砖红色沉淀,说明尿液中可能含有的物质是________ 。
A.食醋 B.白酒 C.葡萄糖 D.食盐
(3)生活中常用药品很多,如:A.碘酒、B. 青霉素、C. 阿司匹林、D. 麻黄碱、E.葡萄糖注射液、F.胃舒平(含氢氧化铝、淀粉等)。
①上述物质中属于抗生素的是__________ (填字母代号,下同),具有止咳平喘作用的天然药物是__________ 。胃舒平可防治胃酸分泌过多,其发挥功效时的离子方程式 为__________________ 。
②低血糖病症发作时,喝葡萄糖水可快速见效。葡萄糖作为营养剂供给人体能量,在体内发生的主要反应是__________ (填字母代号)。
A.氧化反应 B.取代反应 C.加成反应 D.聚合反应
(4)研究发现,长期使用铁锅炒菜,可有效减少缺铁性________ 病症的发生,为了提高补铁效果,在炒菜时可经常加入适量的__________ (填“食醋”或“料酒”)。炒完菜之后不洗锅,铁锅通常会生锈,此过程中主要发生________ 腐蚀(填“化学”或“电化学”),请写出金属防护的一种方法__________ 。
A.馒头越嚼越甜 B.鲜榨橙汁遇到碘水会变蓝
C.油脂经水解可变成葡萄糖 D.土豆中的淀粉经水解可变成酒
(2)把新制的Cu(OH)2悬浊液加入到某病人的尿液中并微热,如果观察到砖红色沉淀,说明尿液中可能含有的物质是
A.食醋 B.白酒 C.葡萄糖 D.食盐
(3)生活中常用药品很多,如:A.碘酒、B. 青霉素、C. 阿司匹林、D. 麻黄碱、E.葡萄糖注射液、F.胃舒平(含氢氧化铝、淀粉等)。
①上述物质中属于抗生素的是
②低血糖病症发作时,喝葡萄糖水可快速见效。葡萄糖作为营养剂供给人体能量,在体内发生的主要反应是
A.氧化反应 B.取代反应 C.加成反应 D.聚合反应
(4)研究发现,长期使用铁锅炒菜,可有效减少缺铁性
您最近一年使用:0次