如何防止铁的锈蚀是工业上研究的重点内容。为研究铁的锈蚀,某同学做了探究实验,如下图所示,铁处于①②③三种不同的环境中
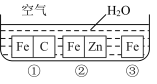
请回答:
(1)金属腐蚀主要分为__________ 腐蚀和_____________ 腐蚀两种。
(2)铁被腐蚀的速率由快到慢的顺序是_________________ (填序号)。
(3)①中正极的电极反应式为_________________________________________________ ,②中负极的电极反应式为_________________________________________ 。
(4)据资料显示,全世界每年因腐蚀而报废的金属材料相当于其年产量的20%以上。为防护金属被腐蚀可采取的措施有__________ (填序号)。
①健身器材刷油漆 ②自行车钢圈镀铬
③将钢管用导线与铜条连接 ④将钢管用导线与碳棒连接

请回答:
(1)金属腐蚀主要分为
(2)铁被腐蚀的速率由快到慢的顺序是
(3)①中正极的电极反应式为
(4)据资料显示,全世界每年因腐蚀而报废的金属材料相当于其年产量的20%以上。为防护金属被腐蚀可采取的措施有
①健身器材刷油漆 ②自行车钢圈镀铬
③将钢管用导线与铜条连接 ④将钢管用导线与碳棒连接
更新时间:2018-03-04 16:22:59
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】化学与社会经济建设、生态文明建设、人类健康保障等密切相关。
(1)①现代以石油化工为基础的三大合成材料是________ 、___________ 、_____________ 。
②生产硅酸盐水泥和普通玻璃都需用到的共同原料是_________ 。
③钢铁制品在潮湿的空气中能发生_____ 腐蚀,发生该腐蚀时的负极反应式为________ 。为防止腐蚀通常在海水中行驶的轮船船身上装有一定数量的________ (填“锌”或“铜”)块来防止钢铁的腐蚀。
(2)防治环境污染,改善生态环境已成为全球共识。
①进入冬季全国多个省市出现严重的雾霾天气。导致雾霾形成的主要污染物是_______ (填字母);
A.SO2 B.CO2 C.PM2.5
②垃圾无害化处理有利于保护生态环境。下列有关生活垃圾的处理合理的是________ (填字母)。 A.用厨余垃圾生产沼气 B.废旧塑料露天焚烧 C.废旧电池就地填埋
(3)①如果人体缺少某种维生素则易患夜盲症,该维生素是________ ;发育出现障碍,患营养缺乏症,这主要是由于摄取_________ (填“蛋白质”、“脂肪”或“糖类”)不足引起的。
②某品牌抗酸药的主要成分有糖衣、碳酸镁、淀粉等。
写出该抗酸药发挥功效时的离子方程式 :____________________________ 。
淀粉在抗酸药中作填充剂、粘合剂,淀粉在人体内酶的催化作用下发生水解反应,最终转化为(写化学式 )______________ 。
③服用补铁(含Fe2+ )剂时,医生常建议同时服用维生素C,这是因为维生素C具有还原性。欲探究该性质,可选择的试剂是_________ (填字母)。
A.碘水、淀粉 B.KI溶液 C.酸性KMnO4溶液
(1)①现代以石油化工为基础的三大合成材料是
②生产硅酸盐水泥和普通玻璃都需用到的共同原料是
③钢铁制品在潮湿的空气中能发生
(2)防治环境污染,改善生态环境已成为全球共识。
①进入冬季全国多个省市出现严重的雾霾天气。导致雾霾形成的主要污染物是
A.SO2 B.CO2 C.PM2.5
②垃圾无害化处理有利于保护生态环境。下列有关生活垃圾的处理合理的是
(3)①如果人体缺少某种维生素则易患夜盲症,该维生素是
②某品牌抗酸药的主要成分有糖衣、碳酸镁、淀粉等。
写出该抗酸药发挥功效时的
淀粉在抗酸药中作填充剂、粘合剂,淀粉在人体内酶的催化作用下发生水解反应,最终转化为(
③服用补铁(含Fe2+ )剂时,医生常建议同时服用维生素C,这是因为维生素C具有还原性。欲探究该性质,可选择的试剂是
A.碘水、淀粉 B.KI溶液 C.酸性KMnO4溶液
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】海水是名副其实的弱碱性液体矿产,平均每立方公里的海水中有3570万吨的矿物质,世界上已知的100多种元素中,80%可以在海水中找到。如何有效利用海水资源,并尽可能减少海水时金属材料的腐蚀,是当今的研究热点。
(1)下列关于金属腐蚀与防护的说法错误的是______ (单选)。

(2)我国首创的海洋电池以铝板、铂网作电极,海水为电解质溶液,空气中的氧气与铝反应产生电流,放电时______ (单选)。
某同学设计一个燃料电池(如图所示),目的是探究氯碱工业原理和粗铜的精炼原理,其中乙装置中X为阳离子交换膜。

(3)通入甲烷的电极为______ (填“正极”、“负极”、“阴极”或“阳极”),该电极反应式为______ 。电子经导线由Pt先传递到______ 棒(填电极材料)。
(4)关于乙装置,下列分析错误的是______ (单选)。
(5)如果粗铜中含有锌、银等杂质,丙装置中反应一段时间,Cu2+浓度将______ (填“增大”、“减小”或“不变”)。精铜电极上的电极反应式为_____ ,当甲池中消耗0.1molO2时,丙池中精铜增重______ g。
(1)下列关于金属腐蚀与防护的说法错误的是

| A.图①,放置于干燥空气中的铁钉不易生锈 |
| B.图②,若断开电源,钢闸门将发生吸氧腐蚀 |
| C.图②,若将钢闸门与电源的正极相连,可防止钢闸门腐蚀 |
| D.图③,若金属M比Fe活泼,可防止输水管腐蚀 |
| A.铝电极上发生还原反应 | B.正离子向负极移动 |
| C.氧气在正极上得电子 | D.电流由铝板经外电路流向铂网 |
某同学设计一个燃料电池(如图所示),目的是探究氯碱工业原理和粗铜的精炼原理,其中乙装置中X为阳离子交换膜。

(3)通入甲烷的电极为
(4)关于乙装置,下列分析错误的是
| A.该装置将电能转化为化学能 |
| B.铁棒周围溶液pH逐渐升高 |
| C.铁棒不会被腐蚀,属于牺牲阳极的阴极保护法 |
| D.若将铁棒和碳棒直接相连,Fe电极发生反应:Fe-2e-=Fe2+ |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】(1)依据反应:2Ag+(aq)+Cu(s)=Cu2+(aq)+2Ag(s)设计的原电池如下图甲所示。

①电极X的材料是_________________ ;
②外电路中的电子是从___ 电极流向__ 电极(填电极材料名称或符号)。
③在电池放电过程中,盛有饱和KCl琼脂溶胶的盐桥中,向CuSO4溶液一端扩散的离子是___________ (填离子符号)。
(2)①金属腐蚀一般可分为化学腐蚀和电化学腐蚀。炒过菜的铁锅未及时清洗容易发生电化学腐蚀而生锈。请写出铁锅生锈过程的正极反应式:____________________ 。
②为了减缓某水库铁闸门被腐蚀的速率,可以采用下图乙所示的方案,其中焊接在铁闸门上的固体材料R可以采用__________ (填写字母序号)。
A.铜 B.钠 C.锌 D.石墨
③图丙所示方案也可以减缓铁闸门的腐蚀速率,则铁闸门应连接直流电源的____ 极。
(3)蓄电池是一种可以反复充电、放电的装置。有一种蓄电池在充电和放电时发生的反应是:NiO2+ Fe + 2H2O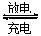 Fe(OH)2+ Ni(OH)2。
Fe(OH)2+ Ni(OH)2。
①若此蓄电池放电时,该电池某一电极发生还原反应的物质是__ (填序号)。
A.NiO2B.Fe C.Fe(OH)2D.Ni(OH)2
②该电池放电时,正极附近溶液的pH________ (填增大、减小、不变)
③充电时该电池阳极的电极反应式___________________________ 。

①电极X的材料是
②外电路中的电子是从
③在电池放电过程中,盛有饱和KCl琼脂溶胶的盐桥中,向CuSO4溶液一端扩散的离子是
(2)①金属腐蚀一般可分为化学腐蚀和电化学腐蚀。炒过菜的铁锅未及时清洗容易发生电化学腐蚀而生锈。请写出铁锅生锈过程的正极反应式:
②为了减缓某水库铁闸门被腐蚀的速率,可以采用下图乙所示的方案,其中焊接在铁闸门上的固体材料R可以采用
A.铜 B.钠 C.锌 D.石墨
③图丙所示方案也可以减缓铁闸门的腐蚀速率,则铁闸门应连接直流电源的
(3)蓄电池是一种可以反复充电、放电的装置。有一种蓄电池在充电和放电时发生的反应是:NiO2+ Fe + 2H2O
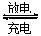 Fe(OH)2+ Ni(OH)2。
Fe(OH)2+ Ni(OH)2。①若此蓄电池放电时,该电池某一电极发生还原反应的物质是
A.NiO2B.Fe C.Fe(OH)2D.Ni(OH)2
②该电池放电时,正极附近溶液的pH
③充电时该电池阳极的电极反应式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】《化学与生活》
(1)合理膳食,保持营养均衡,是青少年学生健康成长的重要保证。
①蛋白质是人体必需的营养物质,它在人体内最终分解为( ) 。
A.葡萄糖 B.氨基酸 C.脂肪酸
②现有下列五种物质 A.食盐 B.食醋 C.苹果汁 D.葡萄糖 E.青霉素,请按下列要求填空(填序号)。
富含维生素C的是_______ ;可直接进入血液,补充能量的是______ ;应用最广泛的抗生素之一的是______ ;即可作为调味剂,又可作为防腐剂、着色剂的是______ ;食用过多会引起血压升高、肾脏受损的________ 。
(2) 材料是人类生存和发展的物质基础,合理使用材料可以改善我们的生活。
①居室装修所使的人造板材会释放出一种挥发性物质,长期接触会引起过敏性皮炎,免疫功能异常,该挥发性物质是( ) 。
A.酒精 B.蔗糖 C.甲醛
②一般情况下,合金比组成它的成分金属硬度__________ (填大、小)。
③_______ 腐蚀是造成钢铁腐蚀的主要原因,自行车的钢圈通常采用________ (填涂油漆或镀Cr)防腐蚀。
(1)合理膳食,保持营养均衡,是青少年学生健康成长的重要保证。
①蛋白质是人体必需的营养物质,它在人体内最终分解为
A.葡萄糖 B.氨基酸 C.脂肪酸
②现有下列五种物质 A.食盐 B.食醋 C.苹果汁 D.葡萄糖 E.青霉素,请按下列要求填空(填序号)。
富含维生素C的是
(2) 材料是人类生存和发展的物质基础,合理使用材料可以改善我们的生活。
①居室装修所使的人造板材会释放出一种挥发性物质,长期接触会引起过敏性皮炎,免疫功能异常,该挥发性物质是
A.酒精 B.蔗糖 C.甲醛
②一般情况下,合金比组成它的成分金属硬度
③
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】金属的腐蚀
(1)概念:金属或合金与周围的_______ 发生_______ 反应而引起损耗的现象。其实质是金属原子_______ 电子变为阳离子,金属发生_______ 反应。
(2)根据与金属接触的_______ 不同,金属腐蚀可分为两类:
①化学腐蚀:金属与其表面接触的一些物质(如_______ 等)直接反应而引起的腐蚀。腐蚀的速率随温度升高而_______ 。
②电化学腐蚀:当_______ 的金属与_______ 溶液接触时会发生_______ 反应,比较_______ 的金属发生氧化反应而被腐蚀。
(1)概念:金属或合金与周围的
(2)根据与金属接触的
①化学腐蚀:金属与其表面接触的一些物质(如
②电化学腐蚀:当
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】对金属制品进行抗腐蚀处理,可延长其使用寿命。
(1)以下为铝材表面处理的一种方法:

①碱洗的目的是除去铝材表面的自然氧化膜,碱洗时常有气泡冒出,原因是______ (用离子方程式表示)。为将碱洗槽液中铝以沉淀形式回收,最好向槽液中加入下列试剂中的______ 。
a.NH3 b.CO2 c.NaOH d.HNO3
②以铝材为阳极,在H2SO4溶液中电解,铝材表面形成氧化膜,阳极电极反应为______ 。取少量废电解液,加入NaHCO3,溶液后产生气泡和白色沉淀,产生沉淀的原因(用离子方程式表示)______ 。
(2)利用如图装置,可以模拟铁的电化学防护。

①若X为碳棒,为减缓铁的腐蚀,开关K应置于______ 处。
②若X为锌,开关K置于M处,该电化学防护法称为______ 。
(1)以下为铝材表面处理的一种方法:

①碱洗的目的是除去铝材表面的自然氧化膜,碱洗时常有气泡冒出,原因是
a.NH3 b.CO2 c.NaOH d.HNO3
②以铝材为阳极,在H2SO4溶液中电解,铝材表面形成氧化膜,阳极电极反应为
(2)利用如图装置,可以模拟铁的电化学防护。

①若X为碳棒,为减缓铁的腐蚀,开关K应置于
②若X为锌,开关K置于M处,该电化学防护法称为
您最近一年使用:0次
【推荐1】铁是人类生活中最常见、应用最广泛的金属,钢铁在空气中很容易被腐蚀。
(1)炒过菜的铁锅未及时洗净(残液中含有 NaCl),不久便会因腐蚀而出现褐色锈斑。铁锅锈蚀的电极反应式为:负极___________________________ ,正极___________________________ 。
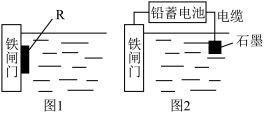
(2)为了降低某水库的铁闸门的腐蚀速率,可以采用图 1 所示的方案,其中焊接在铁闸门上的固体材料 R 可以采用_______________ (填序号)。
A、铜 B、锌 C、钠 D、石墨
(3)图 2 所示的方案也可以降低铁闸门的腐蚀速率,其中铁闸门应该连接在铅蓄电池的_______ 极上(填“正”或“负”)。
(4)常温下以铅蓄电池为电源,用石墨作电极电解 1L 0.1mol/L NaCl溶液,电解一段时间后,测得溶液的 pH 为 13,则铅蓄电池中转移电子的物质的量为__________ 。
(1)炒过菜的铁锅未及时洗净(残液中含有 NaCl),不久便会因腐蚀而出现褐色锈斑。铁锅锈蚀的电极反应式为:负极

(2)为了降低某水库的铁闸门的腐蚀速率,可以采用图 1 所示的方案,其中焊接在铁闸门上的固体材料 R 可以采用
A、铜 B、锌 C、钠 D、石墨
(3)图 2 所示的方案也可以降低铁闸门的腐蚀速率,其中铁闸门应该连接在铅蓄电池的
(4)常温下以铅蓄电池为电源,用石墨作电极电解 1L 0.1mol/L NaCl溶液,电解一段时间后,测得溶液的 pH 为 13,则铅蓄电池中转移电子的物质的量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】下图是几种电化学装置,请答下列问题。
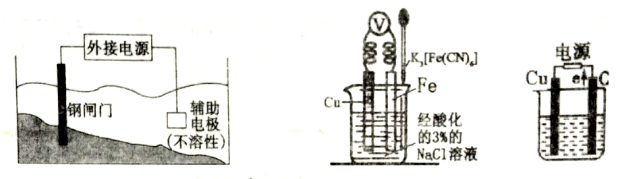
(1)图一被保护的钢闸门应与外接电源的_______ 极相连,这种方法称之为___________ ;
(2)图二往Fe极区滴入2滴黄色的K3[Fe(CN) 6]溶液,一段时间后的现象________________ 。
(3)图三烧杯中盛放足量的CuSO4溶液总反应的离子方程式为_____________________ ;25℃,若起始时盛放100mLpH =5的CuSO4溶液,一段时间后溶液的pH变为1,此时仍只有一个电极上产生气体,若要使溶液恢复到起始时的浓度(忽略溶液体积的变化),可向溶液中加入_____ (填写物质的化学式)___________ g。

(1)图一被保护的钢闸门应与外接电源的
(2)图二往Fe极区滴入2滴黄色的K3[Fe(CN) 6]溶液,一段时间后的现象
(3)图三烧杯中盛放足量的CuSO4溶液总反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】A、B、C三个烧杯中分别盛有相同物质的量浓度的稀硫酸。
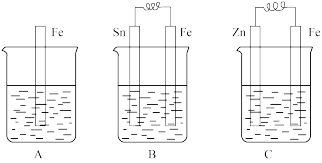
(1)A中反应的离子方程式为_________________________________ 。
(2)B中Fe极为_______ 极,电极反应式为_______________________ 。C中Fe极为_______ 极,电极反应式为__________________________ ,电子从_______ 极流出(填“Zn”或“Fe”)。
(3)比较A、B、C中铁被腐蚀的速率,由快到慢的顺序是___________________ 。

(1)A中反应的离子方程式为
(2)B中Fe极为
(3)比较A、B、C中铁被腐蚀的速率,由快到慢的顺序是
您最近一年使用:0次



