A、B、C三个烧杯中分别盛有相同物质的量浓度的稀硫酸。
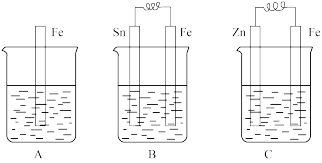
(1)A中反应的离子方程式为_________________________________ 。
(2)B中Fe极为_______ 极,电极反应式为_______________________ 。C中Fe极为_______ 极,电极反应式为__________________________ ,电子从_______ 极流出(填“Zn”或“Fe”)。
(3)比较A、B、C中铁被腐蚀的速率,由快到慢的顺序是___________________ 。

(1)A中反应的离子方程式为
(2)B中Fe极为
(3)比较A、B、C中铁被腐蚀的速率,由快到慢的顺序是
更新时间:2019-12-25 20:05:59
|
相似题推荐
填空题
|
适中
(0.65)
真题
名校
【推荐1】ZnMnO2干电池应用广泛,其电解质溶液是ZnCl2NH4Cl混合溶液。
(1)该电池的负极材料是_______ 。电池工作时,电子流向_______ (填“正极”或“负极”)。
(2)若ZnCl2NH4Cl混合溶液中含有杂质Cu2+,会加速某电极的腐蚀,其主要原因是_______ 。
欲除去Cu2+,最好选用下列试剂中的_______ (填代号)。
A.NaOH B.Zn C.Fe D.NH3·H2O
(3)MnO2的生产方法之一是以石墨为电极,电解酸化的MnSO4溶液。阴极的电极反应式是_______ 。若电解电路中通过2 mol电子,MnO2的理论产量为_______ g。
(1)该电池的负极材料是
(2)若ZnCl2NH4Cl混合溶液中含有杂质Cu2+,会加速某电极的腐蚀,其主要原因是
欲除去Cu2+,最好选用下列试剂中的
A.NaOH B.Zn C.Fe D.NH3·H2O
(3)MnO2的生产方法之一是以石墨为电极,电解酸化的MnSO4溶液。阴极的电极反应式是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】回答下列问题:
(1)如图是某同学设计的一个简易的原电池装置,请回答下列问题。

①若a电极材料为碳、b溶液为 溶液,则正极的电极反应式为
溶液,则正极的电极反应式为_______ ,当有1.6 g负极材料溶解时,转移的电子为_______ mol。
②若a电极材料为铁、b溶液为浓硝酸,电流表的指针也会偏转,则电子的流向为_______ →_______ (填电极材料,下同);溶液中的 向
向_______ 极移动。
(2)有人以化学反应: 为基础设计出一种原电池,移入人体内作为心脏起搏器的能源,它靠人体内血液中溶有一定浓度的
为基础设计出一种原电池,移入人体内作为心脏起搏器的能源,它靠人体内血液中溶有一定浓度的 、
、 进行工作。则原电池的负极材料是
进行工作。则原电池的负极材料是_______ ,正极反应式为_______ 。
(1)如图是某同学设计的一个简易的原电池装置,请回答下列问题。

①若a电极材料为碳、b溶液为
 溶液,则正极的电极反应式为
溶液,则正极的电极反应式为②若a电极材料为铁、b溶液为浓硝酸,电流表的指针也会偏转,则电子的流向为
 向
向(2)有人以化学反应:
 为基础设计出一种原电池,移入人体内作为心脏起搏器的能源,它靠人体内血液中溶有一定浓度的
为基础设计出一种原电池,移入人体内作为心脏起搏器的能源,它靠人体内血液中溶有一定浓度的 、
、 进行工作。则原电池的负极材料是
进行工作。则原电池的负极材料是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】合成氨的反应对人类解决粮食问题贡献巨大。合成氨反应的化学方程式为N2(g)+3H2(g) 2NH3(g)。回答下列问题:
2NH3(g)。回答下列问题:
(1)已知断开1mol化学键所吸收的能量如下:H-H436kJ,N-H391kJ,N≡N946kJ。则N2(g)+3H2(g) 2NH3(g)反应中生成17gNH3
2NH3(g)反应中生成17gNH3_______ (填“吸收”或“放出”)______ kJ热量。
(2)恒温下,将6molN2与17molH2的混合气体通入2L的恒容密闭容器中,进行合成氨反应,当反应进行到5s时,有0.1molNH3生成。
①0~5s内用H2表示该反应的平均反应速率v(H2)=______ mol•L-1•min-1。
②再经一段时间后反应达到平衡,此时混合气体总物质的量为13mol,则平衡时NH3的物质的量为______ mol。
③下列可以说明该反应达到平衡状态的是______ (填标号)。
A.c(N2):c(NH3)=1:2
B.3v正(H2)=2v逆(NH3)
C.容器内气体的密度不再变化
D.混合气体的摩尔质量不再变化
E.单位时间内断开3molH-H的同时,断开6molN-H键
(3)KMnO4是实验室中常用的一种试剂。回答下列问题:
在酸性高锰酸钾溶液中滴加过量的草酸(H2C2O4)溶液,振荡,溶液紫色褪去,同时产生能使带火星的木条熄灭的气体,发生的离子反应方程式为_______ ,若将该反应设计成原电池,则正极反应式为:______ 。
(4)为了探究外界条件对化学反应速率的影响,设计如表方案:
①V=______ 。
②利用实验Ⅲ中数据计算,用H2C2O4的浓度变化表示的反应速率为v(H2C2O4)=______ mol•L-1•min-1(用含t3的最简分数表示)。
③该小组根据经验绘制了n(Mn2+)随时间变化的趋势如图1所示,但有同学查阅已有实验资料发现,该实验过程中n(Mn2+)随时间变化的实际趋势如图2所示。
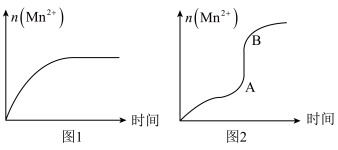
AB段反应速率增大的原因可能是_______ (填字母)。
a.该反应是放热反应 b.H+起催化作用 c.K+起催化作用 d.Mn2+起催化作用 e.SO 起催化作用
起催化作用
 2NH3(g)。回答下列问题:
2NH3(g)。回答下列问题:(1)已知断开1mol化学键所吸收的能量如下:H-H436kJ,N-H391kJ,N≡N946kJ。则N2(g)+3H2(g)
 2NH3(g)反应中生成17gNH3
2NH3(g)反应中生成17gNH3(2)恒温下,将6molN2与17molH2的混合气体通入2L的恒容密闭容器中,进行合成氨反应,当反应进行到5s时,有0.1molNH3生成。
①0~5s内用H2表示该反应的平均反应速率v(H2)=
②再经一段时间后反应达到平衡,此时混合气体总物质的量为13mol,则平衡时NH3的物质的量为
③下列可以说明该反应达到平衡状态的是
A.c(N2):c(NH3)=1:2
B.3v正(H2)=2v逆(NH3)
C.容器内气体的密度不再变化
D.混合气体的摩尔质量不再变化
E.单位时间内断开3molH-H的同时,断开6molN-H键
(3)KMnO4是实验室中常用的一种试剂。回答下列问题:
在酸性高锰酸钾溶液中滴加过量的草酸(H2C2O4)溶液,振荡,溶液紫色褪去,同时产生能使带火星的木条熄灭的气体,发生的离子反应方程式为
(4)为了探究外界条件对化学反应速率的影响,设计如表方案:
| 实验 | 0.1mol/L KMnO4/mL | 0.5mol/L H2C2O4/mL | 0.1mol/L H2SO4/mL | 水浴温度/℃ | 蒸馏水/mL | 褪色时间/min |
| Ⅰ | 5.0 | 15.0 | 5.0 | 35 | 0 | t1 |
| Ⅱ | 5.0 | 10.0 | 5.0 | 35 | 5.0 | t2 |
| Ⅲ | 5.0 | 15.0 | 3.0 | 35 | V | t3 |
②利用实验Ⅲ中数据计算,用H2C2O4的浓度变化表示的反应速率为v(H2C2O4)=
③该小组根据经验绘制了n(Mn2+)随时间变化的趋势如图1所示,但有同学查阅已有实验资料发现,该实验过程中n(Mn2+)随时间变化的实际趋势如图2所示。

AB段反应速率增大的原因可能是
a.该反应是放热反应 b.H+起催化作用 c.K+起催化作用 d.Mn2+起催化作用 e.SO
 起催化作用
起催化作用
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】钠硫电池作为一种新型储能电池,其应用逐渐得到重视和发展。
(1)钠硫电池以熔融金属钠、熔融硫和多硫化钠(Na2SX)分别作为两个电极的反应物,固体Al2O3陶瓷(可传导Na+)为电解质,其反应原理如下图所示:
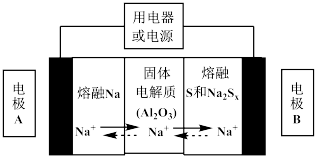
①根据上右表数据,请你判断该电池工作的适宜应控制在_________ (填字母)范围内。
a.100℃以下 b.100~300℃ c.300~350℃ d.350~2050℃
②放电时,电极A为_________ 极,电极B发生_________ 反应(填“氧化或还原”)
③充电时,总反应为Na2SX=2Na+xS(3<x<5),则阳极的电极反应式为:________________ 。
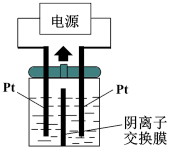
(2)若把钠硫电池作为电源,电解槽内装有KI及淀粉溶液如图所示,槽内的中间用阴离子交换膜隔开。通电一段时间后,发现左侧溶液变蓝色,一段时间后,蓝色逐渐变浅。则右侧发生的电极方程式:___________ ;试分析左侧溶液蓝色逐渐变浅的可能原因是:___________ 。
(3)若把钠硫电池作为电源,按如图所示装置进行实验电解乙池和丙池:
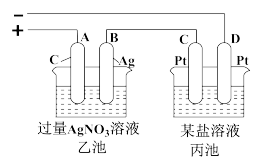
当钠硫电池中消耗0.05xmol的S时,理论上乙池中B极的质量增加__________ g;此时丙装置中___________ (填“C”或“D”)电极析出7.20g金属,则丙装置中的某盐溶液可能是_______ (填序号)。
a.MgSO4溶液 b.CuSO4溶液 c.NaCl溶液 d.AgNO3溶液
(1)钠硫电池以熔融金属钠、熔融硫和多硫化钠(Na2SX)分别作为两个电极的反应物,固体Al2O3陶瓷(可传导Na+)为电解质,其反应原理如下图所示:

①根据上右表数据,请你判断该电池工作的适宜应控制在
| 物质 | Na | S | Al2O3 |
| 熔点/℃ | 97.8 | 115 | 2050 |
| 沸点/℃ | 892 | 444.6 | 2980 |
a.100℃以下 b.100~300℃ c.300~350℃ d.350~2050℃
②放电时,电极A为
③充电时,总反应为Na2SX=2Na+xS(3<x<5),则阳极的电极反应式为:

(2)若把钠硫电池作为电源,电解槽内装有KI及淀粉溶液如图所示,槽内的中间用阴离子交换膜隔开。通电一段时间后,发现左侧溶液变蓝色,一段时间后,蓝色逐渐变浅。则右侧发生的电极方程式:
(3)若把钠硫电池作为电源,按如图所示装置进行实验电解乙池和丙池:

当钠硫电池中消耗0.05xmol的S时,理论上乙池中B极的质量增加
a.MgSO4溶液 b.CuSO4溶液 c.NaCl溶液 d.AgNO3溶液
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】二氧化硫易形成酸雨而污染大气,有效去除和利用 是环境保护的重要议题。
是环境保护的重要议题。
(1) 氧化法吸收
氧化法吸收 。向
。向 溶液中通入含有
溶液中通入含有 的烟气,反应温度为323K,反应一段时间。
的烟气,反应温度为323K,反应一段时间。
①上述反应的离子方程式为_______ 。
②随着吸收反应的进行,吸收剂溶液的pH逐渐_______ (填“增大”、“不变”或“减小”)。
(2) 利用。
利用。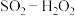 燃料电池的示意图如图。电极a为电池的
燃料电池的示意图如图。电极a为电池的_______ 极,电极b上发生的电极反应为_______ 。
(3)用含碘废水、 制取碘酸钾,其工艺流程如下:
制取碘酸钾,其工艺流程如下:

①检验含碘废水中是否含有 的常用试剂是
的常用试剂是_______ (写试剂名称)。
②通入 的目的是将
的目的是将 还原为
还原为 ,该反应的离子方程式为
,该反应的离子方程式为_______ 。
③该工艺的五种物质的制备反应中,不涉及氧化还原反应的步骤是“制_______ ”。
 是环境保护的重要议题。
是环境保护的重要议题。(1)
 氧化法吸收
氧化法吸收 。向
。向 溶液中通入含有
溶液中通入含有 的烟气,反应温度为323K,反应一段时间。
的烟气,反应温度为323K,反应一段时间。①上述反应的离子方程式为
②随着吸收反应的进行,吸收剂溶液的pH逐渐
(2)
 利用。
利用。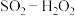 燃料电池的示意图如图。电极a为电池的
燃料电池的示意图如图。电极a为电池的
(3)用含碘废水、
 制取碘酸钾,其工艺流程如下:
制取碘酸钾,其工艺流程如下:
①检验含碘废水中是否含有
 的常用试剂是
的常用试剂是②通入
 的目的是将
的目的是将 还原为
还原为 ,该反应的离子方程式为
,该反应的离子方程式为③该工艺的五种物质的制备反应中,不涉及氧化还原反应的步骤是“制
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】本题为《化学与生活(选修1)》选做题
请根据题意,选择恰当的选项用字母代号填空。
(1)均衡营养和正确使用药物是保证身心健康的重要方面,现有下列四种物质:
A.葡萄糖 B.氨基酸 C.麻黄碱 D.阿司匹林
①蛋白质水解的最终产物是_______ ;
②人体内最重要的供能物质是________ ;
③具有解热镇痛作用,用于治疗感冒的是_______ ;
④对支气管哮喘症有明显疗效的是_________ 。
(2)材料是人类赖以生存和发展的重要物质基础。
①试管、烧杯和烧瓶等化学仪器的主要材质是________ ;
A.玻璃 B.陶瓷
②钢铁是目前用量最大的铁合金。钢铁接触海水发生电化学腐蚀,其负极反应式为_________ ;
A.O2+2H2O + 4e- = 4OH- B.Fe - 2e -= Fe2+
因此,为防止轮船船体被腐蚀,可在船体上安装一定量的_______ 。
A.锌块 B.铜块
(3)当前,环境治理已成为重要的民生工程。
①2014年1月,教育部规定在学校公共场所禁止吸烟。下列有关说法中,不正确
的是_________ ;
A.吸烟会对室内和公共场所造成污染
B.吸入焦油、尼古丁及颗粒物可导致多种病变
C.N2、CO2、CO和尼古丁都属于室内空气污染物
②下列做法可能会加重“雾霾”的是______ ;
A.大量焚烧秸秆
B.在汽车尾气系统装置催化转化器
C.发展煤的气化和液化等洁净煤技术
③下列处理垃圾的方法中,不正确的是_____________ 。
A.回收利用废纸 B.回收利用易拉罐 C.填埋废旧电池
请根据题意,选择恰当的选项用字母代号填空。
(1)均衡营养和正确使用药物是保证身心健康的重要方面,现有下列四种物质:
A.葡萄糖 B.氨基酸 C.麻黄碱 D.阿司匹林
①蛋白质水解的最终产物是
②人体内最重要的供能物质是
③具有解热镇痛作用,用于治疗感冒的是
④对支气管哮喘症有明显疗效的是
(2)材料是人类赖以生存和发展的重要物质基础。
①试管、烧杯和烧瓶等化学仪器的主要材质是
A.玻璃 B.陶瓷
②钢铁是目前用量最大的铁合金。钢铁接触海水发生电化学腐蚀,其负极反应式为
A.O2+2H2O + 4e- = 4OH- B.Fe - 2e -= Fe2+
因此,为防止轮船船体被腐蚀,可在船体上安装一定量的
A.锌块 B.铜块
(3)当前,环境治理已成为重要的民生工程。
①2014年1月,教育部规定在学校公共场所禁止吸烟。下列有关说法中,不正确
的是
A.吸烟会对室内和公共场所造成污染
B.吸入焦油、尼古丁及颗粒物可导致多种病变
C.N2、CO2、CO和尼古丁都属于室内空气污染物
②下列做法可能会加重“雾霾”的是
A.大量焚烧秸秆
B.在汽车尾气系统装置催化转化器
C.发展煤的气化和液化等洁净煤技术
③下列处理垃圾的方法中,不正确的是
A.回收利用废纸 B.回收利用易拉罐 C.填埋废旧电池
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】如图所示,水槽中试管内有一枚铁钉,放置数天观察:

(1)铁钉在逐渐生锈。
(2)若试管内液面上升,发生___ 腐蚀,正极反应式:___ 。
(3)若试管内液面下降,正极反应式:___ 。

(1)铁钉在逐渐生锈。
(2)若试管内液面上升,发生
(3)若试管内液面下降,正极反应式:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】金属的腐蚀
(1)概念:金属或合金与周围的_______ 发生_______ 反应而引起损耗的现象。其实质是金属原子_______ 电子变为阳离子,金属发生_______ 反应。
(2)根据与金属接触的_______ 不同,金属腐蚀可分为两类:
①化学腐蚀:金属与其表面接触的一些物质(如_______ 等)直接反应而引起的腐蚀。腐蚀的速率随温度升高而_______ 。
②电化学腐蚀:当_______ 的金属与_______ 溶液接触时会发生_______ 反应,比较_______ 的金属发生氧化反应而被腐蚀。
(1)概念:金属或合金与周围的
(2)根据与金属接触的
①化学腐蚀:金属与其表面接触的一些物质(如
②电化学腐蚀:当
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】电化学原理在防止金属腐蚀、能量转换、物质制备等方面应用广泛。
(1)钢闸门在海水中易被腐蚀,常用以下两种方法减少其腐蚀:
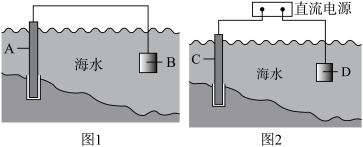
①图1中,A为钢闸门,材料B可以选择___ (填字母序号)。
a.碳棒 b.铜板 c.锌板
②图2中,钢闸门C做___ 极。用氯化钠溶液模拟海水进行实验,D为石墨块,则D电极反应式为___ ,检验该电极反应产物的方法___ 。
(2)镁燃料电池在可移动电子设备电源和备用电源等方面应用前景广阔。图3为“镁—次氯酸盐”燃料电池原理示意图,电极为镁合金和铂合金。E为该燃料电池的___ 极(填“正”或“负”)。F电极上的电极反应式为___ 。
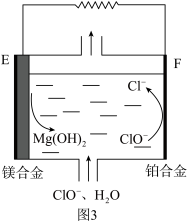
(3)利用电化学法生产硫酸,可使绝大多数单质硫直接转化为SO3,在生产硫酸的同时还能化学发电。图4为电化学法生产硫酸的工艺示意图,电池以固体金属氧化物作电解质,该电解质能传导O2-离子。
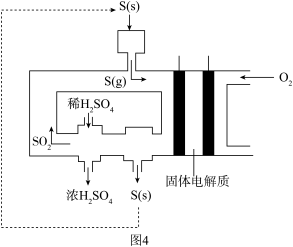
①正极每消耗4.48LO2(标准状况下),电路中转移电子的数目为___ 。
②S(g)在负极生成SO3的电极反应式为___ 。
(1)钢闸门在海水中易被腐蚀,常用以下两种方法减少其腐蚀:

①图1中,A为钢闸门,材料B可以选择
a.碳棒 b.铜板 c.锌板
②图2中,钢闸门C做
(2)镁燃料电池在可移动电子设备电源和备用电源等方面应用前景广阔。图3为“镁—次氯酸盐”燃料电池原理示意图,电极为镁合金和铂合金。E为该燃料电池的

(3)利用电化学法生产硫酸,可使绝大多数单质硫直接转化为SO3,在生产硫酸的同时还能化学发电。图4为电化学法生产硫酸的工艺示意图,电池以固体金属氧化物作电解质,该电解质能传导O2-离子。

①正极每消耗4.48LO2(标准状况下),电路中转移电子的数目为
②S(g)在负极生成SO3的电极反应式为
您最近一年使用:0次
【推荐2】Ⅰ.某化学兴趣小组的同学学了金属的电化学腐蚀,对教材叙述[钢铁在酸性环境中发生析氢腐蚀;在酸性很弱或呈中性,溶有 的环境中发生吸氧腐蚀;钢铁等金属的腐蚀主要为吸氧腐蚀]产生疑问,决定用数字化实验模拟探究钢铁在酸性环境下的腐蚀情况。
的环境中发生吸氧腐蚀;钢铁等金属的腐蚀主要为吸氧腐蚀]产生疑问,决定用数字化实验模拟探究钢铁在酸性环境下的腐蚀情况。
(1)用图1所示装置进行实验:打开a________ (填仪器名称)的活塞,加入1mL溶液,测得压强随时间变化曲线如图2。
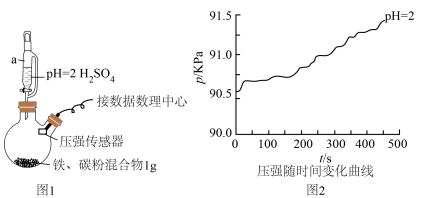
同学甲得出结论:酸性条件下,铁粉发生析氢腐蚀。
(2)同学乙认为甲的结论不科学,锥形瓶内压强变大还可能是___________ ,提出改进措施___________ 。改进后,再次实验,证明甲、乙的猜想均正确,请在图2绘制出改进后的曲线___________ 。
(3)同学丙认为甲、乙的实验不具代表性,建议用不同浓度的酸进行实验。在改进后的装置中分别用 、
、 的硫酸实验,测定压强随时间变化情况,结果如图3.同学丙得出:酸性较弱时,铁会发生吸氧腐蚀,其依据是
的硫酸实验,测定压强随时间变化情况,结果如图3.同学丙得出:酸性较弱时,铁会发生吸氧腐蚀,其依据是___________ 。
(4)对于图3中 时,铁是否发生了腐蚀?同学们意见不统一,经讨论,他们把压强传感器换成氧气传感器,得出不同pH时装置中
时,铁是否发生了腐蚀?同学们意见不统一,经讨论,他们把压强传感器换成氧气传感器,得出不同pH时装置中 浓度随时间的变化曲线如图4。
浓度随时间的变化曲线如图4。
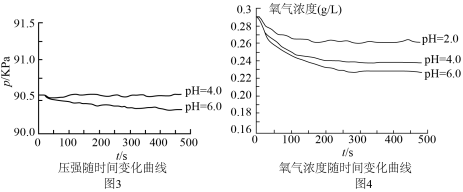
结合实验分析: 时,压强几乎不随时间改变是因为
时,压强几乎不随时间改变是因为___________ 。
综上,小组同学得出结论:教材表述科学严谨。
Ⅱ.拓展研究:
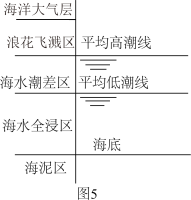
(5)侯保荣院士专门研究海洋钢架结构桥海洋大气层梁腐蚀,他发现腐蚀最严重的是浪花飞溅区浪花飞溅区(海洋环境分区如图5),请你解释原因___________ 。
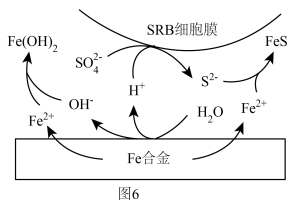
(6)科学家还发现在 浓度很小的海底也有厌氧微生物(如硫酸盐还原菌SRB)对海洋钢制部件的腐蚀,其原理如图6,已知溶液中的
浓度很小的海底也有厌氧微生物(如硫酸盐还原菌SRB)对海洋钢制部件的腐蚀,其原理如图6,已知溶液中的 完全转化为FeS,请写出该铁合金腐蚀的总反应
完全转化为FeS,请写出该铁合金腐蚀的总反应___________ (离子方程式)。
(7)请列举出生产生活中金属制品的防腐措施___________ (任写一点即可)。
 的环境中发生吸氧腐蚀;钢铁等金属的腐蚀主要为吸氧腐蚀]产生疑问,决定用数字化实验模拟探究钢铁在酸性环境下的腐蚀情况。
的环境中发生吸氧腐蚀;钢铁等金属的腐蚀主要为吸氧腐蚀]产生疑问,决定用数字化实验模拟探究钢铁在酸性环境下的腐蚀情况。(1)用图1所示装置进行实验:打开a

同学甲得出结论:酸性条件下,铁粉发生析氢腐蚀。
(2)同学乙认为甲的结论不科学,锥形瓶内压强变大还可能是
(3)同学丙认为甲、乙的实验不具代表性,建议用不同浓度的酸进行实验。在改进后的装置中分别用
 、
、 的硫酸实验,测定压强随时间变化情况,结果如图3.同学丙得出:酸性较弱时,铁会发生吸氧腐蚀,其依据是
的硫酸实验,测定压强随时间变化情况,结果如图3.同学丙得出:酸性较弱时,铁会发生吸氧腐蚀,其依据是(4)对于图3中
 时,铁是否发生了腐蚀?同学们意见不统一,经讨论,他们把压强传感器换成氧气传感器,得出不同pH时装置中
时,铁是否发生了腐蚀?同学们意见不统一,经讨论,他们把压强传感器换成氧气传感器,得出不同pH时装置中 浓度随时间的变化曲线如图4。
浓度随时间的变化曲线如图4。
结合实验分析:
 时,压强几乎不随时间改变是因为
时,压强几乎不随时间改变是因为综上,小组同学得出结论:教材表述科学严谨。
Ⅱ.拓展研究:
(5)侯保荣院士专门研究海洋钢架结构桥海洋大气层梁腐蚀,他发现腐蚀最严重的是浪花飞溅区浪花飞溅区(海洋环境分区如图5),请你解释原因

(6)科学家还发现在
 浓度很小的海底也有厌氧微生物(如硫酸盐还原菌SRB)对海洋钢制部件的腐蚀,其原理如图6,已知溶液中的
浓度很小的海底也有厌氧微生物(如硫酸盐还原菌SRB)对海洋钢制部件的腐蚀,其原理如图6,已知溶液中的 完全转化为FeS,请写出该铁合金腐蚀的总反应
完全转化为FeS,请写出该铁合金腐蚀的总反应
(7)请列举出生产生活中金属制品的防腐措施
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】(1)某研究性学习小组设计了如图所示装置探究钢铁的腐蚀与防护。

为防止金属Fe被腐蚀,可以采用上述________ (填装置序号)装置原理进行防护;装置③中总反应的离子方程式为_________ 。
(2)为处理银器表面的黑斑(Ag2S),将银器浸于铝质容器里的食盐水中并与铝接触,Ag2S转化为Ag,食盐水的作用为__________ 。
(3)纳米级Cu2O由于具有优良的催化性能而受到关注,采用肼(N2H4)燃料电池为电源,用离子交换膜控制电解液中c(OH-)制备纳米Cu2O,其装置如图甲、乙。

①上述装置中D电极应连接肼燃料电池的________ 极(填“A”或“B”)。
②该电解池的阳极反应式为_______ 。
③当反应生成14.4 g Cu2O时,至少需要肼________ mol。

为防止金属Fe被腐蚀,可以采用上述
(2)为处理银器表面的黑斑(Ag2S),将银器浸于铝质容器里的食盐水中并与铝接触,Ag2S转化为Ag,食盐水的作用为
(3)纳米级Cu2O由于具有优良的催化性能而受到关注,采用肼(N2H4)燃料电池为电源,用离子交换膜控制电解液中c(OH-)制备纳米Cu2O,其装置如图甲、乙。

①上述装置中D电极应连接肼燃料电池的
②该电解池的阳极反应式为
③当反应生成14.4 g Cu2O时,至少需要肼
您最近一年使用:0次


 。
。

