电化学原理在防止金属腐蚀、能量转换、物质制备等方面应用广泛。
(1)钢闸门在海水中易被腐蚀,常用以下两种方法减少其腐蚀:
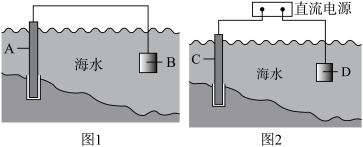
①图1中,A为钢闸门,材料B可以选择___ (填字母序号)。
a.碳棒 b.铜板 c.锌板
②图2中,钢闸门C做___ 极。用氯化钠溶液模拟海水进行实验,D为石墨块,则D电极反应式为___ ,检验该电极反应产物的方法___ 。
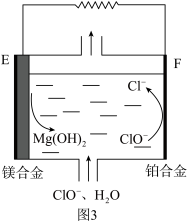
(2)镁燃料电池在可移动电子设备电源和备用电源等方面应用前景广阔。图3为“镁—次氯酸盐”燃料电池原理示意图,电极为镁合金和铂合金。E为该燃料电池的___ 极(填“正”或“负”)。F电极上的电极反应式为___ 。
(3)利用电化学法生产硫酸,可使绝大多数单质硫直接转化为SO3,在生产硫酸的同时还能化学发电。图4为电化学法生产硫酸的工艺示意图,电池以固体金属氧化物作电解质,该电解质能传导O2-离子。
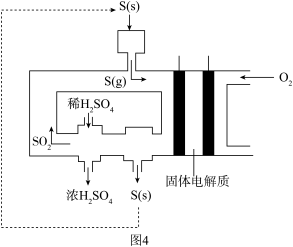
①正极每消耗4.48LO2(标准状况下),电路中转移电子的数目为___ 。
②S(g)在负极生成SO3的电极反应式为___ 。
(1)钢闸门在海水中易被腐蚀,常用以下两种方法减少其腐蚀:

①图1中,A为钢闸门,材料B可以选择
a.碳棒 b.铜板 c.锌板
②图2中,钢闸门C做
(2)镁燃料电池在可移动电子设备电源和备用电源等方面应用前景广阔。图3为“镁—次氯酸盐”燃料电池原理示意图,电极为镁合金和铂合金。E为该燃料电池的

(3)利用电化学法生产硫酸,可使绝大多数单质硫直接转化为SO3,在生产硫酸的同时还能化学发电。图4为电化学法生产硫酸的工艺示意图,电池以固体金属氧化物作电解质,该电解质能传导O2-离子。

①正极每消耗4.48LO2(标准状况下),电路中转移电子的数目为
②S(g)在负极生成SO3的电极反应式为
更新时间:2020-01-18 19:01:32
|
相似题推荐
【推荐1】某课外活动小组用如图装置进行实验,试回答下列问题:
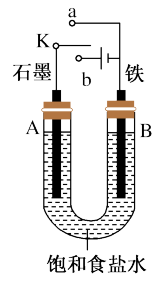
(1)若开始时开关K与a连接,B极的Fe发生_______ 腐蚀(填“析氢”或“吸氧”)。
(2)若开始时开关K与b连接,下列说法正确的是_______ (填序号)。
① 溶液中Na+向A极移动
② 从A极处逸出的气体能使湿润的KI淀粉试纸变蓝
③ 反应一段时间后加适量盐酸可恢复到电解前电解质的浓度
④ 若标准状况下B极产生2.24 L气体,则溶液中转移0.2 mol电子
(3)该小组同学认为,如果模拟工业上离子交换膜法制烧碱的方法,那么可以设想用如图装置电解硫酸钾溶液来制取氢气、氧气、硫酸和氢氧化钾。

① 该电解槽的阳极反应式为_______ ,此时通过阴离子交换膜的离子数_______ (填“大于”“小于”或“等于”)通过阳离子交换膜的离子数。
② 制得的氢氧化钾溶液从出口_______ (填“A”“B”“C”或“D”)导出。
(4)用惰性电极电解体积为1L的CuSO4溶液,当阴阳极都产生3.36L(标况)气体时,请问硫酸铜的浓度为_______ ,若要此溶液恢复到原状态需要加入_______ (填选项)。
ACuSO4 BCuO CCu(OH)2 DCu2(OH)2CO3

(1)若开始时开关K与a连接,B极的Fe发生
(2)若开始时开关K与b连接,下列说法正确的是
① 溶液中Na+向A极移动
② 从A极处逸出的气体能使湿润的KI淀粉试纸变蓝
③ 反应一段时间后加适量盐酸可恢复到电解前电解质的浓度
④ 若标准状况下B极产生2.24 L气体,则溶液中转移0.2 mol电子
(3)该小组同学认为,如果模拟工业上离子交换膜法制烧碱的方法,那么可以设想用如图装置电解硫酸钾溶液来制取氢气、氧气、硫酸和氢氧化钾。

① 该电解槽的阳极反应式为
② 制得的氢氧化钾溶液从出口
(4)用惰性电极电解体积为1L的CuSO4溶液,当阴阳极都产生3.36L(标况)气体时,请问硫酸铜的浓度为
ACuSO4 BCuO CCu(OH)2 DCu2(OH)2CO3
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
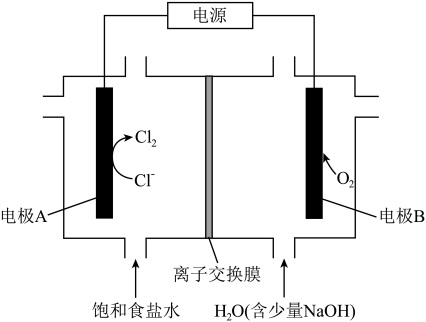
【推荐2】氯碱工业能耗大,通过如图的结构可大幅度降低能耗。_______ 离子交换膜 (填“正”或“负”)。
(2)反应的总化学方程式为_______ 。
(3)当电路中通过0.2mol电子时, 右侧溶液质量_____ (填“增加”或“减少”) _______ g。
(2)反应的总化学方程式为
(3)当电路中通过0.2mol电子时, 右侧溶液质量
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】下图是一个化学过程的示意图。

(1)图中甲池是________ 装置(填“电解池”或“原电池”)
(2)写出通入CH3OH的电极的电极反应式:_______________________ 。
(3)向乙池两电极附近分别滴加适量紫色石蕊试液,附近变红的电极为________ 极(填“A”或“B”),并写出此电极的电极反应式:______________ 。
(4)若丙中电极不变,将其溶液换成NaCl溶液,丙池中总反应的离子方程式:__________ 。
(5)常温下,当乙池中B(Ag)极的质量增加5.40 g时,乙池的pH是________ (若此时乙池中溶液的体积为500 mL);

(1)图中甲池是
(2)写出通入CH3OH的电极的电极反应式:
(3)向乙池两电极附近分别滴加适量紫色石蕊试液,附近变红的电极为
(4)若丙中电极不变,将其溶液换成NaCl溶液,丙池中总反应的离子方程式:
(5)常温下,当乙池中B(Ag)极的质量增加5.40 g时,乙池的pH是
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】钢铁很容易生锈而被腐蚀,每年因腐蚀而损失的钢材占世界钢铁年产量的四分之一。

(1)钢铁腐蚀主要是吸氧腐蚀,该腐蚀过程中的电极反应式为:
正极__________ ,负极________ 。
(2)为了降低某水库的铁闸门被腐蚀的速率,可以采用甲图所示的方案,其中焊接在闸门上的固体材料R可以采用________ 。
A 铜 B 钠 C 锌 D 石墨
(3)乙图所示的方案也可以降低铁闸门的腐蚀速率,其中铁闸门应该连接在直流电源的________ 极。

(1)钢铁腐蚀主要是吸氧腐蚀,该腐蚀过程中的电极反应式为:
正极
(2)为了降低某水库的铁闸门被腐蚀的速率,可以采用甲图所示的方案,其中焊接在闸门上的固体材料R可以采用
A 铜 B 钠 C 锌 D 石墨
(3)乙图所示的方案也可以降低铁闸门的腐蚀速率,其中铁闸门应该连接在直流电源的
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】I.将质量相等的铁片和铜片用导线相连浸入500mL硫酸铜溶液中构成如图1的装置(以下均假设反应过程中溶液体积不变)。
(1)铜片上的电极反应式为___ ,电流由___ (填“铁片”或“铜片”)流向___ 。
(2)若2min后测得铁片和铜片之间的质量差为2.4g,计算导线中流过的电子的物质的量为___ mol。
II.金属的电化学腐蚀的本质是形成了原电池。如图2所示,烧杯中都盛有稀硫酸。
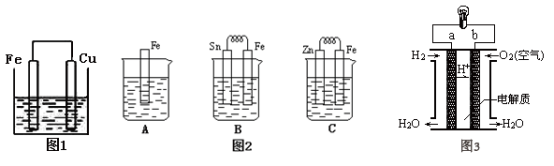
(1)图2的B中的Sn为___ 极,Sn极附近溶液的酸性___ (填增强、减弱或不变)。
(2)图2的C中被腐蚀的金属是___ 。比较A、B、C中纯铁被腐蚀的速率由快到慢的顺序是___ 。
III.人们应用原电池原理制作了多种电池,以满足不同的需要。燃料电池是一种高效、环境友好的供电装置,如图3是电解质为稀硫酸溶液的氢氧燃料电池原理示意图,回答下列问题:
(1)写出该氢氧燃料电池的正极电极反应式___ 。
(2)电池工作一段时间后硫酸溶液的浓度___ (填“增大”、“减小”或“不变”)。
(1)铜片上的电极反应式为
(2)若2min后测得铁片和铜片之间的质量差为2.4g,计算导线中流过的电子的物质的量为
II.金属的电化学腐蚀的本质是形成了原电池。如图2所示,烧杯中都盛有稀硫酸。

(1)图2的B中的Sn为
(2)图2的C中被腐蚀的金属是
III.人们应用原电池原理制作了多种电池,以满足不同的需要。燃料电池是一种高效、环境友好的供电装置,如图3是电解质为稀硫酸溶液的氢氧燃料电池原理示意图,回答下列问题:
(1)写出该氢氧燃料电池的正极电极反应式
(2)电池工作一段时间后硫酸溶液的浓度
您最近半年使用:0次



