下图是一个化学过程的示意图。

(1)图中甲池是________ 装置(填“电解池”或“原电池”)
(2)写出通入CH3OH的电极的电极反应式:_______________________ 。
(3)向乙池两电极附近分别滴加适量紫色石蕊试液,附近变红的电极为________ 极(填“A”或“B”),并写出此电极的电极反应式:______________ 。
(4)若丙中电极不变,将其溶液换成NaCl溶液,丙池中总反应的离子方程式:__________ 。
(5)常温下,当乙池中B(Ag)极的质量增加5.40 g时,乙池的pH是________ (若此时乙池中溶液的体积为500 mL);

(1)图中甲池是
(2)写出通入CH3OH的电极的电极反应式:
(3)向乙池两电极附近分别滴加适量紫色石蕊试液,附近变红的电极为
(4)若丙中电极不变,将其溶液换成NaCl溶液,丙池中总反应的离子方程式:
(5)常温下,当乙池中B(Ag)极的质量增加5.40 g时,乙池的pH是
更新时间:2018-11-16 15:27:48
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】吸入氧气、排出二氧化碳,这看似再简单不过的新陈代谢,在遥远的太空中却并不容易,因为在航天服、航天器、空间站等密闭系统中,CO2浓度会高得多,而超过一定浓度会导致呼吸急促、头晕头痛、昏迷甚至死亡,因此必须通过一定方法将CO2清除。
I.非再生式氢氧化锂(LiOH)除碳技术
(1)我国“飞天”舱外航天服采用非再生式氢氧化锂(LiOH)吸附CO2生成碳酸锂,该技术设备操作简单,功能可靠,适用于短期出舱任务。吸附时发生反应的化学方程式为___________ 。采用LiOH而不用NaOH的原因是___________ 。
Ⅱ.再生式快速循环胺技术
(2)以固态胺作为吸附剂,吸附CO2与水蒸气。当固态胺吸附饱和后,将其暴露于真空中,破坏碳酸氢盐的化学键,释放出CO2,从而完成吸附剂的再生。该技术大大提升了舱外航天服的续航时间。固态胺的吸附是___________ 变化(填“物理”或“化学”)。
Ⅲ.萨巴蒂尔(Sabatier)除碳生氧技术
(3)利用萨巴蒂尔(Sabatier)反应清除二氧化碳并再生氧气的大体流程如下图所示。

下列说法错误的是___________。
Ⅳ.富集CO2的原电池模拟装置如图:

(4)b极为___________ 极,a电极上发生的电极反应为___________ 。
(5)上述电极材料采用多孔碳载镍,“多孔”的优点是___________ 。
(6)该装置若消耗2molH2,则理论上在b极除去CO2的质量为___________ 。
V.能量存储与循环技术
(7)将电解水装置与燃料电池配合使用,可实现充放电的循环过程,应用于长寿命的航天器中,工作原理如图:

关于该循环系统下列说法正确的是___________
I.非再生式氢氧化锂(LiOH)除碳技术
(1)我国“飞天”舱外航天服采用非再生式氢氧化锂(LiOH)吸附CO2生成碳酸锂,该技术设备操作简单,功能可靠,适用于短期出舱任务。吸附时发生反应的化学方程式为
Ⅱ.再生式快速循环胺技术
(2)以固态胺作为吸附剂,吸附CO2与水蒸气。当固态胺吸附饱和后,将其暴露于真空中,破坏碳酸氢盐的化学键,释放出CO2,从而完成吸附剂的再生。该技术大大提升了舱外航天服的续航时间。固态胺的吸附是
Ⅲ.萨巴蒂尔(Sabatier)除碳生氧技术
(3)利用萨巴蒂尔(Sabatier)反应清除二氧化碳并再生氧气的大体流程如下图所示。

下列说法错误的是___________。
| A.CO2的最终产物为CH4和O2 |
| B.电解水装置中,反应物的能量低于生成物的能量 |
| C.萨巴蒂尔反应器中反应的氧化剂与还原剂质量之比为11∶1 |
| D.物质转化中O、H原子的利用率均为100% |
Ⅳ.富集CO2的原电池模拟装置如图:

(4)b极为
(5)上述电极材料采用多孔碳载镍,“多孔”的优点是
(6)该装置若消耗2molH2,则理论上在b极除去CO2的质量为
V.能量存储与循环技术
(7)将电解水装置与燃料电池配合使用,可实现充放电的循环过程,应用于长寿命的航天器中,工作原理如图:

关于该循环系统下列说法正确的是___________
| A.该系统中存在着太阳能、电能、化学能和机械能之间的相互转化 |
| B.电解池中可选用CuSO4来增强水的导电性 |
| C.太阳能电池帆板的主要成分为SiO2 |
| D.利用太阳能代替化石能源符合“低碳经济” |
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】中国正在逐步建立自己的载人空间站“天宫”,神舟十三号载人飞船在北京时间10月16日0时23分点火发射,又一次正式踏上飞向浩渺星辰的征途。
(1)氢氧燃料电池(构造示意图如图)单位质量输出电能较高,反应生成的水可作为航天员的饮用水,氧气可以作为备用氧源供给航天员呼吸。由此判断X极为电池的___________ 极, 向
向___________ (填“正”或“负”)极作定向移动,Y极的电极反应式为___________ 。
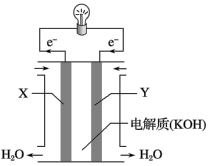
(2)在宇宙飞船或潜艇中,还可利用氢氧燃料电池所产生的水作为饮用水,今欲制得常温下180g水,则电池内电子转移的物质的量约为___________ mol
(3)“神舟”飞船的电源系统共有3种,分别是太阳能电池帆板、镉镍蓄电池和应急电池。
①飞船在光照区运行时,太阳能电池帆板将___________ 转化为___________ ,除供给飞船使用外,多余部分用镉镍蓄电池储存起来。其工作原理为: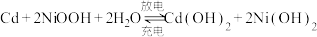 ,充电时,阳极的电极反应式为
,充电时,阳极的电极反应式为___________ ;
②当飞船运行到地影区时,镉镍蓄电池开始为飞船供电,此时负极附近溶液的碱性___________ (填“增大”“减小”或“不变”)。
(1)氢氧燃料电池(构造示意图如图)单位质量输出电能较高,反应生成的水可作为航天员的饮用水,氧气可以作为备用氧源供给航天员呼吸。由此判断X极为电池的
 向
向
(2)在宇宙飞船或潜艇中,还可利用氢氧燃料电池所产生的水作为饮用水,今欲制得常温下180g水,则电池内电子转移的物质的量约为
(3)“神舟”飞船的电源系统共有3种,分别是太阳能电池帆板、镉镍蓄电池和应急电池。
①飞船在光照区运行时,太阳能电池帆板将
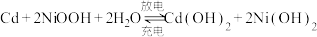 ,充电时,阳极的电极反应式为
,充电时,阳极的电极反应式为②当飞船运行到地影区时,镉镍蓄电池开始为飞船供电,此时负极附近溶液的碱性
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】某兴趣小组的同学用如图所示装置研究有关电化学的问题。当闭合该装置的电键时,观察到电流表的指针发生了偏转。
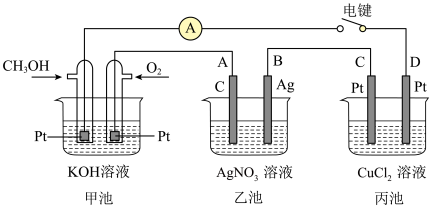
请回答下列问题:
(1)甲池为______ (填“原电池”“电解池”或“电镀池”),通入CH3OH 电极的电极反应式为 _____________________________________ 。
(2)乙池 A(石墨)电极的名称为_________ (填“正极”“负极”“阴极”或“阳极”),乙池中总反应式为 ____________________________________ 。
(3)当乙池中 B 极质量增加 5.40 g 时,甲池中理论上消耗 O2 的体积为_____________ mL(标准状况下),丙池中___________ 极析出 ______ g 铜。
(4)若丙中电极不变,将其溶液换成 NaCl 溶液,电键闭合一段时间后,丙中溶液的 pH 将_______ (填“增大”“减小”或“不变”)。

请回答下列问题:
(1)甲池为
(2)乙池 A(石墨)电极的名称为
(3)当乙池中 B 极质量增加 5.40 g 时,甲池中理论上消耗 O2 的体积为
(4)若丙中电极不变,将其溶液换成 NaCl 溶液,电键闭合一段时间后,丙中溶液的 pH 将
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】某锂电池的反应式为FePO4+Li LiFePO4,回答下列问题:
LiFePO4,回答下列问题:
(1)该蓄电池放电过程中发生还原反应的物质是___________ (写化学式),充电时外电路中转移了2mol电子,则阴极产物的质量为___________ g。
(2)若以该锂电池为电源,电解NaOH稀溶液,制备H2和O2,则阳极的电极反应式为___________ 。
(3)若利用该电源精炼铜,粗铜精炼过程中,因阳极杂质逐渐溶解,电解质溶液中Fe2+、Zn2+的浓度会逐渐增大,而这些杂质离子则会影响后续精炼。某同学设计下图所示的除杂方案:
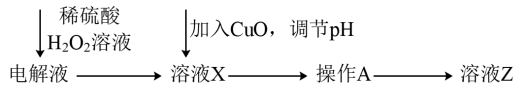
已知有关氢氧化物沉淀的pH如下表:
加入H2O2溶液时发生反应的离子方程式为___________ ;若要检验Fe2+是否完全转化为Fe3+,可选择的试剂是___________ ,对应现象是___________ ;调节pH=5.0时,则沉淀的离子主要是___________ (填离子符号);操作A的名称是___________ ;该同学的方案中未除去的杂质金属阳离子是___________ 。
 LiFePO4,回答下列问题:
LiFePO4,回答下列问题:(1)该蓄电池放电过程中发生还原反应的物质是
(2)若以该锂电池为电源,电解NaOH稀溶液,制备H2和O2,则阳极的电极反应式为
(3)若利用该电源精炼铜,粗铜精炼过程中,因阳极杂质逐渐溶解,电解质溶液中Fe2+、Zn2+的浓度会逐渐增大,而这些杂质离子则会影响后续精炼。某同学设计下图所示的除杂方案:

已知有关氢氧化物沉淀的pH如下表:
| 氢氧化物 | Fe(OH)3 | Cu(OH)2 | Zn(OH)2 | Fe(OH)2 |
| 开始沉淀时的pH | 2.3 | 5.6 | 6.2 | 7.5 |
| 完全沉淀时的pH | 3.9 | 6.4 | 8.0 | 9.7 |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】判断下列离子方程式的书写是否正确,并说明理由。
(1)在 溶液中通入足量氯气:
溶液中通入足量氯气:
_____
(2)用石墨电极材料电解 饱和溶液:
饱和溶液: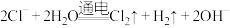
_____
(3)向 溶液中通入二氧化碳气体:
溶液中通入二氧化碳气体: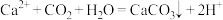
_____
(4)向 溶液中加入稀硫酸:
溶液中加入稀硫酸:
_____
(5)醋酸与锌粒反应: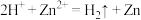
_____
(1)在
 溶液中通入足量氯气:
溶液中通入足量氯气:
(2)用石墨电极材料电解
 饱和溶液:
饱和溶液: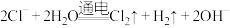
(3)向
 溶液中通入二氧化碳气体:
溶液中通入二氧化碳气体: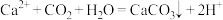
(4)向
 溶液中加入稀硫酸:
溶液中加入稀硫酸:
(5)醋酸与锌粒反应:
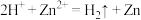
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】电化学脱硫技术是一种温和的净化技术,其基本原理为利用阳极反应产生的羟基自由基(·OH,氧元素为-1价)将燃煤中的含硫物质氧化除去,其装置示意图如图所示。
(1)将煤打成煤浆加入电解槽的目的是________ 。
(2)阳极的电极反应式为________ 。
(3)补全用羟基自由基除去煤中二硫化亚铁(FeS2)的反应的离子方程式:FeS2 +·OH =Fe3+ + SO42- + H2O +___ 。
(4)利用上述装置对某含FeS2的煤样品进行电解脱硫,测得一定时间内随溶液起始pH的改变脱硫率(溶于水中的硫元素质量占煤样中硫元素总质量的百分比)的变化如下图所示。
pH大于1.5后脱硫率下降的可能原因有:随着pH的升高,反应物的氧化性或还原性降低;________ 。

(1)将煤打成煤浆加入电解槽的目的是
(2)阳极的电极反应式为
(3)补全用羟基自由基除去煤中二硫化亚铁(FeS2)的反应的离子方程式:FeS2 +·OH =Fe3+ + SO42- + H2O +
(4)利用上述装置对某含FeS2的煤样品进行电解脱硫,测得一定时间内随溶液起始pH的改变脱硫率(溶于水中的硫元素质量占煤样中硫元素总质量的百分比)的变化如下图所示。

pH大于1.5后脱硫率下降的可能原因有:随着pH的升高,反应物的氧化性或还原性降低;
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】依据氧化还原反应:2Ag+(aq)+Cu(s) Cu2+(aq)+2Ag(s)设计的原电池如图所示。
Cu2+(aq)+2Ag(s)设计的原电池如图所示。

请回答下列问题:
(1)电极X的材料是_______ ;电解质溶液Y是____________ ;
(2)银电极为电池的___ 极,发生的电极反应为_____________ ;X电极上发生的电极反应为___________ ;
(3)外电路中的电子是从_______ 电极流向___________ 电极;
(4)如图所示,a、b、c均为石墨电极,d为碳钢电极,通电进行电解。假设在电解过程中产生的气体全部逸出,则

①a电极反应式为_________________________________ ;
②乙中的总反应为__________________________________ ;
③若整个电路中有2NA 个电子转移,则d电极产生__________ L气体 (标准状况)。
 Cu2+(aq)+2Ag(s)设计的原电池如图所示。
Cu2+(aq)+2Ag(s)设计的原电池如图所示。
请回答下列问题:
(1)电极X的材料是
(2)银电极为电池的
(3)外电路中的电子是从
(4)如图所示,a、b、c均为石墨电极,d为碳钢电极,通电进行电解。假设在电解过程中产生的气体全部逸出,则

①a电极反应式为
②乙中的总反应为
③若整个电路中有2NA 个电子转移,则d电极产生
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】回答下列问题
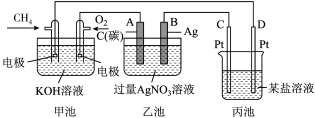
(1)图中甲池是_____ (“原电池”或“电解池”)装置,其中OH-移向 _____ (填“CH4”或“O2")极。
(2)写出通入CH4的电极的电极反应式:_______________________________________
(3)向乙池两电极附近分别滴加适量紫色石蕊溶液,附近变红的电极为_________ (填“A"或“B")极,并写出此电极的电极反应式______________________________________________
(4)乙池中总反应的离子方程式为______________________________
(5)常温下,当乙池中B(Ag)极的质量增加5.40g时,乙池的pH是_______________ (若此时乙池中溶液的体积为500mL);此时丙池某电极析出1.60g某金属,则丙中的某盐溶液可能是________________ (填字母)。
A.MgSO4 B.CuSO4 C.NaCl

(1)图中甲池是
(2)写出通入CH4的电极的电极反应式:
(3)向乙池两电极附近分别滴加适量紫色石蕊溶液,附近变红的电极为
(4)乙池中总反应的离子方程式为
(5)常温下,当乙池中B(Ag)极的质量增加5.40g时,乙池的pH是
A.MgSO4 B.CuSO4 C.NaCl
您最近一年使用:0次
【推荐3】纳米级Cu2O由于具有优良的催化性能而受到关注,采用肼(N2H4)燃料电池为电源,用离子交换膜控制电解液中c(OH-)制备纳米Cu2O,其装置如图甲、乙。
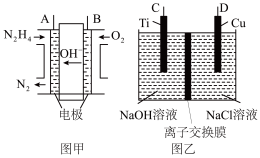
(1)上述装置中D电极应连接肼燃料电池的________ 极(填“A”或“B”),该电解池中离子交换膜为________ 离子交换膜(填“阴”或“阳”)。
(2)该电解池的阳极反应式为________________________________________ ,
肼燃料电池中A极发生的电极反应为____________________________ 。
(3)当反应生成14.4 g Cu2O时,至少需要肼________ mol。

(1)上述装置中D电极应连接肼燃料电池的
(2)该电解池的阳极反应式为
肼燃料电池中A极发生的电极反应为
(3)当反应生成14.4 g Cu2O时,至少需要肼
您最近一年使用:0次



