钢铁很容易生锈而被腐蚀,每年因腐蚀而损失的钢材占世界钢铁年产量的四分之一。

(1)钢铁腐蚀主要是吸氧腐蚀,该腐蚀过程中的电极反应式为:
正极__________ ,负极________ 。
(2)为了降低某水库的铁闸门被腐蚀的速率,可以采用甲图所示的方案,其中焊接在闸门上的固体材料R可以采用________ 。
A 铜 B 钠 C 锌 D 石墨
(3)乙图所示的方案也可以降低铁闸门的腐蚀速率,其中铁闸门应该连接在直流电源的________ 极。

(1)钢铁腐蚀主要是吸氧腐蚀,该腐蚀过程中的电极反应式为:
正极
(2)为了降低某水库的铁闸门被腐蚀的速率,可以采用甲图所示的方案,其中焊接在闸门上的固体材料R可以采用
A 铜 B 钠 C 锌 D 石墨
(3)乙图所示的方案也可以降低铁闸门的腐蚀速率,其中铁闸门应该连接在直流电源的
13-14高二·安徽安庆·课时练习 查看更多[12]
第4节 金属的腐蚀与防护新疆呼图壁县第一中学2021-2022学年高二上学期期中考试化学试题福建省泉州科技中学2021-2022学年高二上学期第一次月考化学试题(已下线)1.3 金属的腐蚀与防护(备作业)-【上好课】2021-2022学年高二化学同步备课系列(苏教版2019选择性必修1)选择性必修1(SJ)专题1第三单元 金属的腐蚀与防护(已下线)4.3.2 金属(练习)-2020-2021学年上学期高二化学同步精品课堂(新教材人教版选择性必修1)的防护鲁科版(2019)高二选择性必修第一册第1章 化学反应与能量变化 第4节 金属的腐蚀与防护步步为赢 高二化学寒假作业:作业十四 金属的腐蚀与防护福建省福州市长乐高级中学2019-2020学年高二上学期第一次月考化学(选考)试题2018-2019学年人教版高中化学选修四电化学基础章末综合测评题(四)(已下线)2015安徽望江中学同步课时(人教选修4)4.4金属的电化学腐蚀与防护2014—2015山东省泰安市高二上学期期末统考高二化学试卷
更新时间:2019-12-16 12:17:24
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】北京冬奥会赛区内将使用氢燃料清洁能源车辆,就是利用原电池原理提供清洁电能,回答下面问题:
(1)某氢氧燃料电池工作示意图如图1。

①电极a是_______ (填“正极”“负极”“阳极”或“阴极”),电极a发生的电极反应是_______ 。
②电解质KOH溶液中K+向_______ 电极移动(填“a”或“b”)。
(2)利用图1中的原电池电解饱和食盐水,可以有效的利用海水资源,原理如图:
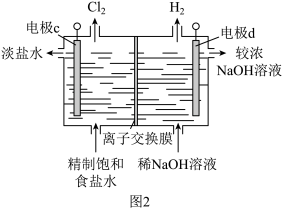
①电极d应连接图1装置的_______ 电极(填“a”或“b”),离子交换膜是_______ (填“阴离子交换膜”或“阳离子交换膜”)。
②写出电极c的电极反应_______ 。
③写出电解饱和食盐水的离子方程式_______ 。
(3)将铁钉的下半部分分别镀上铜和锌,放入培养皿中,加入饱和食盐水溶液,再各滴入几滴酚酞溶液和K3[Fe(CN)6]溶液。装置如图3:
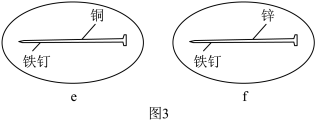
①在铁钉下半部分镀上铜的装置中,阳极材料是_______ (填化学式)。
②e装置中出现蓝色沉淀,铜电极发生的电极反应是_______ 。
③f装置中可能出现的现象是_______ 。
(1)某氢氧燃料电池工作示意图如图1。

①电极a是
②电解质KOH溶液中K+向
(2)利用图1中的原电池电解饱和食盐水,可以有效的利用海水资源,原理如图:

①电极d应连接图1装置的
②写出电极c的电极反应
③写出电解饱和食盐水的离子方程式
(3)将铁钉的下半部分分别镀上铜和锌,放入培养皿中,加入饱和食盐水溶液,再各滴入几滴酚酞溶液和K3[Fe(CN)6]溶液。装置如图3:

①在铁钉下半部分镀上铜的装置中,阳极材料是
②e装置中出现蓝色沉淀,铜电极发生的电极反应是
③f装置中可能出现的现象是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】材料的不断发展促进社会的进步。
(1)“天宫二号”内大量使用了碳纤维复合材料,在碳纤维复合材料中,碳纤维属于_____ (填“增强剂”或“基体”);聚乙烯塑料常用于食品包装,聚乙烯塑料属于_________ (填“热固性”或“热塑性”)塑料。硫化橡胶具有较高的强度和化学稳定性,它具有___________ 结构。天然橡胶的结构简式是________ (填字母)。
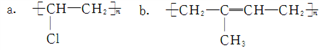 c. (C6H10O5)n
c. (C6H10O5)n
钢铁生锈的负极电极反应式为:_________________________ 。
(2)2015年某研究机构用一种新材料镍纳米粒子作催化剂,将二氧化碳和氢气在加热条件下转化为甲烷,该反应的化学方程式为________________________________ 。
(1)“天宫二号”内大量使用了碳纤维复合材料,在碳纤维复合材料中,碳纤维属于
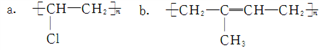 c. (C6H10O5)n
c. (C6H10O5)n钢铁生锈的负极电极反应式为:
(2)2015年某研究机构用一种新材料镍纳米粒子作催化剂,将二氧化碳和氢气在加热条件下转化为甲烷,该反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】铁及其化合物在生活、生产中有广泛应用。请回答下列问题:
(1)黄铁矿(FeS2)是生产硫酸和冶炼钢铁的重要原料。其中一个反应为
3FeS2+8O2 6SO2+Fe3O4,有3 molFeS2参加反应,转移
6SO2+Fe3O4,有3 molFeS2参加反应,转移_______ mol电子。
(2)氯化铁溶液常用作印刷电路铜板腐蚀剂,反应的离子方程式为_________ ;从腐蚀废液回收得到金属铜,还需要的试剂是_______________ 。
(3)与明矾相似,硫酸铁也可用作净水剂,在使用时发现硫酸铁并不能使酸性废水中的悬浮物沉降除去,其原因是____________________________
(4)钢铁的电化腐蚀简单示意图如下,将该图稍作修改即可成为钢铁电化学防护的简单示意图,请在下图虚线框内作出修改,并用箭头标出电子流动方向___________________ 。
(1)黄铁矿(FeS2)是生产硫酸和冶炼钢铁的重要原料。其中一个反应为
3FeS2+8O2
 6SO2+Fe3O4,有3 molFeS2参加反应,转移
6SO2+Fe3O4,有3 molFeS2参加反应,转移(2)氯化铁溶液常用作印刷电路铜板腐蚀剂,反应的离子方程式为
(3)与明矾相似,硫酸铁也可用作净水剂,在使用时发现硫酸铁并不能使酸性废水中的悬浮物沉降除去,其原因是
(4)钢铁的电化腐蚀简单示意图如下,将该图稍作修改即可成为钢铁电化学防护的简单示意图,请在下图虚线框内作出修改,并用箭头标出电子流动方向

您最近一年使用:0次
【推荐1】在日常生活中,金属腐蚀的现象普遍存在,金属腐蚀常常是自发进行的。回答下列问题:
(1)钢铁腐蚀分为析氢腐蚀和吸氧腐蚀:
①在酸性环境中,主要发生的腐蚀称为___________ (填“析氢”或“吸氧”)腐蚀,此时正极上的电极反应式为___________ 。
②发生吸氧腐蚀时,每转移0.2mol电子,消耗气体的体积为___________ mL(标准状况下)。
(2)钢铁的保护法如图所示:___________ (填“牺牲阳极保护法”或“外加电流法”),此时锌板上发生的电极反应为___________ 。
②图2中,a为电源的___________ (填“正”或“负”)极,判断的理由为___________ 。
(1)钢铁腐蚀分为析氢腐蚀和吸氧腐蚀:
①在酸性环境中,主要发生的腐蚀称为
②发生吸氧腐蚀时,每转移0.2mol电子,消耗气体的体积为
(2)钢铁的保护法如图所示:
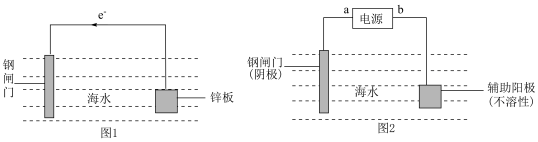
②图2中,a为电源的
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】氧化还原反应与电化学及金属的防护知识密切相关。请回答下列问题:
Ⅰ.依据反应:2Ag+(aq)+Cu= Cu2+ (aq) +2Ag设计的原电池如图1所示。则电解质溶液Y是___________ (填化学式),X的电极反应式__________________ 。若将盐桥换成铜丝,则X电极名称是____________ 。

Ⅱ.用图2的装置进实验。
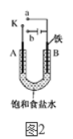
(1)若A为Zn,实验时开关K与a连接,则能模拟钢铁的一种电化学防护方法,名称为______ 。
(2)若A为石墨,将开关K与b连接,则有关该实验的说法正确的是(填序号)________ 。
①溶液中Na+向A极移动
②从A极处逸出的气体能使湿润的蓝色石蕊试纸先变红后褪色
③反应一段时间后加适量盐酸可恢复到电解前电解质的浓度
④若标准状况下B极产生2.24 L气体,则电路中转移0.2 mol电子
⑤电子流动方向:电源负极→B→饱和食盐水→A→电源正极
⑥若实验前滴入酚酞,B极区附近溶液先变红
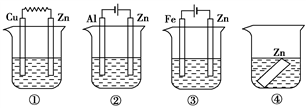
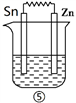
Ⅲ.如下图所示装置中都盛有0.1 mol/L的NaCl溶液,放置一定时间后,装置中的五块相同锌片,腐蚀速率由快到慢的正确顺序是______________ 。
Ⅰ.依据反应:2Ag+(aq)+Cu= Cu2+ (aq) +2Ag设计的原电池如图1所示。则电解质溶液Y是

Ⅱ.用图2的装置进实验。

(1)若A为Zn,实验时开关K与a连接,则能模拟钢铁的一种电化学防护方法,名称为
(2)若A为石墨,将开关K与b连接,则有关该实验的说法正确的是(填序号)
①溶液中Na+向A极移动
②从A极处逸出的气体能使湿润的蓝色石蕊试纸先变红后褪色
③反应一段时间后加适量盐酸可恢复到电解前电解质的浓度
④若标准状况下B极产生2.24 L气体,则电路中转移0.2 mol电子
⑤电子流动方向:电源负极→B→饱和食盐水→A→电源正极
⑥若实验前滴入酚酞,B极区附近溶液先变红
Ⅲ.如下图所示装置中都盛有0.1 mol/L的NaCl溶液,放置一定时间后,装置中的五块相同锌片,腐蚀速率由快到慢的正确顺序是


您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】将质量相等的铁片和铜片用导线相连浸入500mL硫酸铜溶液中构成如图1的装置:

图1
(以下均假设反应过程中溶液体积不变)。
(1)铁片上的电极反应式为_________________ ,铜片上的电极反应式为___________________ ;
(2)铜片周围溶液会出现的现象___________________ 。
(3)若2min后测得铁片质量减少5.6g,导线中流过的电子的物质的量为_________ mol;
(4)金属的电化学腐蚀的本质是形成了原电池。如下图所示,烧杯中都盛有稀硫酸。

①图2 B中的Sn为_________ 极,Sn极附近溶液的pH_________ (填“增大”“减小”或“不变”)。
②图2 C中被腐蚀的金属是_________ 。比较A、B、C中纯铁被腐蚀的速率由快到慢的顺序是_________ 。
(5)人们应用原电池原理制作了多种电池,以满足不同的需要。燃料电池是一种高效、环境友好的供电装置,如图是电解质为稀硫酸溶液的氢氧燃料电池原理示意图,回答下列问题:

氢氧燃料电池的正极电极反应是:_________ 。电池工作一段时间后硫酸溶液的浓度_________ (填“增大”“减小”或“不变”)。

图1
(以下均假设反应过程中溶液体积不变)。
(1)铁片上的电极反应式为
(2)铜片周围溶液会出现的现象
(3)若2min后测得铁片质量减少5.6g,导线中流过的电子的物质的量为
(4)金属的电化学腐蚀的本质是形成了原电池。如下图所示,烧杯中都盛有稀硫酸。

①图2 B中的Sn为
②图2 C中被腐蚀的金属是
(5)人们应用原电池原理制作了多种电池,以满足不同的需要。燃料电池是一种高效、环境友好的供电装置,如图是电解质为稀硫酸溶液的氢氧燃料电池原理示意图,回答下列问题:

氢氧燃料电池的正极电极反应是:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】按要求书写
(1)炒菜用的铸铁锅不用时会因腐蚀而出现红褐色锈斑,这时铁锅的锈蚀主要是电化学腐蚀,请写出正极的电极反应式___________ ;
(2)书写基态铁原子的电子排布式___________ ;
(3)据文献报道,CO2可以在碱性水溶液中电解生成甲烷,生成甲烷的电极反应式是___________ ;
(4)Na2CO3溶液显碱性的原因(用离子方程式表示)___________ ;
(5)铝与氢氧化钠溶液反应的离子方程式___________ 。
(1)炒菜用的铸铁锅不用时会因腐蚀而出现红褐色锈斑,这时铁锅的锈蚀主要是电化学腐蚀,请写出正极的电极反应式
(2)书写基态铁原子的电子排布式
(3)据文献报道,CO2可以在碱性水溶液中电解生成甲烷,生成甲烷的电极反应式是
(4)Na2CO3溶液显碱性的原因(用离子方程式表示)
(5)铝与氢氧化钠溶液反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】用氧化铁包裹的纳米铁粉(用Fe@Fe2O3表示)能有效还原水溶液中的Cr(Ⅵ)。Fe@Fe2O3还原近中性废水中Cr(Ⅵ)的可能反应机理如图所示。Fe@Fe2O3中Fe还原CrO 的过程可描述为
的过程可描述为___________
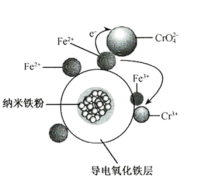 。
。
 的过程可描述为
的过程可描述为 。
。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】按要求填空
(1)NH4Cl溶液呈酸性,用离子方程式表示其原因___________________________________ ;
(2)25℃时1g甲烷完全燃烧生成二氧化碳气体和液态水,放出56千焦的热量,写出该反应的热化学方程式:_____________________________ ;
(3)铁在空气中发生吸氧腐蚀时的正极反应方程式:_________________________________
(4)硫酸铜溶液通电时发生的化学反应方程式:_______________________________
(1)NH4Cl溶液呈酸性,用离子方程式表示其原因
(2)25℃时1g甲烷完全燃烧生成二氧化碳气体和液态水,放出56千焦的热量,写出该反应的热化学方程式:
(3)铁在空气中发生吸氧腐蚀时的正极反应方程式:
(4)硫酸铜溶液通电时发生的化学反应方程式:
您最近一年使用:0次
【推荐1】对金属制品进行抗腐蚀处理,可延长其使用寿命。
(1)镀铜可防止铁制品腐蚀,电镀时用铜而不用石墨作阳极的原因是___________________ 。在此过程中,两个电极上质量的变化值:阴极________ 阳极(填“>”“<”或“=”)。
(2)利用如图所示的装置,可以模拟铁的电化学防护。若X为碳棒,为减缓铁的腐蚀,开关K应置于________ (填“M”或“N”)处。若X为锌,开关K置于M处,该电化学防护法称为________ 。
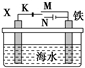
(1)镀铜可防止铁制品腐蚀,电镀时用铜而不用石墨作阳极的原因是
(2)利用如图所示的装置,可以模拟铁的电化学防护。若X为碳棒,为减缓铁的腐蚀,开关K应置于

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】回答下列问题:
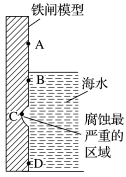
(1)如图是实验室研究海水对铁闸不同部位腐蚀情况的剖面示意图。
①该电化学腐蚀称为______________ 。
②图中A、B、C、D四个区域,生成铁锈最多的是________ (填字母)。
③以锌为负极,采用牺牲阳极的阴极保护法防止铁闸的腐蚀,图中锌块的固定位置最好应在________ 处(填字母)。
(2)石墨可用于自然水体中铜件的电化学防腐,完成如图防腐示意图,并作相应标注:

________
(3)下图所示的各容器中均盛有海水,铁在其中被腐蚀时由快到慢的顺序是__________________ 。

(4)如图,将铁棒和石墨棒插入盛有饱和NaCl溶液的U形管中,下列分析正确的是________ (填字母)。

A.K1闭合,铁棒上发生的反应为2H++2e-===H2↑
B.K1闭合,石墨棒周围溶液pH逐渐升高
C.K2闭合,铁棒不会被腐蚀,属于牺牲阳极的阴极保护法
D.K2闭合,电路中通过0.002NA个电子时,两极共产生0.001 mol气体

(1)如图是实验室研究海水对铁闸不同部位腐蚀情况的剖面示意图。
①该电化学腐蚀称为
②图中A、B、C、D四个区域,生成铁锈最多的是
③以锌为负极,采用牺牲阳极的阴极保护法防止铁闸的腐蚀,图中锌块的固定位置最好应在
(2)石墨可用于自然水体中铜件的电化学防腐,完成如图防腐示意图,并作相应标注:

(3)下图所示的各容器中均盛有海水,铁在其中被腐蚀时由快到慢的顺序是

(4)如图,将铁棒和石墨棒插入盛有饱和NaCl溶液的U形管中,下列分析正确的是

A.K1闭合,铁棒上发生的反应为2H++2e-===H2↑
B.K1闭合,石墨棒周围溶液pH逐渐升高
C.K2闭合,铁棒不会被腐蚀,属于牺牲阳极的阴极保护法
D.K2闭合,电路中通过0.002NA个电子时,两极共产生0.001 mol气体
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】2021年年中,美国国会发表的一篇《中国海军现代化》的调查报告提及,目前我国国产新型航母的技术水平和美国最先进的“福特”级航空母舰为同一级别的对手。
已知:正常海水呈弱碱性。
(1)若经过长时间的海上作业,部分钢铁制成的舰体有可能被腐蚀。舰体发生电化学腐蚀时,负极的电极反应式为____ 。
(2)为了保护航母,工作人员对舰体进行了处理。
①工作人员贴在舰体上的材料块可以是____ (填字母序号)。
A.铝锌合金 B.石墨 C.铅 D.铜
②采用“牺牲阳极的阴极保护法”后,水下舰体上正极的电极反应式为____ 。
(3)国家文物局在辽宁开展水下考古,搜寻、发现并确认了甲午海战北洋水师沉舰——经远舰。考古队员将舰船上的部分文物打捞出水后,采取脱盐、干燥等措施防止文物继续被腐蚀。从电化学原理的角度分析“脱盐、干燥”的防腐原理:____ 。
已知:正常海水呈弱碱性。
(1)若经过长时间的海上作业,部分钢铁制成的舰体有可能被腐蚀。舰体发生电化学腐蚀时,负极的电极反应式为
(2)为了保护航母,工作人员对舰体进行了处理。
①工作人员贴在舰体上的材料块可以是
A.铝锌合金 B.石墨 C.铅 D.铜
②采用“牺牲阳极的阴极保护法”后,水下舰体上正极的电极反应式为
(3)国家文物局在辽宁开展水下考古,搜寻、发现并确认了甲午海战北洋水师沉舰——经远舰。考古队员将舰船上的部分文物打捞出水后,采取脱盐、干燥等措施防止文物继续被腐蚀。从电化学原理的角度分析“脱盐、干燥”的防腐原理:
您最近一年使用:0次



