按要求书写
(1)炒菜用的铸铁锅不用时会因腐蚀而出现红褐色锈斑,这时铁锅的锈蚀主要是电化学腐蚀,请写出正极的电极反应式___________ ;
(2)书写基态铁原子的电子排布式___________ ;
(3)据文献报道,CO2可以在碱性水溶液中电解生成甲烷,生成甲烷的电极反应式是___________ ;
(4)Na2CO3溶液显碱性的原因(用离子方程式表示)___________ ;
(5)铝与氢氧化钠溶液反应的离子方程式___________ 。
(1)炒菜用的铸铁锅不用时会因腐蚀而出现红褐色锈斑,这时铁锅的锈蚀主要是电化学腐蚀,请写出正极的电极反应式
(2)书写基态铁原子的电子排布式
(3)据文献报道,CO2可以在碱性水溶液中电解生成甲烷,生成甲烷的电极反应式是
(4)Na2CO3溶液显碱性的原因(用离子方程式表示)
(5)铝与氢氧化钠溶液反应的离子方程式
更新时间:2022-03-17 08:12:16
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】现有室温下浓度均为1×10-3mol/L的几种溶液①盐酸、②硫酸、③醋酸、④氯化铵、⑤氨水、⑥NaOH溶液,回答下列问题:
(1)pH均等于3的溶液①、②、③、④中水电离产生的c(H+)的比值是________
(2)将③、⑥混合后,若溶液呈中性,则消耗两溶液的体积为③___ ⑥(填“>”、“<”或“=”),溶液中的离子浓度由大到小的顺序为_________________________________________
(3)将等体积的①、⑤混合,则溶液的pH____ 7(填“>”、“<”或“=”),用离子方程式说明其原因__________________________________________________
(4)向相同体积的①、②、③溶液中分别加入相同的且足量的锌粒,反应的初始速率由快到慢的顺序为____________ ,最终产生H2总量的关系为_________________
(5)向相同体积的①、③溶液中分别加入相同浓度、相同体积的CH3COONa溶液,充分混合后,混合液的pH大小关系为①______ ③(填“>”、“<”或“=”)
(6)若将等体积的⑤、⑥溶液加热至相同温度后,溶液的PH⑤____ ⑥(填“>”、“<”或“=”)。
(1)pH均等于3的溶液①、②、③、④中水电离产生的c(H+)的比值是
(2)将③、⑥混合后,若溶液呈中性,则消耗两溶液的体积为③
(3)将等体积的①、⑤混合,则溶液的pH
(4)向相同体积的①、②、③溶液中分别加入相同的且足量的锌粒,反应的初始速率由快到慢的顺序为
(5)向相同体积的①、③溶液中分别加入相同浓度、相同体积的CH3COONa溶液,充分混合后,混合液的pH大小关系为①
(6)若将等体积的⑤、⑥溶液加热至相同温度后,溶液的PH⑤
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】取0.1 mol/L HA溶液与0.1 mol/L NaOH溶液等体积混合(混合后溶液体积的变化不计),测得混合溶液的pH=8。试回答以下问题:
(1)混合溶液的pH=8的原因是_________________ (用离子方程式表示)。
(2)混合溶液中由水电离出的c(H+)________ 0.1 mol/L NaOH溶液中由水电离出的c(H+) (填“>”、“<”或“=”)。
(3)求出混合液中下列算式的精确计算结果(填具体数字):
c(Na+)-c(A-)=________ mol/L;c(OH-)-c(HA)=________ mol/L。
(4)已知NH4A溶液为中性,又知将HA溶液加到Na2CO3溶液中有气体放出,试推断(NH4)2CO3溶液的pH________ 7(填“>”、“<”或“=”)。
(1)混合溶液的pH=8的原因是
(2)混合溶液中由水电离出的c(H+)
(3)求出混合液中下列算式的精确计算结果(填具体数字):
c(Na+)-c(A-)=
(4)已知NH4A溶液为中性,又知将HA溶液加到Na2CO3溶液中有气体放出,试推断(NH4)2CO3溶液的pH
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】回答下列问题
(1)为了研究化学反应A+B=C+D的能量变化情况,某同学设计了如图所示装置。当向盛有A的试管中滴加试剂B时,看到U形管中甲处液面下降乙处液面上升。试回答下列问题:
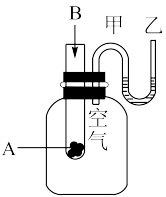
①该反应为___________ 反应(填“放热”或“吸热”)。
②A和B的总能量比C和D的总能量___________ (填“高”或“低”)。
(2)完成下列反应的热化学方程式。
已知:
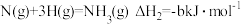
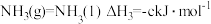
写出 和
和 反应生成液氨的热化学方程式
反应生成液氨的热化学方程式___________ 。
(3)写出 在水溶液中的电离方程式
在水溶液中的电离方程式___________ 。
(4)写出 的水解方程式
的水解方程式___________ 。
(1)为了研究化学反应A+B=C+D的能量变化情况,某同学设计了如图所示装置。当向盛有A的试管中滴加试剂B时,看到U形管中甲处液面下降乙处液面上升。试回答下列问题:

①该反应为
②A和B的总能量比C和D的总能量
(2)完成下列反应的热化学方程式。
已知:

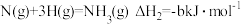
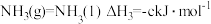
写出
 和
和 反应生成液氨的热化学方程式
反应生成液氨的热化学方程式(3)写出
 在水溶液中的电离方程式
在水溶液中的电离方程式(4)写出
 的水解方程式
的水解方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】I.装置如图所示,C、D、E、F、X、Y都是惰性电极,甲、乙中溶液的体积和浓度都相同(假设通电前后溶液体积不变),A、B为外接直流电源的两极。将直流电源接通后,F极附近呈红色。请回答:

(1)B极是电源的___________ 极,C极的电极反应式为___________ ,一段时间后丁中X极附近的颜色逐渐___________ (填“变深”或“变浅”)。(已知氢氧化铁胶粒带正电荷)
(2)若甲、乙装置中的C、D、E、F电极均只有一种单质生成,对应单质的物质的量之比为___________ 。
(3)现用丙装置给铜件镀银,则H应该是___________ (填“铜”或“银”)。常温下,当乙中溶液的 时(此时乙溶液体积为500 mL),丙中镀件上析出银的质量为
时(此时乙溶液体积为500 mL),丙中镀件上析出银的质量为___________ g。
(4)甲装置中发生反应的化学方程式为___________ ;乙装置中发生反应的离子方程式为___________ 。
II.通过NOx传感器可监测NOx的含量,工作原理示意图如下:

(5)Pt电极上发生的是___________ 反应(填“氧化”或“还原”)。
(6)写出NiO电极的电极反应式:___________ 。

(1)B极是电源的
(2)若甲、乙装置中的C、D、E、F电极均只有一种单质生成,对应单质的物质的量之比为
(3)现用丙装置给铜件镀银,则H应该是
 时(此时乙溶液体积为500 mL),丙中镀件上析出银的质量为
时(此时乙溶液体积为500 mL),丙中镀件上析出银的质量为(4)甲装置中发生反应的化学方程式为
II.通过NOx传感器可监测NOx的含量,工作原理示意图如下:

(5)Pt电极上发生的是
(6)写出NiO电极的电极反应式:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】中国科学院长春应用化学研究所在甲醇(CH3OH)燃料电池技术方面获得新突破,组装出了自呼吸电池及主动式电池。
Ⅰ.甲醇燃料电池的工作原理如下图所示。
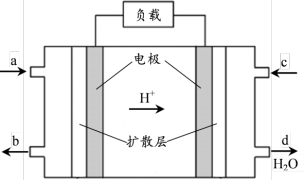
(1)甲醇燃料电池的总反应方程式为___________ 。
(2)左边电极为该电池的___________ (填“正极”或“负极”),该极的电极反应为___________ 。
(3)当6.4 g甲醇完全反应生成CO2时,消耗标准状况下的空气体积约为___________ L。
Ⅱ.某学习小组用石墨作电极电解饱和食盐水进行研究。
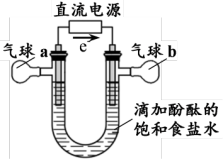
(4)电解一段时间后,U形管___________ (填“左”或“右”)边的溶液变红,该处的电极反应为___________ 。
(5)若要使电解初期的溶液复原,可加入的物质是___________ (填名称)。
Ⅰ.甲醇燃料电池的工作原理如下图所示。

(1)甲醇燃料电池的总反应方程式为
(2)左边电极为该电池的
(3)当6.4 g甲醇完全反应生成CO2时,消耗标准状况下的空气体积约为
Ⅱ.某学习小组用石墨作电极电解饱和食盐水进行研究。

(4)电解一段时间后,U形管
(5)若要使电解初期的溶液复原,可加入的物质是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
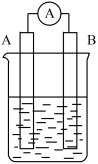
【推荐3】原电池装置如图所示,回答下列问题。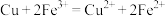 设计原电池,电极A为石墨、则电极B为电池的
设计原电池,电极A为石墨、则电极B为电池的________ 极,发生的电极反应式为:________________ ,电极A上发生的电极反应为________ (填“氧化”或“还原”)反应。
(2)若A、B均为铂片,分别从A、B两极通入 和
和 。当烧杯内的液体为稀硫酸溶液,A为
。当烧杯内的液体为稀硫酸溶液,A为________ (填正极或负极)写出B电极的电极反应式:________________ ,溶液中的 向
向________ (填“A”或“B”)极移动;当烧杯内的液体为氢氧化钾溶液,此时A电极的电极反应式:________ ,当消耗0.2mo1氧气时,电路中通过电子数为________ 。
(3)若A为 ,B为
,B为 ,烧杯内的液体为浓硫酸,电池反应为:
,烧杯内的液体为浓硫酸,电池反应为: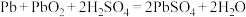 。写出B电极的电极反应式:
。写出B电极的电极反应式:________________ 。
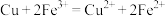 设计原电池,电极A为石墨、则电极B为电池的
设计原电池,电极A为石墨、则电极B为电池的(2)若A、B均为铂片,分别从A、B两极通入
 和
和 。当烧杯内的液体为稀硫酸溶液,A为
。当烧杯内的液体为稀硫酸溶液,A为 向
向(3)若A为
 ,B为
,B为 ,烧杯内的液体为浓硫酸,电池反应为:
,烧杯内的液体为浓硫酸,电池反应为: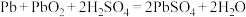 。写出B电极的电极反应式:
。写出B电极的电极反应式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】金属的腐蚀
(1)金属腐蚀的本质
金属原子失去电子变为金属阳离子,金属发生_______________ 反应.
(2)金属腐蚀的类型
①化学腐蚀与电化学腐蚀
②析氢腐蚀与吸氧腐蚀(以钢铁的腐蚀为例)
(1)金属腐蚀的本质
金属原子失去电子变为金属阳离子,金属发生
(2)金属腐蚀的类型
①化学腐蚀与电化学腐蚀
| 类型 | 化学腐蚀 | 电化学腐蚀 |
| 条件 | 金属与其表面接触到的物质直接发生化学反应 | 不纯的金属接触到电解质溶液发生原电池反应 |
| 本质 |  |  |
| 现象 | 金属被腐蚀 | 较活泼金属被腐蚀 |
| 区别 | 无电流产生 | 有微弱电流产生 |
| 联系 | 电化学腐蚀比化学腐蚀普遍得多,腐蚀速率更快,危害也更严重 | |
②析氢腐蚀与吸氧腐蚀(以钢铁的腐蚀为例)
| 类型 | 析氢腐蚀 | 吸氧腐蚀 | |
| 条件 | 水膜酸性较强 | 水膜酸性很弱或呈中性 | |
| 电 | 负极 |
| |
| 正极 | |||
| 总反应式 | |||
| 联系 | 吸氧腐蚀更普遍 | ||
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】I.炒过菜的铁锅未及时洗净,不久便会因腐蚀而出现红褐色锈斑。请回答:
(1)铁锅的锈蚀是________ 腐蚀(填“析氢”或“吸氧”)。
(2)写出铁锅腐蚀正极的电极反应式:_______________
II.在如图用石墨作电极的电解池中,放入500mL饱和NaCl溶液并滴入酚酞,进行电解,观察到B电极附近溶液先变红。请回答下列问题:
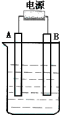
(1)A接的是电源的_______ 极,B是该装置______ 。
(2)写出电解时总反应的离子方程式:____________________________ 。
(3)电解后溶液的pH______ ;(填 增大、减小或不变)要使电解后溶液恢复到电解前的状态,则需加入_______ 。
(4)若电源为碱性锌锰干电池,负极为______ 正极为______ 电解质溶液是_______
(1)铁锅的锈蚀是
(2)写出铁锅腐蚀正极的电极反应式:
II.在如图用石墨作电极的电解池中,放入500mL饱和NaCl溶液并滴入酚酞,进行电解,观察到B电极附近溶液先变红。请回答下列问题:

(1)A接的是电源的
(2)写出电解时总反应的离子方程式:
(3)电解后溶液的pH
(4)若电源为碱性锌锰干电池,负极为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】电子排布式
用数字在能级符号右上角标明该能级上排布的电子数,这就是电子排布式。写出下列基态原子的电子排布式:
(1)16S:_______ ;
(2)20Ca:_______ ;
(3)26Fe:_______ ;
(4)29Cu:_______ 。
用数字在能级符号右上角标明该能级上排布的电子数,这就是电子排布式。写出下列基态原子的电子排布式:
(1)16S:
(2)20Ca:
(3)26Fe:
(4)29Cu:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】回答下列问题:
(1)1 mol CO2中含有的σ键数目为________ ,π键数目为________ 。
(2)已知CO和CN-与N2结构相似,CO分子内σ键与π键个数之比为________ 。CH2=CHCN分子中σ键与π键数目之比为________ 。
(3)肼(N2H4)分子可视为NH3分子中的—个氢原子被-NH2(氨基)取代形成的另一种氮的氢化物。肼可用作火箭燃料,燃烧时发生的反应:N2O4(l)+2N2H4(l)===3N2(g)+4H2O(g) ΔH=-1 038.7 kJ·mol-1若该反应中有4 mol N—H键断裂,则形成的π键有________ mol。
(4)Co 基态原子核外电子排布式为____________ ;
基态Ge原子的核外电子排布式为____________ ;
Zn2+的价电子轨道表示式为_______________ ;
Co3+核外电子未成对电子数为__________________ 。
(5)CH4、NH3、H2O、HF分子中共价键的极性由强到弱的顺序是_______________________ 。
(1)1 mol CO2中含有的σ键数目为
(2)已知CO和CN-与N2结构相似,CO分子内σ键与π键个数之比为
(3)肼(N2H4)分子可视为NH3分子中的—个氢原子被-NH2(氨基)取代形成的另一种氮的氢化物。肼可用作火箭燃料,燃烧时发生的反应:N2O4(l)+2N2H4(l)===3N2(g)+4H2O(g) ΔH=-1 038.7 kJ·mol-1若该反应中有4 mol N—H键断裂,则形成的π键有
(4)Co 基态原子核外电子排布式为
基态Ge原子的核外电子排布式为
Zn2+的价电子轨道表示式为
Co3+核外电子未成对电子数为
(5)CH4、NH3、H2O、HF分子中共价键的极性由强到弱的顺序是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】已知A、B、C、D四种分子所含原子的数目依次为1、3、6、2,且都含有18个电子,B、C是由两种元素的原子组成,且分子中两种原子的个数比均为1∶2。D物质能刻蚀玻璃。
(1)A的分子式是________ ,写出A原子的价层电子排布式________ 。
(2)B分子的中心原子的杂化类型是________ ,分子空间构型是________ ,该分子属于________ 分子(填“极性”或“非极性”)。
(3)C的化学式是________ ,分子中含有的化学键类型是________ 。
(4)D物质的沸点比HCl的沸点高,其主要原因是___________________ 。
(1)A的分子式是
(2)B分子的中心原子的杂化类型是
(3)C的化学式是
(4)D物质的沸点比HCl的沸点高,其主要原因是
您最近一年使用:0次




