2021年年中,美国国会发表的一篇《中国海军现代化》的调查报告提及,目前我国国产新型航母的技术水平和美国最先进的“福特”级航空母舰为同一级别的对手。
已知:正常海水呈弱碱性。
(1)若经过长时间的海上作业,部分钢铁制成的舰体有可能被腐蚀。舰体发生电化学腐蚀时,负极的电极反应式为____ 。
(2)为了保护航母,工作人员对舰体进行了处理。
①工作人员贴在舰体上的材料块可以是____ (填字母序号)。
A.铝锌合金 B.石墨 C.铅 D.铜
②采用“牺牲阳极的阴极保护法”后,水下舰体上正极的电极反应式为____ 。
(3)国家文物局在辽宁开展水下考古,搜寻、发现并确认了甲午海战北洋水师沉舰——经远舰。考古队员将舰船上的部分文物打捞出水后,采取脱盐、干燥等措施防止文物继续被腐蚀。从电化学原理的角度分析“脱盐、干燥”的防腐原理:____ 。
已知:正常海水呈弱碱性。
(1)若经过长时间的海上作业,部分钢铁制成的舰体有可能被腐蚀。舰体发生电化学腐蚀时,负极的电极反应式为
(2)为了保护航母,工作人员对舰体进行了处理。
①工作人员贴在舰体上的材料块可以是
A.铝锌合金 B.石墨 C.铅 D.铜
②采用“牺牲阳极的阴极保护法”后,水下舰体上正极的电极反应式为
(3)国家文物局在辽宁开展水下考古,搜寻、发现并确认了甲午海战北洋水师沉舰——经远舰。考古队员将舰船上的部分文物打捞出水后,采取脱盐、干燥等措施防止文物继续被腐蚀。从电化学原理的角度分析“脱盐、干燥”的防腐原理:
更新时间:2022-08-28 10:02:21
|
相似题推荐
【推荐1】能源是现代文明的原动力,随着常规能源的有限性以及环境问题的日益突出,以环保和可再生为特质的新能源越来越得到各国的重视。新能源包括风能、氢能、沼气、酒精、甲醇等,新能源的使用与研究在一定程度上助力中国实现“碳达峰、碳中和”。通过化学方法可以使能量按人们所期望的形式转化,从而开辟新能源和提高能源的利用率。
(1)二氧化碳的资源化利用是目前研究的热点问题之一,西北工业大学团队研究锂-二氧化碳二次电池,取得了重大科研成果。该电池放电的总反应为3CO2+4Li=2Li2CO3+C。下列说法正确的是_______ 。
(2)如图所示为CH4燃料电池的装置(A、B为多孔碳棒):______ (填A或B)处电极入口通甲烷,其电极反应式为:_______ ;当消耗甲烷的体积为11.2L(标准状况下)时,消耗KOH的质量为_______ g。
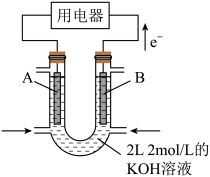
(3)用上述CH4燃料电池连接成如图装置。
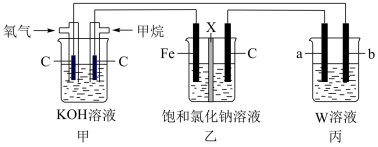
乙池中X为阳离子交换膜,石墨电极(C)作_______ 极,写出乙池总反应的离子方程式_______ 。
(4)若将乙装置中两电极用导线直接相连,则铁发生_______ 腐蚀,写出碳棒的电极反应式:______ 。若将乙装置中两电极连接电源的正负两极,铁连接电源的_______ 极(填“正”或“负”)时,可防止铁腐蚀。
(5)若丙中要实现铁上镀银,b电极材料为_______ 。
(1)二氧化碳的资源化利用是目前研究的热点问题之一,西北工业大学团队研究锂-二氧化碳二次电池,取得了重大科研成果。该电池放电的总反应为3CO2+4Li=2Li2CO3+C。下列说法正确的是
| A.该电池的电解液可以是稀硫酸 |
| B.放电时,若消耗1.5molCO2时,转移2mol电子 |
| C.放电时,电子从锂电极流出,通过电解液流回锂电极,构成闭合回路 |
| D.放电时,锂电极作正极 |

(3)用上述CH4燃料电池连接成如图装置。

乙池中X为阳离子交换膜,石墨电极(C)作
(4)若将乙装置中两电极用导线直接相连,则铁发生
(5)若丙中要实现铁上镀银,b电极材料为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】钢铁工业是国家工业的基础。请回答钢铁腐蚀、防护过程中的有关问题:
(1)生产中可用盐酸来除铁锈。现将一生锈的铁片放入盐酸中,当铁锈被除尽后,溶液中发生的属于化合反应的化学方程式是______________ 。
(2)下列装置可防止铁棒被腐蚀的是___________ 。
A. B.
B.  C.
C.  D.
D. 
(3)在实际生产中,可在铁件的表面镀铜防止铁被腐蚀,装置示意图如图所示。

①A电极对应的金属是______ (填元素名称),B电极的电极反应式是________ 。
②镀层破损后,镀铜铁比镀锌铁更易被腐蚀,原因是_________ 。
(1)生产中可用盐酸来除铁锈。现将一生锈的铁片放入盐酸中,当铁锈被除尽后,溶液中发生的属于化合反应的化学方程式是
(2)下列装置可防止铁棒被腐蚀的是
A.
 B.
B.  C.
C.  D.
D. 
(3)在实际生产中,可在铁件的表面镀铜防止铁被腐蚀,装置示意图如图所示。

①A电极对应的金属是
②镀层破损后,镀铜铁比镀锌铁更易被腐蚀,原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】钢铁很容易生锈腐蚀,每年因腐蚀而损失的钢材占世界钢铁年产量的四分之一。因此,该小组同学又进行了钢铁腐蚀探究,希望能找到防止钢铁腐蚀的好办法。如图,U形管内为红墨水,a、b试管内分别盛有氯化铵溶液(显酸性)和食盐水,各加入生铁块,放置一段时间均被腐蚀。红墨水柱两边液面变为:左低、右高。
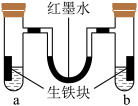
(1)请猜测a试管中铁发生的是________ (填“析氢”或“吸氧”)腐蚀。
(2)b管中生铁中碳上发生的电极反应式________________________ 。

(1)请猜测a试管中铁发生的是
(2)b管中生铁中碳上发生的电极反应式
您最近一年使用:0次
【推荐1】I.炒过菜的铁锅未及时洗净,不久便会因腐蚀而出现红褐色锈斑。请回答:
(1) 铁锅的锈蚀是___________ 腐蚀(填“析氢”或“吸氧”);
(2) 写出铁锅腐蚀正极的电极反应式:___________ ;
(3) 关于铁的腐蚀随处可见,例如海水中船体的外壳易生锈,为此可在船体外壳设备上装上锌块以减缓金属的腐蚀,则该保护措施称___________ 法。
II.在如下图用石墨作电极的电解池中,放入500mL含一种溶质的某蓝色溶液进行电解,观察到A电极表面有红色的固态物质生成,B电极有无色无味气体生成;当溶液中的原有溶质完全电解后,停止电解,取出A电极,洗涤、干燥、称量、电极增重1.6g。请回答下列问题:
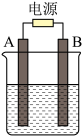
(1) A接的是电源的___________ 极;
(2) 写出电解时反应的总离子方程式___________ ;
(3) 电解后溶液的pH为___________ ;要使电解后溶液恢复到电解前的状态,则需加入___________ ,其质量为___________ (假设电解前后溶液的体积不变)。
(1) 铁锅的锈蚀是
(2) 写出铁锅腐蚀正极的电极反应式:
(3) 关于铁的腐蚀随处可见,例如海水中船体的外壳易生锈,为此可在船体外壳设备上装上锌块以减缓金属的腐蚀,则该保护措施称
II.在如下图用石墨作电极的电解池中,放入500mL含一种溶质的某蓝色溶液进行电解,观察到A电极表面有红色的固态物质生成,B电极有无色无味气体生成;当溶液中的原有溶质完全电解后,停止电解,取出A电极,洗涤、干燥、称量、电极增重1.6g。请回答下列问题:

(1) A接的是电源的
(2) 写出电解时反应的总离子方程式
(3) 电解后溶液的pH为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】A、B、C三个烧杯中分别盛有相同物质的量浓度的稀硫酸。
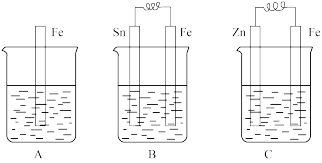
(1)A中反应的离子方程式为_________________________________ 。
(2)B中Fe极为_______ 极,电极反应式为_______________________ 。C中Fe极为_______ 极,电极反应式为__________________________ ,电子从_______ 极流出(填“Zn”或“Fe”)。
(3)比较A、B、C中铁被腐蚀的速率,由快到慢的顺序是___________________ 。

(1)A中反应的离子方程式为
(2)B中Fe极为
(3)比较A、B、C中铁被腐蚀的速率,由快到慢的顺序是
您最近一年使用:0次



