能源是现代文明的原动力,随着常规能源的有限性以及环境问题的日益突出,以环保和可再生为特质的新能源越来越得到各国的重视。新能源包括风能、氢能、沼气、酒精、甲醇等,新能源的使用与研究在一定程度上助力中国实现“碳达峰、碳中和”。通过化学方法可以使能量按人们所期望的形式转化,从而开辟新能源和提高能源的利用率。
(1)二氧化碳的资源化利用是目前研究的热点问题之一,西北工业大学团队研究锂-二氧化碳二次电池,取得了重大科研成果。该电池放电的总反应为3CO2+4Li=2Li2CO3+C。下列说法正确的是_______ 。
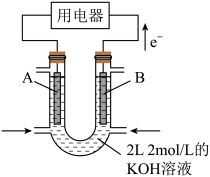
(2)如图所示为CH4燃料电池的装置(A、B为多孔碳棒):______ (填A或B)处电极入口通甲烷,其电极反应式为:_______ ;当消耗甲烷的体积为11.2L(标准状况下)时,消耗KOH的质量为_______ g。
(3)用上述CH4燃料电池连接成如图装置。
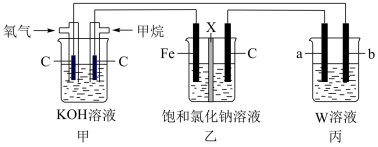
乙池中X为阳离子交换膜,石墨电极(C)作_______ 极,写出乙池总反应的离子方程式_______ 。
(4)若将乙装置中两电极用导线直接相连,则铁发生_______ 腐蚀,写出碳棒的电极反应式:______ 。若将乙装置中两电极连接电源的正负两极,铁连接电源的_______ 极(填“正”或“负”)时,可防止铁腐蚀。
(5)若丙中要实现铁上镀银,b电极材料为_______ 。
(1)二氧化碳的资源化利用是目前研究的热点问题之一,西北工业大学团队研究锂-二氧化碳二次电池,取得了重大科研成果。该电池放电的总反应为3CO2+4Li=2Li2CO3+C。下列说法正确的是
| A.该电池的电解液可以是稀硫酸 |
| B.放电时,若消耗1.5molCO2时,转移2mol电子 |
| C.放电时,电子从锂电极流出,通过电解液流回锂电极,构成闭合回路 |
| D.放电时,锂电极作正极 |

(3)用上述CH4燃料电池连接成如图装置。

乙池中X为阳离子交换膜,石墨电极(C)作
(4)若将乙装置中两电极用导线直接相连,则铁发生
(5)若丙中要实现铁上镀银,b电极材料为
更新时间:2023-04-27 16:22:51
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】I.为了探究化学反应中的能量变化,某同学设计了如图两个实验。

(1)相同条件下,实验发现图I中温度计的示数高于图II的示数,其原因是___________ 。
(2)图II实验结束后,实验报告上记录信息如下:
①实验报告中记录信息合理的是___________ (填序号)。
②若有1mol电子流过导线,则溶液中有___________ molH+移向___________ (填“锌极”或“铜极”),理论上溶解Zn的质量为___________ g。
③将稀H2SO4换成CuSO4溶液,请写出该电池的正极电极反应式___________ 。
II.碳中和作为一种新型环保理念可推动全社会绿色发展。我国争取2060年前实现碳中和。复合催化是工业合成甲醇(CH3OH)的重要反应,在2L密闭容器中,充入10molCO2和40molH2,在催化剂、200℃的条件下发生反应。部分反应物和产物随时间变化如图所示:

已知:平衡转化率= ×100%。
×100%。
(3)请写出该复合催化反应的化学方程式为___________ 。
(4)2min时,正、逆反应速率的大小关系为v逆___________ v正(填“>”“<”或“=”)。
(5)当反应达到平衡时,H2的转化率是___________ 。

(1)相同条件下,实验发现图I中温度计的示数高于图II的示数,其原因是
(2)图II实验结束后,实验报告上记录信息如下:
| a.Cu、Zn电极 均有气泡产生 | b.Cu电极 发生氧化反应 | c.电流计指针偏转 | d.电流由Zn经导线流向Cu |
②若有1mol电子流过导线,则溶液中有
③将稀H2SO4换成CuSO4溶液,请写出该电池的正极电极反应式
II.碳中和作为一种新型环保理念可推动全社会绿色发展。我国争取2060年前实现碳中和。复合催化是工业合成甲醇(CH3OH)的重要反应,在2L密闭容器中,充入10molCO2和40molH2,在催化剂、200℃的条件下发生反应。部分反应物和产物随时间变化如图所示:

已知:平衡转化率=
 ×100%。
×100%。(3)请写出该复合催化反应的化学方程式为
(4)2min时,正、逆反应速率的大小关系为v逆
(5)当反应达到平衡时,H2的转化率是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】减排是各个国家都在努力为之的事, 和
和 的处理是许多科学家都在着力研究的重点。有学者想以如图所示装置利用原电池原理将
的处理是许多科学家都在着力研究的重点。有学者想以如图所示装置利用原电池原理将 、
、 转化为重要的化工原料。
转化为重要的化工原料。

(1)若A为 ,B为
,B为 ,C为
,C为 ,电池总反应方程式为
,电池总反应方程式为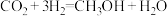 ,则正极的电极反应式为
,则正极的电极反应式为________ 。
(2)若A为 ,B为
,B为 ,C为
,C为 ,则负极的电极反应式为
,则负极的电极反应式为_________ ,电池的总反应方程式为___________ 。
 和
和 的处理是许多科学家都在着力研究的重点。有学者想以如图所示装置利用原电池原理将
的处理是许多科学家都在着力研究的重点。有学者想以如图所示装置利用原电池原理将 、
、 转化为重要的化工原料。
转化为重要的化工原料。
(1)若A为
 ,B为
,B为 ,C为
,C为 ,电池总反应方程式为
,电池总反应方程式为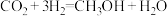 ,则正极的电极反应式为
,则正极的电极反应式为(2)若A为
 ,B为
,B为 ,C为
,C为 ,则负极的电极反应式为
,则负极的电极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】(1)若2.6g乙炔(C2H2气态)完全燃烧生成液态水和CO2时放热130kJ。则此反应的热化学方程式为:______________________________________ 。
(2)图中铜板上铁铆钉处容易生锈,被腐蚀的金属是_______ ,负极的电极反应式为____________

(3)氢气被公认为21世纪替代矿物燃料的理想能源,已知破坏1mol氢气中的化学键消耗的能量为Q1kJ,破坏1mol氧气中的化学键消耗的能量为Q2kJ,形成1molH-O键释放的能量为Q3kJ。则1mol氢气燃烧放出的热量是___________________ kJ。
(4)氢氧燃料电池是符合绿色化学理念的新型发电装置。下图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定。

请回答:
①氢氧燃料电池的能量转化主要形式是_______________________ ,在导线中电子流动方向为__________________ (用a、b表示)。
②负极反应式为______________________________________ 。
(2)图中铜板上铁铆钉处容易生锈,被腐蚀的金属是

(3)氢气被公认为21世纪替代矿物燃料的理想能源,已知破坏1mol氢气中的化学键消耗的能量为Q1kJ,破坏1mol氧气中的化学键消耗的能量为Q2kJ,形成1molH-O键释放的能量为Q3kJ。则1mol氢气燃烧放出的热量是
(4)氢氧燃料电池是符合绿色化学理念的新型发电装置。下图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定。

请回答:
①氢氧燃料电池的能量转化主要形式是
②负极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】我国利用氯碱厂生产的 作燃料,将氢燃料电站应用于氯碱工业,其示意图如下。
作燃料,将氢燃料电站应用于氯碱工业,其示意图如下。
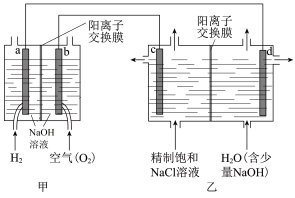
(1) 极为
极为_____ (填“正”或“负”)极,其电极反应式是______ 。
(2)乙装置中电解饱和 溶液的化学方程式为
溶液的化学方程式为______ 。
(3)结合化学用语解释 极区产生
极区产生 的原因:
的原因:________ 。
(4)电解时用盐酸控制阳极区溶液的 在
在 。用化学平衡移动原理解释盐酸的作用:
。用化学平衡移动原理解释盐酸的作用:______ 。
(5)下列说法正确的是_______。
 作燃料,将氢燃料电站应用于氯碱工业,其示意图如下。
作燃料,将氢燃料电站应用于氯碱工业,其示意图如下。
(1)
 极为
极为(2)乙装置中电解饱和
 溶液的化学方程式为
溶液的化学方程式为(3)结合化学用语解释
 极区产生
极区产生 的原因:
的原因:(4)电解时用盐酸控制阳极区溶液的
 在
在 。用化学平衡移动原理解释盐酸的作用:
。用化学平衡移动原理解释盐酸的作用:(5)下列说法正确的是_______。
| A.甲装置可以实现化学能向电能转化 |
B.甲装置中 透过阳离子交换膜向 透过阳离子交换膜向 极移动 极移动 |
C.乙装置中 极一侧流出的是淡盐水 极一侧流出的是淡盐水 |
D.理论上,每消耗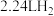 (标况下),可制得 (标况下),可制得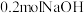 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】电化学在生活、生产、科学技术等各个领域的发展中扮演着越来越重要的角色。 燃料电池的工作示意图如图,乙池中的电解质溶液为
燃料电池的工作示意图如图,乙池中的电解质溶液为 物质的量浓度均为
物质的量浓度均为 的
的 的混合溶液,一段时间后,观察到乙池中铁片溶解。
的混合溶液,一段时间后,观察到乙池中铁片溶解。

(1)乙池中的能量转化形式为_______ 。
(2)气体Y为_______ ,闭合开关K,电极a上发生的电极反应为_______ ,溶液中 的移动方向为
的移动方向为_______ (填“移向电极a”或“移向电极b”)。
(3)乙池中铁电极发生的电极反应为_______ ,一段时间后,向铁电极附近滴入几滴铁氰化钾溶液,可观察到_______ 。
(4)电池工作一段时间后,乙池中石墨电极上产生 (标准状况)气体,则甲池中消耗
(标准状况)气体,则甲池中消耗 的质量为
的质量为_______ g,石墨电极增重_______ g。
 燃料电池的工作示意图如图,乙池中的电解质溶液为
燃料电池的工作示意图如图,乙池中的电解质溶液为 物质的量浓度均为
物质的量浓度均为 的
的 的混合溶液,一段时间后,观察到乙池中铁片溶解。
的混合溶液,一段时间后,观察到乙池中铁片溶解。
(1)乙池中的能量转化形式为
(2)气体Y为
 的移动方向为
的移动方向为(3)乙池中铁电极发生的电极反应为
(4)电池工作一段时间后,乙池中石墨电极上产生
 (标准状况)气体,则甲池中消耗
(标准状况)气体,则甲池中消耗 的质量为
的质量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】电化学技术在处理污染气体领域的应用广泛。
(1)利用反应 构成电池的方法,既能实现有效消除氮氧化物的排放,又能提供电能,装置如图所示。
构成电池的方法,既能实现有效消除氮氧化物的排放,又能提供电能,装置如图所示。
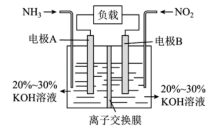
①A电极的电极反应式为___________ 。
②下列关于该电池的说法正确的是___________ 。
A.电子从右侧电极经过负载后流向左侧电极
B.为使电池持续放电,离子交换膜需选用阴离子交换膜
C.电池工作一段时间,溶液的 不变
不变
D.当有 被处理时,转移电子物质的量为
被处理时,转移电子物质的量为
(2)以含 废气为原料,用电化学方法制取硫酸。装置如图。
废气为原料,用电化学方法制取硫酸。装置如图。

写出负极电极反应式___________ 。
(1)利用反应
 构成电池的方法,既能实现有效消除氮氧化物的排放,又能提供电能,装置如图所示。
构成电池的方法,既能实现有效消除氮氧化物的排放,又能提供电能,装置如图所示。
①A电极的电极反应式为
②下列关于该电池的说法正确的是
A.电子从右侧电极经过负载后流向左侧电极
B.为使电池持续放电,离子交换膜需选用阴离子交换膜
C.电池工作一段时间,溶液的
 不变
不变D.当有
 被处理时,转移电子物质的量为
被处理时,转移电子物质的量为
(2)以含
 废气为原料,用电化学方法制取硫酸。装置如图。
废气为原料,用电化学方法制取硫酸。装置如图。
写出负极电极反应式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】课题式研究性学习是培养学生创造性思维的良好方法,某研究性学习小组将下列装置如图连接,C、D、E、F、X、Y都是惰性电极。将电源接通后,向乙中滴入酚酞试液,在F极附近显红色。试回答下列问题:

(1)电源A极的名称是____________ 。
(2)甲装置中电解反应的总化学方程式:______________________________ 。
(3)如果收集乙装置中产生的气体,两种气体的体积比是____________ 。
(4)欲用丙装置给铜镀银,G应该是__________ (填“铜”或“银”),电镀液的主要成分是___________ (填化学式)。
(5)装置丁中的现象是_______________ 。

(1)电源A极的名称是
(2)甲装置中电解反应的总化学方程式:
(3)如果收集乙装置中产生的气体,两种气体的体积比是
(4)欲用丙装置给铜镀银,G应该是
(5)装置丁中的现象是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】如图A为直流电源,B为浸泡饱和NaCl溶液和酚酞溶液的滤纸,C为电镀槽,接通电路后,发现B上的c点显红色。请填空:

(1)电源A上的a为_______ 极;
(2)滤纸B上发生的总化学方程式为_________________ ;
(3)欲在电镀槽中实现铁上镀锌,接通K点,使c、d两点短路,则电极e材料为_______ (写物质名称),电极f上发生的反应为____________ ,槽中盛放的电镀液可以是_______________ ,电镀液浓度 _________ (不变、变大、变小)。

(1)电源A上的a为
(2)滤纸B上发生的总化学方程式为
(3)欲在电镀槽中实现铁上镀锌,接通K点,使c、d两点短路,则电极e材料为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】如图所示,某同学设计了一个燃料电池并探究氯碱工业原理和电镀实验,其中乙装置中X为离子交换膜。请按要求回答相关问题:
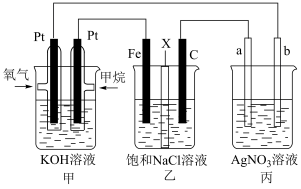
(1)甲烷燃料电池负极反应式是___________ 。
(2) 电极的电极反应式为
电极的电极反应式为___________ 。
(3)X选择___________ 离子交换膜(填“阴”或“阳”)。
(4)若在标准状况下,甲装置有112mL氧气参加反应,则乙装置中左侧极室的 为
为___________ 。(设该极室内溶液体积为 )
)
(5)若用丙装置给铜制品镀银,铜制品应放在___________ (填“a”或“b”)极,反应结束后 溶液的浓度
溶液的浓度___________ (填“变大”、“变小”或“不变”)。
(6)若a、b为惰性电极,写出图丙中电解总反应的离子反应方程式___________ 。

(1)甲烷燃料电池负极反应式是
(2)
 电极的电极反应式为
电极的电极反应式为(3)X选择
(4)若在标准状况下,甲装置有112mL氧气参加反应,则乙装置中左侧极室的
 为
为 )
)(5)若用丙装置给铜制品镀银,铜制品应放在
 溶液的浓度
溶液的浓度(6)若a、b为惰性电极,写出图丙中电解总反应的离子反应方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】金属的腐蚀
(1)概念:金属或合金与周围的_______ 发生_______ 反应而引起损耗的现象。其实质是金属原子_______ 电子变为阳离子,金属发生_______ 反应。
(2)根据与金属接触的_______ 不同,金属腐蚀可分为两类:
①化学腐蚀:金属与其表面接触的一些物质(如_______ 等)直接反应而引起的腐蚀。腐蚀的速率随温度升高而_______ 。
②电化学腐蚀:当_______ 的金属与_______ 溶液接触时会发生_______ 反应,比较_______ 的金属发生氧化反应而被腐蚀。
(1)概念:金属或合金与周围的
(2)根据与金属接触的
①化学腐蚀:金属与其表面接触的一些物质(如
②电化学腐蚀:当
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】金属的腐蚀可分为化学腐蚀和电化学腐蚀。下列腐蚀类型中
①铜板在氯化铁溶液中被腐蚀②钢铁在空气中生锈而被腐蚀③化工厂里的铁与氯气反应被腐蚀④铜铝电线接头处铝被腐蚀⑤高温下铁丝被氧气腐蚀⑥铜在空气中生成铜绿而被腐蚀
(1)属于化学腐蚀是_______________ (填序号,下同)。
(2)属于电化学腐蚀的是_______________ 。
①铜板在氯化铁溶液中被腐蚀②钢铁在空气中生锈而被腐蚀③化工厂里的铁与氯气反应被腐蚀④铜铝电线接头处铝被腐蚀⑤高温下铁丝被氧气腐蚀⑥铜在空气中生成铜绿而被腐蚀
(1)属于化学腐蚀是
(2)属于电化学腐蚀的是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】芜湖是安徽省第二个建设轨道交通的城市,目前1、2号线在建,工程建设需要大量水泥、钢铁等材料。
(1)工业上生产水泥的主要原料是石灰石和_______ 。轨道交通信息传输系统中使用的光导纤维主要成分是_______ 。
(2)钢铁在潮湿的空气中可发生析氢腐蚀,其中正极电极反应式为_______ 。
(3)轨道交通的使用有助于缓解城市交通压力,提高环境质量。
①空气质量报告的各项指标可反映出空气质量。下列物质已纳入我国空气质量报告的是_______ (填字母)。
a. b.可吸入颗粒物 c.
b.可吸入颗粒物 c.
②在机动车尾气系统中安装催化转化器,可将尾气中的 、
、 转化为无害的
转化为无害的 和
和_______ 。
③复合材料“钙塑板”质轻、消声、隔热,以高压聚乙烯、轻质碳酸钙及少量助剂为原料压制而成,聚乙烯的结构简式为_______ 。
(1)工业上生产水泥的主要原料是石灰石和
(2)钢铁在潮湿的空气中可发生析氢腐蚀,其中正极电极反应式为
(3)轨道交通的使用有助于缓解城市交通压力,提高环境质量。
①空气质量报告的各项指标可反映出空气质量。下列物质已纳入我国空气质量报告的是
a.
 b.可吸入颗粒物 c.
b.可吸入颗粒物 c.
②在机动车尾气系统中安装催化转化器,可将尾气中的
 、
、 转化为无害的
转化为无害的 和
和③复合材料“钙塑板”质轻、消声、隔热,以高压聚乙烯、轻质碳酸钙及少量助剂为原料压制而成,聚乙烯的结构简式为
您最近一年使用:0次



