下表是元素周期表的一部分,请针对表中所列标号为①~⑩的元素回答下列问题。
(1)非金属性最强的元素是____ (填元素符号,下同),考古时利用____ 测定一些文物的年代。
(2)第三周期元素除⑩外原子半径最小的是____ (填元素符号),这些元素的最高价氧化物对应水化物中碱性最强的是____ (填氧化物的化学式,下同)、具有两性的是____ 。
(3)由⑨和⑥两种元素组成的化合物的电子式是____ ;
(4)②和③两种元素的气态氢化物更稳定的是____ (填“②”或“③”)。
| IA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 二 | ① | ② | ③ | ④ | ||||
| 三 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
(1)非金属性最强的元素是
(2)第三周期元素除⑩外原子半径最小的是
(3)由⑨和⑥两种元素组成的化合物的电子式是
(4)②和③两种元素的气态氢化物更稳定的是
更新时间:2020-07-28 04:27:22
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】元素周期表的形式多种多样,如图是扇形元素周期表的一部分,回答下列问题:
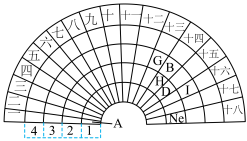
(1)已知 的最外层电子数为2,则
的最外层电子数为2,则 的原子结构示意图为
的原子结构示意图为___________ 。
(2)元素B的最高价氧化物能溶于一种酸,发生反应的化学方程式为___________ ;元素 的最高价氧化物的电子式为
的最高价氧化物的电子式为___________ 。
(3)下列不能证明非金属性: 的是
的是___________ (填字母)。
a.气态氢化物的稳定性:
b.含氧酸的酸性:
c.气态氢化物的还原性:
(4)用A、D、G表示上述周期表中相应元素形成的单质,甲、乙、丙、丁、戊为短周期元素组成的化合物。戊是一种难溶于水的白色胶状物质,既能与强酸反应,也能与强碱反应。丁是一种高能燃料,其组成元素与丙相同, 丁分子中含有
丁分子中含有 电子。
电子。
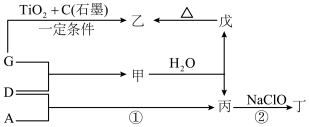
①戊的化学式为___________ 。
②丁中所含化学键类型是___________ 。
③甲被大量用于制造电子元件,工业上用乙、H的单质和D的单质在高温下制备甲,其中乙和H单质的物质的量之比为 ,该反应的化学方程式为
,该反应的化学方程式为___________ 。

(1)已知
 的最外层电子数为2,则
的最外层电子数为2,则 的原子结构示意图为
的原子结构示意图为(2)元素B的最高价氧化物能溶于一种酸,发生反应的化学方程式为
 的最高价氧化物的电子式为
的最高价氧化物的电子式为(3)下列不能证明非金属性:
 的是
的是a.气态氢化物的稳定性:

b.含氧酸的酸性:

c.气态氢化物的还原性:

(4)用A、D、G表示上述周期表中相应元素形成的单质,甲、乙、丙、丁、戊为短周期元素组成的化合物。戊是一种难溶于水的白色胶状物质,既能与强酸反应,也能与强碱反应。丁是一种高能燃料,其组成元素与丙相同,
 丁分子中含有
丁分子中含有 电子。
电子。
①戊的化学式为
②丁中所含化学键类型是
③甲被大量用于制造电子元件,工业上用乙、H的单质和D的单质在高温下制备甲,其中乙和H单质的物质的量之比为
 ,该反应的化学方程式为
,该反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】下表为元素周期表的一部分,请参照元素①一⑩在周期表中的位置,用元素符号或化学式回答下列问题。
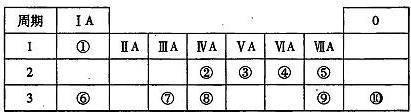
(1)⑤、⑥、⑦的原子半径由大到小的顺序___________ 。
(2)②、③、⑧的最高价含氧酸的酸性由强到弱的顺序是_____________ 。
(3)①、④、⑥、⑨中的某些元素可以形成既含有离子键又含有共价键的化合物,写出其中两种不同类别物质的化学式_________ 、___________ 。
(4)上表中所列出的部分元素能形成多种带有18个电子的分子,请写出其中三种的化学式
_____________ 。

(1)⑤、⑥、⑦的原子半径由大到小的顺序
(2)②、③、⑧的最高价含氧酸的酸性由强到弱的顺序是
(3)①、④、⑥、⑨中的某些元素可以形成既含有离子键又含有共价键的化合物,写出其中两种不同类别物质的化学式
(4)上表中所列出的部分元素能形成多种带有18个电子的分子,请写出其中三种的化学式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】元素周期表是学习物质结构和性质的重要工具,下图是元素周期表的一部分,表中所列字母A、D、F、G、Q、M、R、N、T分别代表某种化学元素。请依据这9种元素回答下列问题
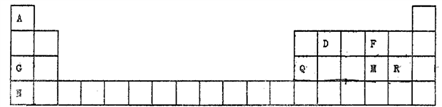
(1)金属性最强的元素是_______ (填元素符号),写出表中所绘元素的氧化物中具有两性的氧化物与表中所给的元素中碱性最强的最高价氧化物的水化物的离子反应:_______ 。
(2)元素的非金属性: M_______ R(填“>”或“<”)。
(3)R的最高价氧化物对应水化物的化学式是_______ 。
(4)F、G两元素形成的淡黄色固体物质的电子式为____ ,该物质含有的化学键的类型是___ 。
(5)表中某些元素的原子可形成与Ar具有相同电子层结构的简单离子,这些离子的半径由大到小的顺序是_______ (填离子符号)。
(6)表中某元素原子的核外电子层数是最外层电子数的3倍,该元素的原子结构示意图为_____ 。

(1)金属性最强的元素是
(2)元素的非金属性: M
(3)R的最高价氧化物对应水化物的化学式是
(4)F、G两元素形成的淡黄色固体物质的电子式为
(5)表中某些元素的原子可形成与Ar具有相同电子层结构的简单离子,这些离子的半径由大到小的顺序是
(6)表中某元素原子的核外电子层数是最外层电子数的3倍,该元素的原子结构示意图为
您最近一年使用:0次
【推荐1】Ⅰ.我国科学家在铁基高温超导体的研究上取得重大突破,发现了该超导体是由Fe、Ba、As三种元素组成,这为进一步理解超导配对机理及其与电荷密度波的关系提供了重要实验证据。回答下列问题:
(1)As元素属于元素周期表的________ 区元素,其价电子排布式是________ 。
(2)基态Fe原子核外电子排布式为________ 。 的稳定性强于
的稳定性强于 ,从微观角度解释其原因为
,从微观角度解释其原因为________ 。
Ⅱ.某元素原子的最外电子层只有一个电子,该电子的电子层数n=4。请回答下列问题:
(3)符合上述条件的元素共有________ 种。
(4)在符合上述条件的元素中,原子序数最小的在元素周期表中的________ 区(用符号填空),原子序数最大的在周期表位置________ 。
(5)过渡元素的金属离子与水分子形成的配合物是否有颜色,与其d轨道电子排布有关。一般而言,为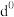 或
或 排布时,无颜色,为
排布时,无颜色,为 排布时,有颜色,如
排布时,有颜色,如 显粉红色。据此判断,
显粉红色。据此判断,
________ (填“无”或“有”)颜色。
(1)As元素属于元素周期表的
(2)基态Fe原子核外电子排布式为
 的稳定性强于
的稳定性强于 ,从微观角度解释其原因为
,从微观角度解释其原因为Ⅱ.某元素原子的最外电子层只有一个电子,该电子的电子层数n=4。请回答下列问题:
(3)符合上述条件的元素共有
(4)在符合上述条件的元素中,原子序数最小的在元素周期表中的
(5)过渡元素的金属离子与水分子形成的配合物是否有颜色,与其d轨道电子排布有关。一般而言,为
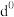 或
或 排布时,无颜色,为
排布时,无颜色,为 排布时,有颜色,如
排布时,有颜色,如 显粉红色。据此判断,
显粉红色。据此判断,
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】标号为①~⑩的元素,在元素周期表中的位置如下:
试回答下列问题:
(1)(填写元素符号)①_____ ③______ ⑤_____ ⑦_____
(2)①和④号元素形成的化合物的化学式为________ ,用电子式表示其形成过程为__________ 。
(3)⑦和⑧号元素的最高价氧化物的水化物的碱性是:______ ﹥_________ (填化学式)。⑨和⑩号元素的最高价氧化物的水化物的酸性是: ______ ﹥_________ (填化学式)。
(4)①、⑤、⑦号元素形成的一种化合物的电子式是________ ,在该化合物中既含有________ 键,又含有________ 键。
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 1 | ① | ② | ||||||
| 2 | ③ | ④ | ⑤ | ⑥ | ||||
| 3 | ⑦ | ⑧ | ⑨ | ⑩ |
试回答下列问题:
(1)(填写元素符号)①
(2)①和④号元素形成的化合物的化学式为
(3)⑦和⑧号元素的最高价氧化物的水化物的碱性是:
(4)①、⑤、⑦号元素形成的一种化合物的电子式是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】下表为长式周期表的一部分,其中的编号代表对应的元素。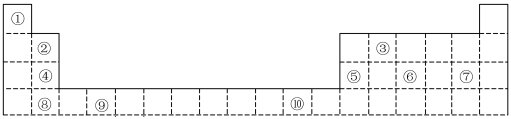
请回答下列问题:
(1)表中属于d区元素的是________ (填元素符号)。
(2)表中元素①的6个原子与元素③的6个原子形成的某种环状分子名称为____ ;③和⑦形成的一种常见溶剂的化学式为_____ 。
(3)元素④的第一电离能________ 元素⑤(选填“>”、“=”或“<”)的第一电离能;元素⑥的电负性________ 元素⑦(选填“>”、“=”或“<”)的电负性。
(4)元素⑦和⑧形成的化合物的电子式为________________ 。
(5)某些不同族元素的性质也有一定的相似性,如上表中元素②与元素⑤的氢氧化物有相似的性质。请写出元素②的氢氧化物与NaOH溶液反应的化学方程式:________ 。

请回答下列问题:
(1)表中属于d区元素的是
(2)表中元素①的6个原子与元素③的6个原子形成的某种环状分子名称为
(3)元素④的第一电离能
(4)元素⑦和⑧形成的化合物的电子式为
(5)某些不同族元素的性质也有一定的相似性,如上表中元素②与元素⑤的氢氧化物有相似的性质。请写出元素②的氢氧化物与NaOH溶液反应的化学方程式:
您最近一年使用:0次



