Ⅰ.我国科学家在铁基高温超导体的研究上取得重大突破,发现了该超导体是由Fe、Ba、As三种元素组成,这为进一步理解超导配对机理及其与电荷密度波的关系提供了重要实验证据。回答下列问题:
(1)As元素属于元素周期表的________ 区元素,其价电子排布式是________ 。
(2)基态Fe原子核外电子排布式为________ 。 的稳定性强于
的稳定性强于 ,从微观角度解释其原因为
,从微观角度解释其原因为________ 。
Ⅱ.某元素原子的最外电子层只有一个电子,该电子的电子层数n=4。请回答下列问题:
(3)符合上述条件的元素共有________ 种。
(4)在符合上述条件的元素中,原子序数最小的在元素周期表中的________ 区(用符号填空),原子序数最大的在周期表位置________ 。
(5)过渡元素的金属离子与水分子形成的配合物是否有颜色,与其d轨道电子排布有关。一般而言,为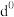 或
或 排布时,无颜色,为
排布时,无颜色,为 排布时,有颜色,如
排布时,有颜色,如 显粉红色。据此判断,
显粉红色。据此判断,
________ (填“无”或“有”)颜色。
(1)As元素属于元素周期表的
(2)基态Fe原子核外电子排布式为
 的稳定性强于
的稳定性强于 ,从微观角度解释其原因为
,从微观角度解释其原因为Ⅱ.某元素原子的最外电子层只有一个电子,该电子的电子层数n=4。请回答下列问题:
(3)符合上述条件的元素共有
(4)在符合上述条件的元素中,原子序数最小的在元素周期表中的
(5)过渡元素的金属离子与水分子形成的配合物是否有颜色,与其d轨道电子排布有关。一般而言,为
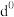 或
或 排布时,无颜色,为
排布时,无颜色,为 排布时,有颜色,如
排布时,有颜色,如 显粉红色。据此判断,
显粉红色。据此判断,
更新时间:2024-04-10 09:58:14
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】在周期表中找到第3横行17纵行的元素,回答下列问题:
(1)该元素的符号是________ ,其原子结构示意图为________
(2)该元素位于第________ 周期,第________ 族。
(3)写出下列反应的化学方程式:
①该元素的单质+水:_______________________________________ ;
②该元素的单质+氢氧化钠:_________________________________ 。
(1)该元素的符号是
(2)该元素位于第
(3)写出下列反应的化学方程式:
①该元素的单质+水:
②该元素的单质+氢氧化钠:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】I. 填空:
(1)写出表示含有8个质子、10个中子的原子的化学符号:_________ 。
(2)元素周期表中位于第8纵行的铁元素属于_________ 族。
(3)元素周期表中最活泼的非金属元素位于第_________ 纵行。
(4)所含元素超过18种的周期是第_________ 周期。
II. 4种相邻主族短周期元素的相对位置如表,元素x的原子核外电子数是m的2倍,y的氧化物具有两性。
(1)元素x在周期表中的位置是第________ 周期、第________ 族。
(2)四种元素最高价氧化物的水化物中,酸性最强的是_____ ,碱性最强的是_____ (填化学式)。
(1)写出表示含有8个质子、10个中子的原子的化学符号:
(2)元素周期表中位于第8纵行的铁元素属于
(3)元素周期表中最活泼的非金属元素位于第
(4)所含元素超过18种的周期是第
II. 4种相邻主族短周期元素的相对位置如表,元素x的原子核外电子数是m的2倍,y的氧化物具有两性。
| m | n | ||
| x | y |
(1)元素x在周期表中的位置是第
(2)四种元素最高价氧化物的水化物中,酸性最强的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】下表是元素周期表的一部分,按要求回答下列问题:
(1)⑦的原子结构示意图为___________ ;
(2)①~⑩对应元素中,非金属性最强的是___________ (填元素符号,下同),金属性最强的是___________ ,单质的化学性质最不活泼的是___________ ;
(3)②③④三种元素对应的单质中,最容易与H2化合的是___________ (填化学式,下同),⑥⑦⑧三种元素的最高价氧化物对应水化物中,碱性由弱到强的顺序是___________ ;
(4)请用电子式表示⑦和⑩反应时生成化合物的形成过程:___________ ;
(5)④和⑩元素对应的氢化物的沸点___________ (填化学式)更高,原因是___________ 。
| 族 周期 | ⅠA | ⅡA | ··· | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | ① | ||||||||
| 2 | ② | ③ | ④ | ⑤ | |||||
| 3 | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
(1)⑦的原子结构示意图为
(2)①~⑩对应元素中,非金属性最强的是
(3)②③④三种元素对应的单质中,最容易与H2化合的是
(4)请用电子式表示⑦和⑩反应时生成化合物的形成过程:
(5)④和⑩元素对应的氢化物的沸点
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】下表是元素周期表中的一部分。
根据A—J在周期表中的位置,用元素符号或化学式 回答下列问题:
(1)化学性质最不活泼的元素是___________ ,氧化性最强的单质是_______ ,用一个化学反应证明H单质的氧化性强于G单质____________________________ 。
(2)D的最高价氧化物与I的最高价氧化物对应的水化物反应的离子方程式为_____________ 。
(3)A分别与F、G、H形成的简单化合物中,稳定性由强到弱的顺序为_______________ 。
(4)B、C、D、G、I离子半径由大到小的顺序是_______________________ 。
(5)用电子式表示化合物MgCl2的形成过程_________________________ 。
族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
1 | A | |||||||
2 | E | F | G | H | J | |||
3 | B | C | D | I |
根据A—J在周期表中的位置,用
(1)化学性质最不活泼的元素是
(2)D的最高价氧化物与I的最高价氧化物对应的水化物反应的离子方程式为
(3)A分别与F、G、H形成的简单化合物中,稳定性由强到弱的顺序为
(4)B、C、D、G、I离子半径由大到小的顺序是
(5)用电子式表示化合物MgCl2的形成过程
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】下表为长式周期表的一部分,其中的编号代表对应的元素。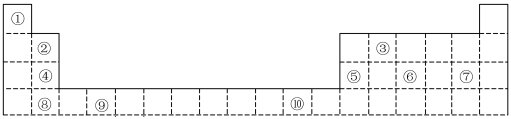
请回答下列问题:
(1)表中属于d区元素的是________ (填元素符号)。
(2)表中元素①的6个原子与元素③的6个原子形成的某种环状分子名称为____ ;③和⑦形成的一种常见溶剂的化学式为_____ 。
(3)元素④的第一电离能________ 元素⑤(选填“>”、“=”或“<”)的第一电离能;元素⑥的电负性________ 元素⑦(选填“>”、“=”或“<”)的电负性。
(4)元素⑦和⑧形成的化合物的电子式为________________ 。
(5)某些不同族元素的性质也有一定的相似性,如上表中元素②与元素⑤的氢氧化物有相似的性质。请写出元素②的氢氧化物与NaOH溶液反应的化学方程式:________ 。

请回答下列问题:
(1)表中属于d区元素的是
(2)表中元素①的6个原子与元素③的6个原子形成的某种环状分子名称为
(3)元素④的第一电离能
(4)元素⑦和⑧形成的化合物的电子式为
(5)某些不同族元素的性质也有一定的相似性,如上表中元素②与元素⑤的氢氧化物有相似的性质。请写出元素②的氢氧化物与NaOH溶液反应的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】原子序数依次增大的四种主族元素A、B、C、D分别处于第一至第四周期,其中A原子核是一个质子;B原子核外电子有6种不同的运动状态,B与C可形成正四面体型分子,D原子外围电子排布为3d104s1。请回答下列问题:
(1)这四种元素中电负性最大的是____ (填元素符号)、第一电离能最小的是____ (填元素符号)
(2)C所在的主族元素气态氢化物中,沸点最低的是_____ (填化学式)
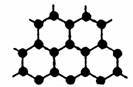
(3)B元素可形成多种单质,其中“只有一层原子厚”的物质,被公认为目前世界上已知的最薄、最坚硬、传导电子速度最快的新型材料,该材料晶体结构如右图所示,其原子的杂化类型为____________ ;
(4)D的水合醋酸盐晶体局部结构如右图,该晶体中含有的化学键是___ (填选项序号);
①极性键 ②非极性键 ③配位键 ④金属键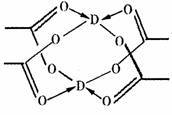
(1)这四种元素中电负性最大的是
(2)C所在的主族元素气态氢化物中,沸点最低的是
(3)B元素可形成多种单质,其中“只有一层原子厚”的物质,被公认为目前世界上已知的最薄、最坚硬、传导电子速度最快的新型材料,该材料晶体结构如右图所示,其原子的杂化类型为

(4)D的水合醋酸盐晶体局部结构如右图,该晶体中含有的化学键是
①极性键 ②非极性键 ③配位键 ④金属键

您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】A元素原子M电子层上有6个电子。B元素与A元素的原子核外电子层数相同,B元素的原子最外电子层只有1个电子。
(1)B元素的原子结构示意图为___________ 。
(2)A、B两元素形成的化合物的名称是________________ 。
(3)用电子式表示B2A的形成过程______________________
(1)B元素的原子结构示意图为
(2)A、B两元素形成的化合物的名称是
(3)用电子式表示B2A的形成过程
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】已知W、Y、Z、T均为短周期元素,且原子半径依次增大。请填空:
(1)W、Z是形成化合物种类最多的两种元素,写出Z原子的核外电子排布图____ ;
(2)化合物YW3的水溶液能使酚酞变红,用方程式表示酚酞变红的原因_________ ;
(3)元素T的原子中电子共占据了7个轨道,则T在元素周期表____ 周期____ 族。T的化合物TY熔融时不导电,常用作砂轮及耐高温材料,由此推知,它属于_____ .
a离子晶体 b.原子晶体 c.分子晶体 d.无法判断断
(4)YW3属于______ (填“极性”、“非极性”)分子其中Y的化合价为______ .
(1)W、Z是形成化合物种类最多的两种元素,写出Z原子的核外电子排布图
(2)化合物YW3的水溶液能使酚酞变红,用方程式表示酚酞变红的原因
(3)元素T的原子中电子共占据了7个轨道,则T在元素周期表
a离子晶体 b.原子晶体 c.分子晶体 d.无法判断断
(4)YW3属于
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】下列原子或离子的电子排布式或排布图正确的是________ (填序号,下同),违反能量最低原理的是____________ ,违反洪特规则的是________ ,违反泡利原理的是________ 。
①Ca2+:1s22s22p63s23p6 ②F-:1s22s23p6
③P: ④Cr:1s22s22p63s23p63d44s2
④Cr:1s22s22p63s23p63d44s2
⑤Fe:1s22s22p63s23p63d64s2 ⑥Mg2+:1s22s22p6⑦C: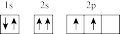
①Ca2+:1s22s22p63s23p6 ②F-:1s22s23p6
③P:
 ④Cr:1s22s22p63s23p63d44s2
④Cr:1s22s22p63s23p63d44s2⑤Fe:1s22s22p63s23p63d64s2 ⑥Mg2+:1s22s22p6⑦C:
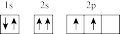
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】我国科学家合成了一种深紫外非线性光学晶体新材料ABF,晶体中的阴离子为[RY3Z]4-,阳离子为[XQ4]+。Q、R、X、Y和Z为原子序数依次增大的主族元素,基态Y原子最外层有两个未成对电子,Z为电负性最强的元素,Q、R、X和Z质子数均为奇数且和为22。请回答下列问题:
(1)基态Y原子核外电子有______ 种空间运动状态。Y、Z形成的简单离子半径较大的是______ (用离子符号表示)。
(2)基态Z原子中能量最高的电子占据的原子轨道呈______ 形。Q与Y形成的既含极性键又含非极性键的化合物的电子式为______ 。
(3)X2Z2分子中,X原子的杂化类型为sp2,分子中σ键和π键的数目比为______ 。YZ2主要用于火箭工程液体助燃剂,其分子的空间构型为______ 。
(1)基态Y原子核外电子有
(2)基态Z原子中能量最高的电子占据的原子轨道呈
(3)X2Z2分子中,X原子的杂化类型为sp2,分子中σ键和π键的数目比为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】氯吡苯脲是一种常用的膨大剂,其结构简式为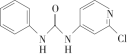 ,它是经国家批准使用的植物生长调节剂。请回答下列问题:
,它是经国家批准使用的植物生长调节剂。请回答下列问题:
(1)基态氯原子核外未成对电子数为_______ 。
(2)氯吡苯脲分子中,氮原子的杂化类型为_______ ,碳原子的杂化类型为_______ ,该分子_______ (填“是”或“不是”)手性分子。
(3)查阅文献知,可用2-氯-4-氨基吡啶与异氰酸苯酯反应生成氯吡苯脲。反应方程式如下:
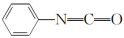 +
+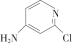 ―→
―→
反应过程中,每生成1mol氯吡苯脲,断裂_______ 个σ键、_______ 个π键。
(4)膨大剂能在动物体内代谢,其产物较为复杂,其中有H2O、NH3、CO2等。
①请用共价键知识解释H2O比NH3稳定的原因:_______ 。
②CO2的水溶液中含有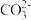 ,则该阴离子的VSEPR模型名称为
,则该阴离子的VSEPR模型名称为_______ ,中心原子的杂化类型为_______ 。
 ,它是经国家批准使用的植物生长调节剂。请回答下列问题:
,它是经国家批准使用的植物生长调节剂。请回答下列问题:(1)基态氯原子核外未成对电子数为
(2)氯吡苯脲分子中,氮原子的杂化类型为
(3)查阅文献知,可用2-氯-4-氨基吡啶与异氰酸苯酯反应生成氯吡苯脲。反应方程式如下:
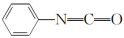 +
+ ―→
―→
反应过程中,每生成1mol氯吡苯脲,断裂
(4)膨大剂能在动物体内代谢,其产物较为复杂,其中有H2O、NH3、CO2等。
①请用共价键知识解释H2O比NH3稳定的原因:
②CO2的水溶液中含有
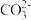 ,则该阴离子的VSEPR模型名称为
,则该阴离子的VSEPR模型名称为
您最近一年使用:0次



