氯吡苯脲是一种常用的膨大剂,其结构简式为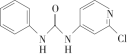 ,它是经国家批准使用的植物生长调节剂。请回答下列问题:
,它是经国家批准使用的植物生长调节剂。请回答下列问题:
(2)氯吡苯脲分子中,氮原子的杂化类型为
(3)查阅文献知,可用2-氯-4-氨基吡啶与异氰酸苯酯反应生成氯吡苯脲。反应方程式如下:
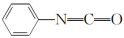 +
+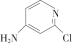 ―→
―→
(4)膨大剂能在动物体内代谢,其产物较为复杂,其中有H2O、NH3、CO2等。
①请用共价键知识解释H2O比NH3稳定的原因:
②CO2的水溶液中含有
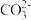 ,则该阴离子的VSEPR模型名称为
,则该阴离子的VSEPR模型名称为
2022高三·全国·专题练习 查看更多[1]
(已下线)第30讲 分子结构与性质(练)-2023年高考化学一轮复习讲练测(新教材新高考)
更新时间:2022/10/17 17:05:49
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】下表是元素周期表的一部分,表中所列的每个序号分别代表某一元素。
(1)元素②在周期表的位置是_______ 。元素③④组成原子个数比为1:1的化合物的电子式_______ 。
(2)⑦⑧⑨分别形成的简单离子,它们的离子半径由小到大的顺序是_______ (填离子符号)。
(3)元素⑩原子最外层电子数是L层电子数的1/4,其二价阳离子的电子数为24,请画出该元素的原子结构示意图_______ 。
(4)写出工业制取元素⑥的单质的化学方程式_______ 。
(5)第四周期中分别与①、②同主族的Ga、As形成的GaAs的熔点为1238℃,其熔融状态下不导电。GaAs属于_______ (填“离子化合物”或“共价化合物”);元素⑤与Ga性质相似,下列关于Ga说法错误的是_______ (填写序号)。
A.一定条件下,Ga可溶于强酸与强碱
B.常温下,Ga可与水剧烈反应
C.Ga(OH)3受热能分解
D.一定条件下,Ga2O3可与NaOH溶液反应
| ① | ② | ③ | |||||||||||||||
| ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||||||||||||
| ⑨ | ⑩ |
(1)元素②在周期表的位置是
(2)⑦⑧⑨分别形成的简单离子,它们的离子半径由小到大的顺序是
(3)元素⑩原子最外层电子数是L层电子数的1/4,其二价阳离子的电子数为24,请画出该元素的原子结构示意图
(4)写出工业制取元素⑥的单质的化学方程式
(5)第四周期中分别与①、②同主族的Ga、As形成的GaAs的熔点为1238℃,其熔融状态下不导电。GaAs属于
A.一定条件下,Ga可溶于强酸与强碱
B.常温下,Ga可与水剧烈反应
C.Ga(OH)3受热能分解
D.一定条件下,Ga2O3可与NaOH溶液反应
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】将下列物质按要求填空
①131 I 与132I ②C60 与石墨 ③CH3Cl 与CH3CH2Cl ④硫酸氢钠 ⑤ 氯化镁 ⑥氩
⑦过氧化氢 ⑧
⑨CS2 ⑩过氧化钠
(1)互为同位素的是_______________________
(2)互为同素异形体的是__________________________
(3)互为同系物的是________________________________
(4)⑧中两种物质的关系是______________ (同系物,同素异形体,同一种物质)
(5)含共价键的离子化合物__________________________________
(6)仅含共价键的物质______________________________________
(7)用电子式表示⑨的形成过程______________________________
①131 I 与132I ②C60 与石墨 ③CH3Cl 与CH3CH2Cl ④硫酸氢钠 ⑤ 氯化镁 ⑥氩
⑦过氧化氢 ⑧

⑨CS2 ⑩过氧化钠
(1)互为同位素的是
(2)互为同素异形体的是
(3)互为同系物的是
(4)⑧中两种物质的关系是
(5)含共价键的离子化合物
(6)仅含共价键的物质
(7)用电子式表示⑨的形成过程
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】(1)下列变化中①NaCl 溶于水 ②HCl 溶于水 ③ 葡萄糖溶于水
④Na2O2溶于水 ⑤ I2升华 ⑥固体NaOH熔化。
未发生化学键破坏的是_____ ,仅发生离子键破坏的是________ ,仅发生共价键破坏的是_______ ,既发生离子键破坏,又发生共价键破坏的是____________ (填序号)。
(2)对于下列物质:(填序号)
①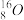 ②
② ③
③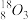 ④
④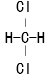 ⑤
⑤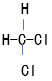 ⑥
⑥
⑦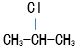 ⑧一氯甲烷 ⑨ CCl4 ⑩ CH3-CH2-CH2-Cl
⑧一氯甲烷 ⑨ CCl4 ⑩ CH3-CH2-CH2-Cl
属于同一物质的是___________________ ;
互为同位素的是______________________ ;
互为同分异构体的是_____________________ ;
互为同系物的是⑩和______________________ ;
④Na2O2溶于水 ⑤ I2升华 ⑥固体NaOH熔化。
未发生化学键破坏的是
(2)对于下列物质:(填序号)
①
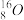 ②
② ③
③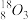 ④
④ ⑤
⑤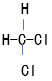 ⑥
⑥
⑦
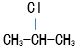 ⑧一氯甲烷 ⑨ CCl4 ⑩ CH3-CH2-CH2-Cl
⑧一氯甲烷 ⑨ CCl4 ⑩ CH3-CH2-CH2-Cl属于同一物质的是
互为同位素的是
互为同分异构体的是
互为同系物的是⑩和
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】如图是s能级和p能级的电子云轮廓图,试回答问题。
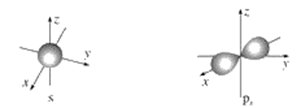
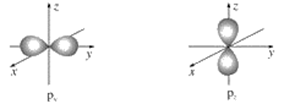
(1)s电子云轮廓图呈________ 形,每个s能级有________ 个原子轨道;p电子云轮廓图呈________ 状,每个p能级有________ 个原子轨道,其能量关系为____________ (填“相同”或“不相同”)。
(2)元素X的原子最外层的电子排布式为nsnnpn+1,原子中能量最高的是________ 电子;元素X的名称是____ ,它的氢化物的电子式是________ 。
(3)若元素Y的原子最外层的电子排布式为nsn-1npn+1,那么Y的元素符号应为________ ,原子的电子排布图为______________________________ 。
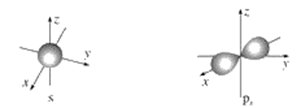
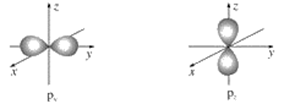
(1)s电子云轮廓图呈
(2)元素X的原子最外层的电子排布式为nsnnpn+1,原子中能量最高的是
(3)若元素Y的原子最外层的电子排布式为nsn-1npn+1,那么Y的元素符号应为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】填空。
(1))蓝矾(CuSO4·5H2O)的结构如图所示:
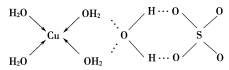
 的空间结构是
的空间结构是___________ ,其中S原子的杂化轨道类型是___________ ;基态O原子的价轨道表示式为___________ 。
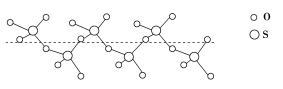
(2)气态SO3分子的空间结构为___________ ;将纯液态SO3冷却到289.8K时凝固得到一种螺旋状单链结构的固体,其结构如图,此固态SO3中S原子的杂化轨道类型是___________ 。
(1))蓝矾(CuSO4·5H2O)的结构如图所示:

 的空间结构是
的空间结构是(2)气态SO3分子的空间结构为

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】氮族元素包括氮、磷、砷、锑、铋等元素,其单质及其化合物在研究和生产中有着广泛的应用。试回答下列问题:
(1)NaNO2是一种重要的化工原料,有毒,NaNO2也是一种食品添加剂,使用时须严格控制用量。已知:HNO2有强氧化性,酸性H2SO3>HNO2>CH3COOH。
①氮原子核外共有____ 种能量不同的电子。
②亚硝酰氯(NOCl)是一种红褐色液体,每个原子最外层都达到8e-结构,则其电子式为____ ,其水解会生成两种酸,写出水解的化学方程式____ 。
③往冷的NaNO2溶液中加入下列某种物质可得HNO2稀溶液,该物质是____ (填序号)。
a.稀硫酸 b.二氧化碳 c.二氧化硫 d.醋酸
(2)砷化镓(GaAs)是当前最重要,技术成熟度最高的半导体材料之一,我国“玉兔二号”月球车就是通过砷化镓太阳能电池提供能量。基态As原子外围电子排布式为____ ,最高能级的电子云形状为____ ,As元素在元素周期表中的位置为____ 。
(3)GaN是一种直接能隙(directbandgap)的半导体,自1990年起常用在发光二极管中。工业上以镓粉为原料,用镍催化法生产GaN,在氨气流中于1050~1100℃下加热30min可制得疏松的灰色粉末状GaN,同时得到一种单质,请写出对应的化学方程式____ 。
(1)NaNO2是一种重要的化工原料,有毒,NaNO2也是一种食品添加剂,使用时须严格控制用量。已知:HNO2有强氧化性,酸性H2SO3>HNO2>CH3COOH。
①氮原子核外共有
②亚硝酰氯(NOCl)是一种红褐色液体,每个原子最外层都达到8e-结构,则其电子式为
③往冷的NaNO2溶液中加入下列某种物质可得HNO2稀溶液,该物质是
a.稀硫酸 b.二氧化碳 c.二氧化硫 d.醋酸
(2)砷化镓(GaAs)是当前最重要,技术成熟度最高的半导体材料之一,我国“玉兔二号”月球车就是通过砷化镓太阳能电池提供能量。基态As原子外围电子排布式为
(3)GaN是一种直接能隙(directbandgap)的半导体,自1990年起常用在发光二极管中。工业上以镓粉为原料,用镍催化法生产GaN,在氨气流中于1050~1100℃下加热30min可制得疏松的灰色粉末状GaN,同时得到一种单质,请写出对应的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】铬与氮能形成多种化合物,其中氮化铬(CrN)具有高的硬度和良好的耐磨性,是一种很受重视的耐磨涂层。将低碳铬铁在真空加热炉于1150℃氮化得到粗氮化铬铁,再经硫酸处理,除去铁杂质。经过滤、水洗、干燥,即得氮化铬。也可由氨和卤化铬反应制得。
(1)三价铬离子能形成多种配位化合物。 中提供电子对形成配位键的原子是N、O、Cl,配体是NH3、
中提供电子对形成配位键的原子是N、O、Cl,配体是NH3、___________ 和Cl- ,中心离子的配位数为___________ ,N、O、Cl原子半径较大的是___________ ,N和O电负性较大的是___________ ,N和O第一电离能较大的是___________ 。
(2)Cr是24号元素,则基态Cr核外电子排布式为___________ 。
(3) 中心原子轨道的杂化类型为
中心原子轨道的杂化类型为___________ 。
(4)元素As与N同族。预测As的氢化物分子的立体结构为___________ ,其沸点比 的
的___________ (填“高”或“低”),其判断理由___________ 。
(1)三价铬离子能形成多种配位化合物。
 中提供电子对形成配位键的原子是N、O、Cl,配体是NH3、
中提供电子对形成配位键的原子是N、O、Cl,配体是NH3、(2)Cr是24号元素,则基态Cr核外电子排布式为
(3)
 中心原子轨道的杂化类型为
中心原子轨道的杂化类型为(4)元素As与N同族。预测As的氢化物分子的立体结构为
 的
的
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】完成下列问题。
(1)SiCl4是生产高纯硅的前驱体,其中Si采取的杂化类型为___________ 。SiCl4可发生水解反应,机理如下:
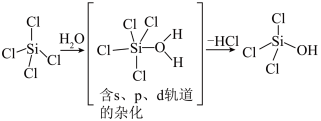
含s、p、d轨道的杂化类型有:①dsp2、②sp3d、③sp3d2,中间体SiCl4(H2O)中Si采取的杂化类型为___________ (填标号)。
(2)PH3中P的杂化类型是___________ 。
(3)N−甲基咪唑(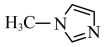 )中碳原子的杂化轨道类型为
)中碳原子的杂化轨道类型为___________ 。
(1)SiCl4是生产高纯硅的前驱体,其中Si采取的杂化类型为

含s、p、d轨道的杂化类型有:①dsp2、②sp3d、③sp3d2,中间体SiCl4(H2O)中Si采取的杂化类型为
(2)PH3中P的杂化类型是
(3)N−甲基咪唑(
 )中碳原子的杂化轨道类型为
)中碳原子的杂化轨道类型为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】阿散酸(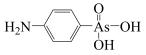 )是一种饲料添加剂,能溶于
)是一种饲料添加剂,能溶于 溶液中,常含有
溶液中,常含有 、
、 等杂质。回答下列问题(用元表符号或化学式表示):
等杂质。回答下列问题(用元表符号或化学式表示):
 在元素周期表中的位置为
在元素周期表中的位置为 原子核外电子占据的最高能级为
原子核外电子占据的最高能级为(2)
 元素的第一电离能
元素的第一电离能 元素的第一电离能,原因是
元素的第一电离能,原因是(3)
 的中心原子的杂化方式为
的中心原子的杂化方式为 的空间构型为
的空间构型为(4)阿散酸分子中C和N的杂化类型分别是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】用VSEPR模型和杂化轨道理论相关知识填表:
| 分子或离子 | 孤电子对数 | 杂化轨道数 | 中心原子杂化轨道类型 | 分子或离子的立体结构 |
| NH3 | ||||
| BeCl2 | ||||
| SO3 | ||||
| SO42- | ||||
| NCl3 |
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】含碳、氮的化合物广泛存在于自然界中。回答下列问题:
(1)Sb和N同族,原子序数为51,基态Sb原子的价电子排布式为___________ 。
(2)在有机反应中有许多活性中间体,如异丁烯与水加成中生成的 ,其中C的轨道杂化方式有
,其中C的轨道杂化方式有___________ , 中C-C间的夹角度数为
中C-C间的夹角度数为___________ 。
(3)成键原子中的孤电子对对键能有影响,现有化合物:① ②
② ③
③ ,其中标出的单键的键能(单位:
,其中标出的单键的键能(单位: )由大到小的顺序为
)由大到小的顺序为___________ ,原因是___________ 。
(4)醋酸(熔点16.6℃)和硝酸(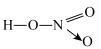 ,熔点-42℃)的相对分子质量接近,但两种物质的熔沸点相差较大,原因是
,熔点-42℃)的相对分子质量接近,但两种物质的熔沸点相差较大,原因是___________ 。
(5) 具有较强的配位能力,能与
具有较强的配位能力,能与 形成一种长链离子,其片段为
形成一种长链离子,其片段为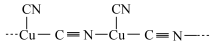 ,该离子的化学式为
,该离子的化学式为___________ 。
(1)Sb和N同族,原子序数为51,基态Sb原子的价电子排布式为
(2)在有机反应中有许多活性中间体,如异丁烯与水加成中生成的
 ,其中C的轨道杂化方式有
,其中C的轨道杂化方式有 中C-C间的夹角度数为
中C-C间的夹角度数为(3)成键原子中的孤电子对对键能有影响,现有化合物:①
 ②
② ③
③ ,其中标出的单键的键能(单位:
,其中标出的单键的键能(单位: )由大到小的顺序为
)由大到小的顺序为(4)醋酸(熔点16.6℃)和硝酸(
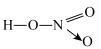 ,熔点-42℃)的相对分子质量接近,但两种物质的熔沸点相差较大,原因是
,熔点-42℃)的相对分子质量接近,但两种物质的熔沸点相差较大,原因是(5)
 具有较强的配位能力,能与
具有较强的配位能力,能与 形成一种长链离子,其片段为
形成一种长链离子,其片段为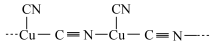 ,该离子的化学式为
,该离子的化学式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】NA为阿伏加德罗常数的值。下列说法正确的是___________ 。
A.1molCHCl3含有C-Cl键的数目为3NA
B.28gC2H4分子中含有的 键数目为4NA
键数目为4NA
C.1mol[Cu(H2O)4]2+中配位键的个数为4NA
D.1molN2中,σ键的数目为3NA
E.3.9gNa2O2中含有的共价键的数目为0.1NA
F.CH2=CH2+H2 CH3CH3,生成1mol乙烷时断裂的共价键总数为NA
CH3CH3,生成1mol乙烷时断裂的共价键总数为NA
G.32g环状S8( )分子中含有的S-S键数为1NA
)分子中含有的S-S键数为1NA
H.1molHC≡CH分子中所含σ键数为5NA
A.1molCHCl3含有C-Cl键的数目为3NA
B.28gC2H4分子中含有的
 键数目为4NA
键数目为4NAC.1mol[Cu(H2O)4]2+中配位键的个数为4NA
D.1molN2中,σ键的数目为3NA
E.3.9gNa2O2中含有的共价键的数目为0.1NA
F.CH2=CH2+H2
 CH3CH3,生成1mol乙烷时断裂的共价键总数为NA
CH3CH3,生成1mol乙烷时断裂的共价键总数为NAG.32g环状S8(
 )分子中含有的S-S键数为1NA
)分子中含有的S-S键数为1NAH.1molHC≡CH分子中所含σ键数为5NA
您最近一年使用:0次



