在周期表中找到第3横行17纵行的元素,回答下列问题:
(1)该元素的符号是________ ,其原子结构示意图为________
(2)该元素位于第________ 周期,第________ 族。
(3)写出下列反应的化学方程式:
①该元素的单质+水:_______________________________________ ;
②该元素的单质+氢氧化钠:_________________________________ 。
(1)该元素的符号是
(2)该元素位于第
(3)写出下列反应的化学方程式:
①该元素的单质+水:
②该元素的单质+氢氧化钠:
更新时间:2018-04-07 10:15:14
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】常温下将Cl2缓慢通入水中至饱和,然后改向其中滴加浓NaOH溶液至恰好完全反应。上述整个实验过程中溶液的pH变化曲线如图所示(不考虑次氯酸的分解以及溶液体积的变化)。
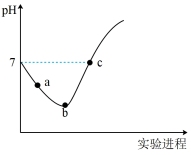
①请对图中pH的整个变化趋势作出解释(用离子方程式表示)________ 。
②写出b点对应溶液中的电荷守恒式___________ 。并且比较c(HClO) :a点___________ b点;c(Cl–):b点___________ c点(填>、<或=)
③Cl2O为淡棕黄色气体,是次氯酸的酸酐,可由新制的HgO和Cl2反应来制备,该反应为歧化反应(氧化剂和还原剂为同一种物质的反应)。上述制备Cl2O的化学方程式为___________ 。
④ClO2常温下为黄色气体,易溶于水,其水溶液是一种广谱杀菌剂。一种有效成分为NaClO2、NaHSO4、NaHCO3的“二氧化氯泡腾片”,能快速溶于水,溢出大量气泡,得到ClO2溶液。上述过程中,生成ClO2的反应属于歧化反应,每生成1mol ClO2消耗NaClO2的量为______ mol; 产生“气泡”的化学方程式为____ 。
⑤“84消毒液“的有效成分为NaClO,不可与酸性清洁剂混用的原因是___________ (用离子方程式表示)。工业上是将氯气通入到30%的NaOH溶液中来制备NaClO溶液,若NaClO溶液中NaOH的质量分数为1%,则生产1000kg该溶液需消耗氯气的质量为 ___________ kg(保留整数)。

①请对图中pH的整个变化趋势作出解释(用离子方程式表示)
②写出b点对应溶液中的电荷守恒式
③Cl2O为淡棕黄色气体,是次氯酸的酸酐,可由新制的HgO和Cl2反应来制备,该反应为歧化反应(氧化剂和还原剂为同一种物质的反应)。上述制备Cl2O的化学方程式为
④ClO2常温下为黄色气体,易溶于水,其水溶液是一种广谱杀菌剂。一种有效成分为NaClO2、NaHSO4、NaHCO3的“二氧化氯泡腾片”,能快速溶于水,溢出大量气泡,得到ClO2溶液。上述过程中,生成ClO2的反应属于歧化反应,每生成1mol ClO2消耗NaClO2的量为
⑤“84消毒液“的有效成分为NaClO,不可与酸性清洁剂混用的原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】饮用水质量是关系人类的重要问题,硫酸铝、活性炭等均为常用的净水剂。回答下列问题:
(1) 中铁元素的化合价是
中铁元素的化合价是___________ 。
(2)以下物质均为常用的净水剂,其中属于盐的是___________ 。
A.氯气 B.次氯酸钙 C.活性炭 D.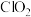 E.
E.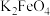
(3)自来水厂净水过程如图所示。
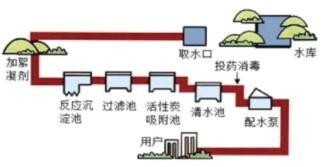
①硫酸铝可用作絮凝剂,其溶于水的电离方程式为___________ 。
②活性炭因其具有___________ 性,用于去除水中的色素和臭味。另有研究表明,活性炭可用于去除水中多余的氯气,反应生成了氯化氢和二氧化碳,写出该反应的化学方程式,并用单线桥法标明电子转移的方向和数目______ ,该反应中体现了活性炭的___________ 性。
③氯气是最早用于饮用水消毒的物质,其在水中发生反应的离子方程式为___________ 。
④二氧化氯是一种广谱杀菌剂,在起消毒作用后以 存在于溶液中。若以
存在于溶液中。若以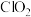 替代
替代 ,提供相同数目的电子,消耗二氧化氯和氯气的物质的量之比为
,提供相同数目的电子,消耗二氧化氯和氯气的物质的量之比为___________ 。
(1)
 中铁元素的化合价是
中铁元素的化合价是(2)以下物质均为常用的净水剂,其中属于盐的是
A.氯气 B.次氯酸钙 C.活性炭 D.
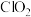 E.
E.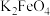
(3)自来水厂净水过程如图所示。

①硫酸铝可用作絮凝剂,其溶于水的电离方程式为
②活性炭因其具有
③氯气是最早用于饮用水消毒的物质,其在水中发生反应的离子方程式为
④二氧化氯是一种广谱杀菌剂,在起消毒作用后以
 存在于溶液中。若以
存在于溶液中。若以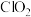 替代
替代 ,提供相同数目的电子,消耗二氧化氯和氯气的物质的量之比为
,提供相同数目的电子,消耗二氧化氯和氯气的物质的量之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】写出下列反应的化学方程式
(1)钠与水反应___________________________________________________________________________________ ;
(2)Na2O2与水反应___________________________________________________________________________________ ;
(3)Cl2与NaOH溶液反应__________________________________________________________________________________ ;
(4)Cl2与水反应___________________________________________________________________________________ 。
(1)钠与水反应
(2)Na2O2与水反应
(3)Cl2与NaOH溶液反应
(4)Cl2与水反应
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】写出下列反应的化学方程式,是离子反应的写离子方程式
(1)工业上制备氨气反应的化学方程式___________
(2)铜和浓硫酸发生反应的化学方程式___________
(3)氨气催化氧化生成一氧化氮的化学方程式___________
(4)工业上制备漂白液发生反应的离子方程式___________
(5)将亚硫酸钠溶液滴入酸性高锰酸钾溶液中发生反应的离子方程式___________
(1)工业上制备氨气反应的化学方程式
(2)铜和浓硫酸发生反应的化学方程式
(3)氨气催化氧化生成一氧化氮的化学方程式
(4)工业上制备漂白液发生反应的离子方程式
(5)将亚硫酸钠溶液滴入酸性高锰酸钾溶液中发生反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】写出下列反应的离子方程式。
(1)硫酸溶液与金属锌的反应___ ;
(2)CuSO4溶液中加入Ba(OH)2溶液___ ;
(3)盐酸溶液与氧化钙的反应___ ;
(4)钠与水的反应___ ;
(5)氯气与NaOH溶液的反应___ ;
(6)CO2通入澄清石灰水使石灰水变浑浊___ 。
(1)硫酸溶液与金属锌的反应
(2)CuSO4溶液中加入Ba(OH)2溶液
(3)盐酸溶液与氧化钙的反应
(4)钠与水的反应
(5)氯气与NaOH溶液的反应
(6)CO2通入澄清石灰水使石灰水变浑浊
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】疫情期间,环境消毒是极其关键的,常常喷洒“84”消毒液,其有效成分为NaClO。已知某“84”消毒液瓶体部分标签如图所示。请回答下列问题:

(1)Cl2是制取“84”消毒液的主要原料之一,请写出实验室用MnO2制Cl2的化学方程式:__ ,工业上将Cl2通入NaOH溶液中可制得“84”消毒液,请写出该反应的化学方程式:__ 。
(2)该同学参阅该“84”消毒液的配方,欲用NaClO固体配制480mL此消毒液。

①配制过程中使用的玻璃仪器有烧杯、玻璃棒、胶头滴管、量筒、__ 。
②关于配制过程的说法正确的是__ (填字母)。
A.容量瓶用蒸馏水洗净后,必须烘干后才能用于溶液配制
B..配制过程中,未用蒸馏水洗涤烧杯和玻璃棒会导致结果偏低
C.需要称量NaClO固体的质量为148.8g
D.将称量NaClO固体完全溶于水后,直接将溶液转移至如图仪器中
E.按如图所示转移烧杯中的溶液,对所配溶液浓度无影响
F.定容时,俯视观察刻度线可能导致结果偏高
G.称量时,所使用的砝码有残缺可能导致结果偏高
(3)曾有报道,在清洗卫生间时,因混合使用“洁厕灵”(主要成分是盐酸)与“84”消毒液而发生氯气中毒事件。请用离子方程式解释原因:__ 。
(4)2016年巴西奥运会期间,由于工作人员将“84”消毒液与双氧水两种消毒剂混用,导致游泳池藻类快速生长,池水变绿。一种可能的原因是NaClO与H2O2反应产生O2促进藻类快速生长。在此过程中H2O2表现了__ (填“氧化性”或“还原性”),当有0.1molO2生成时,转移电子__ mol。

(1)Cl2是制取“84”消毒液的主要原料之一,请写出实验室用MnO2制Cl2的化学方程式:
(2)该同学参阅该“84”消毒液的配方,欲用NaClO固体配制480mL此消毒液。

①配制过程中使用的玻璃仪器有烧杯、玻璃棒、胶头滴管、量筒、
②关于配制过程的说法正确的是
A.容量瓶用蒸馏水洗净后,必须烘干后才能用于溶液配制
B..配制过程中,未用蒸馏水洗涤烧杯和玻璃棒会导致结果偏低
C.需要称量NaClO固体的质量为148.8g
D.将称量NaClO固体完全溶于水后,直接将溶液转移至如图仪器中
E.按如图所示转移烧杯中的溶液,对所配溶液浓度无影响
F.定容时,俯视观察刻度线可能导致结果偏高
G.称量时,所使用的砝码有残缺可能导致结果偏高
(3)曾有报道,在清洗卫生间时,因混合使用“洁厕灵”(主要成分是盐酸)与“84”消毒液而发生氯气中毒事件。请用离子方程式解释原因:
(4)2016年巴西奥运会期间,由于工作人员将“84”消毒液与双氧水两种消毒剂混用,导致游泳池藻类快速生长,池水变绿。一种可能的原因是NaClO与H2O2反应产生O2促进藻类快速生长。在此过程中H2O2表现了
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】下表为元素周期表的一部分,请回答有关问题:
(1)⑧的元素符号是_____________ ;⑤号元素最高价氧化物对应的水化物为_____________ (写出化学式);
(2)表中原子半径最大的元素是_____________ ;非金属性最强的元素是_____________ ;(填元素符号)
(3)表中能形成两性氢氧化物的元素是_____________ (填写元素符号);写出该氢氧化物与⑥的最高价氧化物对应水化物反应的化学方程式:________________________________________ ;
(4)⑥、⑦、⑨三种元素的简单离子的半径大小顺序为_____________ (用“>”连接离子符号);
(5)工业上从海水大规模提取元素⑩的单质X的常用方法,流程如下:

分别写出流程a和c中发生的离子方程式:_____________________ 、_____________________ .
(6)用 从水溶液中提取⑩的单质X所使用的操作是
从水溶液中提取⑩的单质X所使用的操作是_____________ .
|
|
|
|
|
|
| 0 | |
2 | ① | ② | ||||||
3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
4 | ⑨ | ⑩ |
(1)⑧的元素符号是
(2)表中原子半径最大的元素是
(3)表中能形成两性氢氧化物的元素是
(4)⑥、⑦、⑨三种元素的简单离子的半径大小顺序为
(5)工业上从海水大规模提取元素⑩的单质X的常用方法,流程如下:

分别写出流程a和c中发生的离子方程式:
(6)用
 从水溶液中提取⑩的单质X所使用的操作是
从水溶液中提取⑩的单质X所使用的操作是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】(1)已知某粒子的结构示意图为: 。请回答:
。请回答:
①当x−y=10时,该粒子为________ (填“原子”、“阳离子”或“阴离子”)。
②当y=8时,阳离子可能为(填离子符号)________ 、________ 。
(2)原子序数大于4的主族元素A和B的离子Am+和Bn−它们的核外电子排布相同,据此推断:元素A和B所属周期序数之差为________ ;元素A和B的原子序数之差为________ 。
 。请回答:
。请回答:①当x−y=10时,该粒子为
②当y=8时,阳离子可能为(填离子符号)
(2)原子序数大于4的主族元素A和B的离子Am+和Bn−它们的核外电子排布相同,据此推断:元素A和B所属周期序数之差为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】如图是元素周期表的草图,表中所列字母代号分别代表某一种元素,请回答:

(1)表中最活泼的金属元素与最活泼的非金属元素形成的物质是___ (化学式),其中所含化学键类型为___ (填“离子键”或“共价键”)。
(2)a、d两种元素可形成两种化合物,其中原子个数比为1:1的化合物的结构式为___ 。
(3)e、f、k、m对应的单原子离子的半径由大到小的顺序为___ (填离子符号)。
(4)d、m对应的阴离子还原性由强到弱顺序为___ (填离子符号)。
(5)用电子式表示n与m形成的原子个数比2:1的化合物的形成过程:___ 。
(6)写出k的最高价氧化物对应的水化物与f的最高价氧化物对应的水化物反应的离子方程式:___ 。

(1)表中最活泼的金属元素与最活泼的非金属元素形成的物质是
(2)a、d两种元素可形成两种化合物,其中原子个数比为1:1的化合物的结构式为
(3)e、f、k、m对应的单原子离子的半径由大到小的顺序为
(4)d、m对应的阴离子还原性由强到弱顺序为
(5)用电子式表示n与m形成的原子个数比2:1的化合物的形成过程:
(6)写出k的最高价氧化物对应的水化物与f的最高价氧化物对应的水化物反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】 、
、 、
、 、
、 、
、 代表
代表 种短周期元素,已知
种短周期元素,已知 、
、 、
、 处于相邻位置,
处于相邻位置, 、
、 同周期,
同周期, 、
、 同主族,其核外电子数之和为
同主族,其核外电子数之和为 、
、 为同一周期,
为同一周期,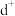 中各层电子数都是
中各层电子数都是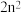 个,
个, 、
、 、
、 、
、 、
、 各元素最外层电子数和为
各元素最外层电子数和为 ,已知
,已知 和
和 形成
形成 种化合物
种化合物_______ 。
 、
、 、
、 、
、 、
、 代表
代表 种短周期元素,已知
种短周期元素,已知 、
、 、
、 处于相邻位置,
处于相邻位置, 、
、 同周期,
同周期, 、
、 同主族,其核外电子数之和为
同主族,其核外电子数之和为 、
、 为同一周期,
为同一周期,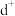 中各层电子数都是
中各层电子数都是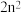 个,
个, 、
、 、
、 、
、 、
、 各元素最外层电子数和为
各元素最外层电子数和为 ,已知
,已知 和
和 形成
形成 种化合物
种化合物
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】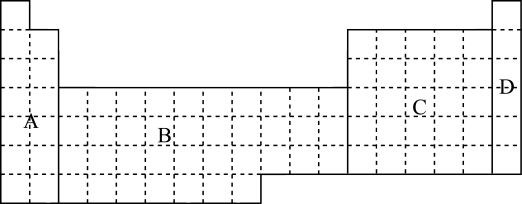
(1)在上面元素周期表中全部是金属元素的区域为____ 。
A B C D
(2)有人认为形成化合物最多的元素不是IVA族的碳元素,而是另一种短周期元素,请你根据学过的化学知识判断这一元素是____ (写出元素符号)。
(3)现有甲、乙两种短周期元素,室温下,甲元素单质在冷的浓硫酸或空气中,表面都生成致密的氧化膜,乙元素原子核外M电子层与K电子层上的电子数相等。
①画出甲原子的基态外围电子轨道表示式:_____ 。
② 甲、乙两元素相比较,金属性较强的是____ (填名称),可以验证该结论的实验是__ 。
A 将在空气中放置已久的这两种元素的块状单质分别放入热水中
B 将这两种元素的单质粉末分别和同浓度的盐酸反应
C 将这两种元素的单质粉末分别和热水作用,并滴入酚酞溶液
D 比较这两种元素的气态氢化物的稳定性
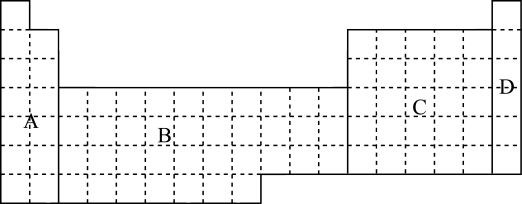
(1)在上面元素周期表中全部是金属元素的区域为
A B C D
(2)有人认为形成化合物最多的元素不是IVA族的碳元素,而是另一种短周期元素,请你根据学过的化学知识判断这一元素是
(3)现有甲、乙两种短周期元素,室温下,甲元素单质在冷的浓硫酸或空气中,表面都生成致密的氧化膜,乙元素原子核外M电子层与K电子层上的电子数相等。
①画出甲原子的基态外围电子轨道表示式:
② 甲、乙两元素相比较,金属性较强的是
A 将在空气中放置已久的这两种元素的块状单质分别放入热水中
B 将这两种元素的单质粉末分别和同浓度的盐酸反应
C 将这两种元素的单质粉末分别和热水作用,并滴入酚酞溶液
D 比较这两种元素的气态氢化物的稳定性
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】铁及其化合物在生产和生活中有着广泛的应用。
(1)铁元素在元素周期表中的位置为_____ 。
(2)等物质的量的铁分别与足量的盐酸、水蒸气在一定条件下反应,产生相同条件下的气体体积比为_____ ,铁在高温条件下与水蒸气反应的化学方程式为______________ 。
(3)高铁酸钾(K2FeO4)也是常用的水处理剂。它的制备方法有多种:其中熔融法又称为过氧化钠氧化法。先在高温熔融的条件下制备高铁酸钠:Fe+3Na2O2 Na2FeO4+2Na2O,再将高铁酸钠加入到氢氧化钾溶液里,发生反应:2KOH+Na2FeO4=K2FeO4+2NaOH,请根据复分解反应原理分析该反应发生的原因:
Na2FeO4+2Na2O,再将高铁酸钠加入到氢氧化钾溶液里,发生反应:2KOH+Na2FeO4=K2FeO4+2NaOH,请根据复分解反应原理分析该反应发生的原因:_______________________________________ 。
(1)铁元素在元素周期表中的位置为
(2)等物质的量的铁分别与足量的盐酸、水蒸气在一定条件下反应,产生相同条件下的气体体积比为
(3)高铁酸钾(K2FeO4)也是常用的水处理剂。它的制备方法有多种:其中熔融法又称为过氧化钠氧化法。先在高温熔融的条件下制备高铁酸钠:Fe+3Na2O2
 Na2FeO4+2Na2O,再将高铁酸钠加入到氢氧化钾溶液里,发生反应:2KOH+Na2FeO4=K2FeO4+2NaOH,请根据复分解反应原理分析该反应发生的原因:
Na2FeO4+2Na2O,再将高铁酸钠加入到氢氧化钾溶液里,发生反应:2KOH+Na2FeO4=K2FeO4+2NaOH,请根据复分解反应原理分析该反应发生的原因:
您最近一年使用:0次