常温下将Cl2缓慢通入水中至饱和,然后改向其中滴加浓NaOH溶液至恰好完全反应。上述整个实验过程中溶液的pH变化曲线如图所示(不考虑次氯酸的分解以及溶液体积的变化)。
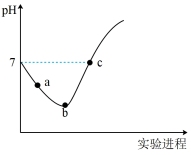
①请对图中pH的整个变化趋势作出解释(用离子方程式表示)________ 。
②写出b点对应溶液中的电荷守恒式___________ 。并且比较c(HClO) :a点___________ b点;c(Cl–):b点___________ c点(填>、<或=)
③Cl2O为淡棕黄色气体,是次氯酸的酸酐,可由新制的HgO和Cl2反应来制备,该反应为歧化反应(氧化剂和还原剂为同一种物质的反应)。上述制备Cl2O的化学方程式为___________ 。
④ClO2常温下为黄色气体,易溶于水,其水溶液是一种广谱杀菌剂。一种有效成分为NaClO2、NaHSO4、NaHCO3的“二氧化氯泡腾片”,能快速溶于水,溢出大量气泡,得到ClO2溶液。上述过程中,生成ClO2的反应属于歧化反应,每生成1mol ClO2消耗NaClO2的量为______ mol; 产生“气泡”的化学方程式为____ 。
⑤“84消毒液“的有效成分为NaClO,不可与酸性清洁剂混用的原因是___________ (用离子方程式表示)。工业上是将氯气通入到30%的NaOH溶液中来制备NaClO溶液,若NaClO溶液中NaOH的质量分数为1%,则生产1000kg该溶液需消耗氯气的质量为 ___________ kg(保留整数)。

①请对图中pH的整个变化趋势作出解释(用离子方程式表示)
②写出b点对应溶液中的电荷守恒式
③Cl2O为淡棕黄色气体,是次氯酸的酸酐,可由新制的HgO和Cl2反应来制备,该反应为歧化反应(氧化剂和还原剂为同一种物质的反应)。上述制备Cl2O的化学方程式为
④ClO2常温下为黄色气体,易溶于水,其水溶液是一种广谱杀菌剂。一种有效成分为NaClO2、NaHSO4、NaHCO3的“二氧化氯泡腾片”,能快速溶于水,溢出大量气泡,得到ClO2溶液。上述过程中,生成ClO2的反应属于歧化反应,每生成1mol ClO2消耗NaClO2的量为
⑤“84消毒液“的有效成分为NaClO,不可与酸性清洁剂混用的原因是
更新时间:2021-01-03 09:54:47
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】实验室有甲、乙两瓶丢失标签的无色溶液,其中一瓶是盐酸,另一瓶是碳酸钠溶液。为确定甲、乙两瓶溶液的成分及其物质的量浓度,现操作如下:
①量取50.00mL甲溶液,向其中缓慢滴加乙溶液20.00mL,共收集到二氧化碳气体560mL。
②另取20.00mL乙溶液,向其中缓慢滴加甲溶液50.00mL,共收集到二氧化碳气体224mL。
上述气体体积均已换算为标准状况,则根据上述操述及实验数据填空:乙是___________ ,甲溶液的物质的量浓度为___________ ,乙溶液的物质的量浓度为___________ 。(二氧化碳在溶液中的少量溶解忽略不计)
①量取50.00mL甲溶液,向其中缓慢滴加乙溶液20.00mL,共收集到二氧化碳气体560mL。
②另取20.00mL乙溶液,向其中缓慢滴加甲溶液50.00mL,共收集到二氧化碳气体224mL。
上述气体体积均已换算为标准状况,则根据上述操述及实验数据填空:乙是
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】如图为电解水的简易装置图:
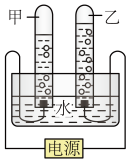
(1)甲试管收集到的气体为_______ ,乙试管收集到的气体为_______ ,在同温同压下,收集到的氢气与氧气的体积比为_______ ;
(2)写出电解水的化学方程式_______ ,该反应中参加反应的H2、O2、H2O的物质的量之比为_______ ,若有1mol的水参与反应,则生成的H2在标准状况下的体积为_______ 。

(1)甲试管收集到的气体为
(2)写出电解水的化学方程式
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】I.20mL0.1mol/LBaCl2溶液中Cl-的物质的量浓度为________ ,Ba2+的物质的量为_______ 。
II.把5.1g镁铝合金的粉末放入过量的盐酸中,得到5.6 LH2(标准状况下)。
(1)合金中镁的物质的量_________ 。
(2)写出该合金溶于足量NaOH溶液的化学方程式_________ 。同时产生H2的体积(标准状况下)为____________ 。
III.在一定质量的AlCl3和MgCl2混合溶液中逐渐滴入一定溶质质量分数的NaOH溶液,生成沉淀的物质的量与加入NaOH的物质的量的关系如图所示,则:
①生成Mg(OH)2的质量为__________ ;
②X=_______ ;Y=_________ 。
II.把5.1g镁铝合金的粉末放入过量的盐酸中,得到5.6 LH2(标准状况下)。
(1)合金中镁的物质的量
(2)写出该合金溶于足量NaOH溶液的化学方程式
III.在一定质量的AlCl3和MgCl2混合溶液中逐渐滴入一定溶质质量分数的NaOH溶液,生成沉淀的物质的量与加入NaOH的物质的量的关系如图所示,则:
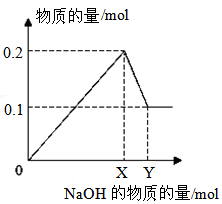
①生成Mg(OH)2的质量为
②X=
您最近半年使用:0次
填空题
|
适中
(0.64)
【推荐1】某化学反应的反应物和产物如下:Al+NaNO3+H2O→Al(OH)3+N2+NaAlO2
(1)该反应的氧化剂是______ 。
(2)该反应的氧化产物是______ 。
(3)反应过程中转移5 mol e-,生成标准状况下N2的体积______ L。
(4)配平该反应的化学方程式:______
______Al+______NaNO3+______H2O=______Al(OH)3+______N2+______NaAlO2
(1)该反应的氧化剂是
(2)该反应的氧化产物是
(3)反应过程中转移5 mol e-,生成标准状况下N2的体积
(4)配平该反应的化学方程式:
______Al+______NaNO3+______H2O=______Al(OH)3+______N2+______NaAlO2
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】工业上高炉炼铁时常用赤铁矿和焦炭(主要成分为碳)为原料,而将赤铁矿中的三氧化二铁转化为铁的过程中实际起作用的是一氧化碳。
(1)请分析高炉炼铁过程中碳元素的转化过程,以及含有碳元素的物质在转化过程中的作用_____ 。
(2)如图是高炉炼铁流程示意图,请分析其中的化学变化,判断哪些是氧化还原反应_____ 。在这些氧化还原反应中,分析哪种物质是氧化剂、哪种物质是还原剂_____ 。任选其中的两个氧化还原反应,分析电子转移情况_____ 。
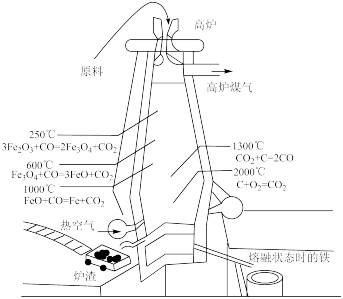
(1)请分析高炉炼铁过程中碳元素的转化过程,以及含有碳元素的物质在转化过程中的作用
(2)如图是高炉炼铁流程示意图,请分析其中的化学变化,判断哪些是氧化还原反应

您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】亚硝酸(HNO2)是一种弱酸,且不稳定,易分解生成NO气体和NO2(红棕色)气体;亚硝酸是一种还原剂,能被常见的强氧化剂氧化,但在酸性溶液中它也是一种氧化剂,如能把Fe2+(浅绿色)氧化成Fe3+(棕黄色);AgNO2是一种难溶于水(白色)、易溶于酸的化合物。请仔细阅读以上信息,并结合有关原理回答以下问题:
(1)人体正常的血红蛋白含有Fe2+,若误食亚硝酸盐(如NaNO2),则导致血红蛋白中的Fe2+转换为Fe3+ 而中毒,可以服用维生素C解毒。下列对此过程 中叙述不正确的是______ (填选项)。
a.亚硝酸盐被还原 b. 亚硝酸盐是还原剂
c.维生素C将Fe3+还原为Fe2+ d. 维生素C被氧化
(2)NaNO2能和HI发生反应:2NaNO2 + 4HI = 2NO↑ + I2 + 2NaI + 2H2O,若有1.2mol还原剂被氧化,则消耗氧化剂___________ mol,该过程中转移的电子为___________ mol。
(3)下列方法中,不能用来区别NaNO2和NaCl的是_______ (填选项)。
a.取样加水溶解后,向其中加入稀硫酸
b.取样加水溶解后,向其中加入AgNO3溶液
c.取样加水溶解后,向其中加入稀硫酸酸化的KI-淀粉溶液
(4)某同学把氯气通入到NaNO2溶液中,生成NaNO3和HCl,请写出该反应的离子方程式:________________________________________________________ 。
(5)工业废水中的NO2- 可用铝粉除去。已知此反应体系中包含Al、NaOH、NaAlO2、NaNO2、NH3和H2O六种物质,该反应的化学方程式为:______________________________________ 。
(1)人体正常的血红蛋白含有Fe2+,若误食亚硝酸盐(如NaNO2),则导致血红蛋白中的Fe2+转换为Fe3+ 而中毒,可以服用维生素C解毒。下列对
a.亚硝酸盐被还原 b. 亚硝酸盐是还原剂
c.维生素C将Fe3+还原为Fe2+ d. 维生素C被氧化
(2)NaNO2能和HI发生反应:2NaNO2 + 4HI = 2NO↑ + I2 + 2NaI + 2H2O,若有1.2mol还原剂被氧化,则消耗氧化剂
(3)下列方法中,不能用来区别NaNO2和NaCl的是
a.取样加水溶解后,向其中加入稀硫酸
b.取样加水溶解后,向其中加入AgNO3溶液
c.取样加水溶解后,向其中加入稀硫酸酸化的KI-淀粉溶液
(4)某同学把氯气通入到NaNO2溶液中,生成NaNO3和HCl,请写出该反应的离子方程式:
(5)工业废水中的NO2- 可用铝粉除去。已知此反应体系中包含Al、NaOH、NaAlO2、NaNO2、NH3和H2O六种物质,该反应的化学方程式为:
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐1】写出下列反应的化学方程式
(1)钠与水反应___________________________________________________________________________________ ;
(2)Na2O2与水反应___________________________________________________________________________________ ;
(3)Cl2与NaOH溶液反应__________________________________________________________________________________ ;
(4)Cl2与水反应___________________________________________________________________________________ 。
(1)钠与水反应
(2)Na2O2与水反应
(3)Cl2与NaOH溶液反应
(4)Cl2与水反应
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】按要求填空:
现有以下物质:①石墨;②铝;③乙醇;④氨气;⑤液氯;⑥碳酸氢钠固体;⑦氢氧化钡溶液;⑧纯醋酸;⑨氢氧化钠固体。
(1)属于电解质的是___________ (填写序号)。
(2)写出物质⑤在水中反应的离子方程式:___________ 。
(3)40.5g某金属氯化物MCl2中含有0.6molCl-,则该氯化物的摩尔质量为___________ 。
(4)标准状况下,体积为11.2LCO2与足量Na2O2反应,生成气体的体积为___________ L,反应转移电子数为___________ (用NA表示),Na2O2中阴、阳离子个数比为___________ 。
(5)已知P2O5为酸性氧化物,可与水反应生成磷酸(H3PO4),写出P2O5与足量NaOH溶液反应的离子方程式:___________ 。
现有以下物质:①石墨;②铝;③乙醇;④氨气;⑤液氯;⑥碳酸氢钠固体;⑦氢氧化钡溶液;⑧纯醋酸;⑨氢氧化钠固体。
(1)属于电解质的是
(2)写出物质⑤在水中反应的离子方程式:
(3)40.5g某金属氯化物MCl2中含有0.6molCl-,则该氯化物的摩尔质量为
(4)标准状况下,体积为11.2LCO2与足量Na2O2反应,生成气体的体积为
(5)已知P2O5为酸性氧化物,可与水反应生成磷酸(H3PO4),写出P2O5与足量NaOH溶液反应的离子方程式:
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】A、B、C、D、E是高中阶段学习的常见单质或化合物,单质A在单质B中燃烧产生苍白色的火焰,产物溶于水得到常见的强酸。化合物C具有强氧化性、漂白性,是单质B与水反应的产物之一、化合物D是淡黄色物质,可用于呼吸面具,可由一种活泼金属E在氧气中燃烧得到。回答问题:
(1)物质C的名称为_______ ,化合物D中非金属元素的化合价为_______ 。
(2)单质A在单质B中燃烧的化学方程式为_______ 。
(3)单质B与水反应的化学方程式为_______ 。
(4)化合物D与水反应的化学方程式为_______ 。
(1)物质C的名称为
(2)单质A在单质B中燃烧的化学方程式为
(3)单质B与水反应的化学方程式为
(4)化合物D与水反应的化学方程式为
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】将一定量 通入1kg质量分数为
通入1kg质量分数为 的
的 溶液中,制成含有
溶液中,制成含有 、
、 和
和 的混合溶液。用此溶液吸收标准状况下
的混合溶液。用此溶液吸收标准状况下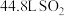 ,恰好形成中性溶液(假设气体均完全反应),请计算:
,恰好形成中性溶液(假设气体均完全反应),请计算:
(1)原 溶液中
溶液中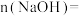
_______  。
。
(2)所通 在标准状况下的体积为
在标准状况下的体积为_______ L。
 通入1kg质量分数为
通入1kg质量分数为 的
的 溶液中,制成含有
溶液中,制成含有 、
、 和
和 的混合溶液。用此溶液吸收标准状况下
的混合溶液。用此溶液吸收标准状况下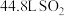 ,恰好形成中性溶液(假设气体均完全反应),请计算:
,恰好形成中性溶液(假设气体均完全反应),请计算:(1)原
 溶液中
溶液中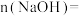
 。
。(2)所通
 在标准状况下的体积为
在标准状况下的体积为
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】利用图,可以从不同角度研究含氯物质的性质及其转化关系,图中甲~辛均含氯元素。回答下列问题:

(1)丙的化学式为______ ;丁属于______ (“酸性”或“碱性”)氧化物。
(2)图中甲、乙、丁、戊中,属于电解质的是_____ (填化学式);根据氯元素的化合价判断,乙物质的性质______ (填标号)。
a.只有氧化性 b.既有氧化性又有还原性 c.只有还原性
(3)物质己的化学式为HClO4,电解甲溶液制备己的化学反应为:甲+H2O 己+H2↑(未配平),配平后参与反应的甲与H2O的微粒个数之比是
己+H2↑(未配平),配平后参与反应的甲与H2O的微粒个数之比是_____ 。
(4)庚是家庭中常用消毒液的有效成分NaClO,用乙制取庚的化学方程式为_____ 。NaClO溶液中显碱性原因:______ (用离子方程式表示)。
(5)辛在MnO2催化下受热分解可用于制备氧气,每生成1.204×1024氧气分子,转移e-的个数为______ 。

(1)丙的化学式为
(2)图中甲、乙、丁、戊中,属于电解质的是
a.只有氧化性 b.既有氧化性又有还原性 c.只有还原性
(3)物质己的化学式为HClO4,电解甲溶液制备己的化学反应为:甲+H2O
 己+H2↑(未配平),配平后参与反应的甲与H2O的微粒个数之比是
己+H2↑(未配平),配平后参与反应的甲与H2O的微粒个数之比是(4)庚是家庭中常用消毒液的有效成分NaClO,用乙制取庚的化学方程式为
(5)辛在MnO2催化下受热分解可用于制备氧气,每生成1.204×1024氧气分子,转移e-的个数为
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】判断下列正误:
(1)将氯水滴入Na2CO3溶液中有气泡产生______ 。
(2)铁丝在Cl2中燃烧,产生棕褐色的烟。______ 。
(3)钠在Cl2中燃烧,生成白色的雾。______ 。
(4)铜丝在Cl2中燃烧,生成棕黄色的烟。______ 。
(5)可将氯气与氢气混合光照制备氯化氢。______ 。
(6)实验室制氯气时,为了防止环境污染,多余氯气用氢氧化钙溶液吸收。______ 。
(7)向久置的氯水中滴入紫色石蕊试液,溶液将先变红后褪色。______ 。
(8)检验HCl气体中是否混有Cl2的方法是将气体通入硝酸银溶液。______ 。
(9)除去CO2中的HCl,可使气体通过饱和碳酸氢钠溶液。______ 。
(10))在含有NaOH的酚酞试液中加入新制氯水,红色褪去,说明氯水中含有HClO。______ 。
(1)将氯水滴入Na2CO3溶液中有气泡产生
(2)铁丝在Cl2中燃烧,产生棕褐色的烟。
(3)钠在Cl2中燃烧,生成白色的雾。
(4)铜丝在Cl2中燃烧,生成棕黄色的烟。
(5)可将氯气与氢气混合光照制备氯化氢。
(6)实验室制氯气时,为了防止环境污染,多余氯气用氢氧化钙溶液吸收。
(7)向久置的氯水中滴入紫色石蕊试液,溶液将先变红后褪色。
(8)检验HCl气体中是否混有Cl2的方法是将气体通入硝酸银溶液。
(9)除去CO2中的HCl,可使气体通过饱和碳酸氢钠溶液。
(10))在含有NaOH的酚酞试液中加入新制氯水,红色褪去,说明氯水中含有HClO。
您最近半年使用:0次



