下列原子或离子的电子排布式或排布图正确的是________ (填序号,下同),违反能量最低原理的是____________ ,违反洪特规则的是________ ,违反泡利原理的是________ 。
①Ca2+:1s22s22p63s23p6 ②F-:1s22s23p6
③P: ④Cr:1s22s22p63s23p63d44s2
④Cr:1s22s22p63s23p63d44s2
⑤Fe:1s22s22p63s23p63d64s2 ⑥Mg2+:1s22s22p6⑦C: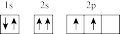
①Ca2+:1s22s22p63s23p6 ②F-:1s22s23p6
③P:
 ④Cr:1s22s22p63s23p63d44s2
④Cr:1s22s22p63s23p63d44s2⑤Fe:1s22s22p63s23p63d64s2 ⑥Mg2+:1s22s22p6⑦C:
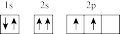
更新时间:2018-02-11 15:33:23
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】推导下列元素,回答有关问题:
(1)具有1个4p电子的元素为________ (写元素名称,下同),简化电子排布式为________ 。
(2)N层只有1个电子的主族元素是________ ,其氯化物的焰色反应呈________ 色,其原子核外有________ 种不同运动状态的电子。
(3)3d能级全充满,4s能级只有1个电子的元素为________ ,原子序数为________ 。
(4)离子M2+的3d轨道中有5个电子,则M原子的最外层电子数和未成对电子数分别为_____ 和___ 。
(5)原子序数小于36的元素X和Y,在周期表中既处于同一周期又位于同一族,且Y的原子序数比X大2,则Y的基态原子的价电子排布式是____ ,X在参与化学反应时,1个原子失去的电子数为_____ 。
(1)具有1个4p电子的元素为
(2)N层只有1个电子的主族元素是
(3)3d能级全充满,4s能级只有1个电子的元素为
(4)离子M2+的3d轨道中有5个电子,则M原子的最外层电子数和未成对电子数分别为
(5)原子序数小于36的元素X和Y,在周期表中既处于同一周期又位于同一族,且Y的原子序数比X大2,则Y的基态原子的价电子排布式是
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
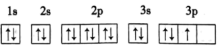
【推荐2】下列基态原子或离子的电子排布式或轨道表示式正确的是___________ (填序号,下同),违反能量最低原理的是___________ ,违反洪特规则的是___________ ,违反泡利原理的是___________ 。
① :
: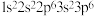
② :
: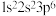
③ :
:
④ :
: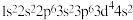
⑤ :
:
⑥ :
: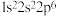
⑦ :
: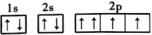
①
 :
: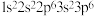
②
 :
: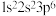
③
 :
:
④
 :
: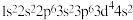
⑤
 :
:
⑥
 :
: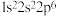
⑦
 :
: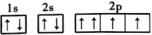
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】按要求填空:
(1)元素周期表中,电负性最大的元素是___ (填元素符号),其氢化物为___ 酸(填“强”、“中强”“弱”)。
(2)以下是一些原子的2p能级和3d能级中电子排布的情况。试判断,哪些违反了泡利不相容原理,哪些违反了洪特规则。
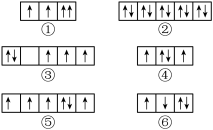
违反泡利不相容原理的有___ (填序号,下同),违反洪特规则的有___ 。
(3)海洋是元素的摇篮,海水中含有大量卤族元素。根据价层电子对互斥理论,预测ClO 的VSEPR模型
的VSEPR模型___ 形,空间构型为___ 形。
(1)元素周期表中,电负性最大的元素是
(2)以下是一些原子的2p能级和3d能级中电子排布的情况。试判断,哪些违反了泡利不相容原理,哪些违反了洪特规则。

违反泡利不相容原理的有
(3)海洋是元素的摇篮,海水中含有大量卤族元素。根据价层电子对互斥理论,预测ClO
 的VSEPR模型
的VSEPR模型
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】下列基态原子或离子的电子排布式或轨道表示式正确的是___________ (填序号,下同),违反能量最低原理的是___________ ,违反洪特规则的是___________ ,违反泡利原理的是___________ 。
① :
: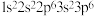
② :
: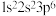
③ :
:
④ :
: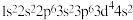
⑤ :
:
⑥ :
: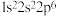
⑦ :
: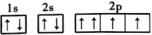
①
 :
: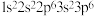
②
 :
: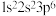
③
 :
:
④
 :
: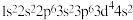
⑤
 :
:
⑥
 :
: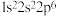
⑦
 :
: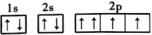
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】过渡金属元素在工农业生产和国防建设中有着广泛应用。回答下列问题:
(1)原子序数为21~30的元素基态原子中,未成对电子数最多的和成对电子数最多的元素在周期表中的位置分别是___________ 和___________ ,其价层电子排布图(轨道表示式)为___________ 与___________
(2)基态钒原子核外电子的运动状态有___________ 种。
(3)根据原子结构、元素周期表和元素周期律的知识回答下列问题:
A元素M层电子数是N电子数7倍,其价层电子轨道表示式___________ 。
(4)C元素基态原子的轨道表示式是下图中的___________ (填“①”或“②”),另一轨道表示式不能作为基态原子的轨道表示式是因为它不符合___________ (填“A”“B”或“C”)。
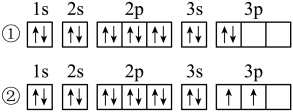
A.能量最低原理 B.泡利原理 C.洪特规则
(5)第三周期元素的气态电中性基态原子失去最外层一个电子转化为气态基态正离子所需的最低能量叫作第一电离能(设为E)。如图所示:
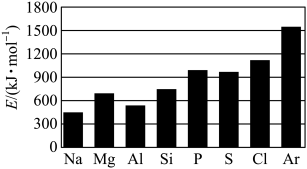
①同周期内,随着原子序数的增大,E值变化的总趋势是___________ ;
②根据图中提供的信息,可推断出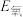
___________ 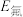 (填“>”“<”或“=”,下同);
(填“>”“<”或“=”,下同);
③根据第一电离能的含义和元素周期律,可推断出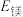
___________ 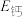 。
。
(1)原子序数为21~30的元素基态原子中,未成对电子数最多的和成对电子数最多的元素在周期表中的位置分别是
(2)基态钒原子核外电子的运动状态有
(3)根据原子结构、元素周期表和元素周期律的知识回答下列问题:
A元素M层电子数是N电子数7倍,其价层电子轨道表示式
(4)C元素基态原子的轨道表示式是下图中的

A.能量最低原理 B.泡利原理 C.洪特规则
(5)第三周期元素的气态电中性基态原子失去最外层一个电子转化为气态基态正离子所需的最低能量叫作第一电离能(设为E)。如图所示:

①同周期内,随着原子序数的增大,E值变化的总趋势是
②根据图中提供的信息,可推断出
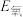
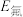 (填“>”“<”或“=”,下同);
(填“>”“<”或“=”,下同);③根据第一电离能的含义和元素周期律,可推断出
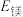
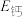 。
。
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】根据已学知识,请你回答下列问题:
(1)写出原子序数最小的第Ⅷ族元素原子的原子结构示意图__________ 。
(2)写出3p轨道上有2个未成对电子的元素的符号:______________ 。
(3)该元素被科学家称之为人体微量元素中的“防癌之王”,其原子的外围电子排布式为4s24p4,该元素的名称是____________ 。
(4)NH4BF4(氟硼酸铵)是合成氮化硼纳米管的原料之一。1 mol NH4BF4含有____ mol配位键。
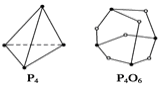
(5)化学反应可视为旧键的断裂和新键的形成过程。化学键的键能是形成化学键时释放的能量。已知白磷和P4O6的分子结构如图所示,现提供以下化学键的键能(kJ·mol-1):P—P:198 P—O:360 O===O:498,则反应P4(白磷)+3O2===P4O6的反应热ΔH为______ 。
(6)写出二氧化硫中的S原子和水合氢离子中O原子分别采用______ 和______ 杂化形式,二氧化硫分子和水合氢离子其空间构型分别为________ 和__________ 。
(7)HF水溶液中含有的氢键共_______________ 种。
(8)无水CoCl2为深蓝色,吸水后变为粉红色的水合物,水合物受热后又变成无水CoCl2,故常在实验室中用作吸湿剂和空气湿度指示剂。
CoCl2+xH2O = CoCl2·xH2O
深蓝色 粉红色
现有65g无水CoCl2,吸水后变成CoCl2·xH2O 119g。(CoCl2的相对分子质量:131)
①水合物中x=________ 。
②若该化合物中Co2+配位数为6,而且经定量测定得知内界和外界占有Cl-的个数比为1∶1,则其化学式可表示为______________________ 。
(1)写出原子序数最小的第Ⅷ族元素原子的原子结构示意图
(2)写出3p轨道上有2个未成对电子的元素的符号:
(3)该元素被科学家称之为人体微量元素中的“防癌之王”,其原子的外围电子排布式为4s24p4,该元素的名称是
(4)NH4BF4(氟硼酸铵)是合成氮化硼纳米管的原料之一。1 mol NH4BF4含有
(5)化学反应可视为旧键的断裂和新键的形成过程。化学键的键能是形成化学键时释放的能量。已知白磷和P4O6的分子结构如图所示,现提供以下化学键的键能(kJ·mol-1):P—P:198 P—O:360 O===O:498,则反应P4(白磷)+3O2===P4O6的反应热ΔH为

(6)写出二氧化硫中的S原子和水合氢离子中O原子分别采用
(7)HF水溶液中含有的氢键共
(8)无水CoCl2为深蓝色,吸水后变为粉红色的水合物,水合物受热后又变成无水CoCl2,故常在实验室中用作吸湿剂和空气湿度指示剂。
CoCl2+xH2O = CoCl2·xH2O
深蓝色 粉红色
现有65g无水CoCl2,吸水后变成CoCl2·xH2O 119g。(CoCl2的相对分子质量:131)
①水合物中x=
②若该化合物中Co2+配位数为6,而且经定量测定得知内界和外界占有Cl-的个数比为1∶1,则其化学式可表示为
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】请填空:
(1)A元素L能层p电子数比s电子数多2个,A的元素符号为______ ;B元素M能层p电子数为s电子数的一半,B的元素名称为______ 。
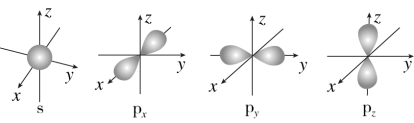
(2)下图是s能级和p能级的原子轨道图。____ 形,每个s能级有____ 个原子轨道;p电子的原子轨道呈____ 形,每个p能级有____ 个原子轨道。
(3)C元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,C的元素符号为____ ,其基态原子的核外电子排布式为______ 。
(4)常温下,向100 mL 0.01 mol⋅L HA溶液中逐滴加入0.02 mol⋅L
HA溶液中逐滴加入0.02 mol⋅L MOH溶液,图中所示曲线表示混合溶液的pH变化情况(体积变化忽略不计)。回答下列问题。
MOH溶液,图中所示曲线表示混合溶液的pH变化情况(体积变化忽略不计)。回答下列问题。_____ (填“强”或“弱”)酸。常温下一定浓度的MA稀溶液的 ,则a
,则a_____ (填“>”“<”或“=”)7,用离子方程式表示其原因:______ 。
(1)A元素L能层p电子数比s电子数多2个,A的元素符号为
(2)下图是s能级和p能级的原子轨道图。
(3)C元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,C的元素符号为
(4)常温下,向100 mL 0.01 mol⋅L
 HA溶液中逐滴加入0.02 mol⋅L
HA溶液中逐滴加入0.02 mol⋅L MOH溶液,图中所示曲线表示混合溶液的pH变化情况(体积变化忽略不计)。回答下列问题。
MOH溶液,图中所示曲线表示混合溶液的pH变化情况(体积变化忽略不计)。回答下列问题。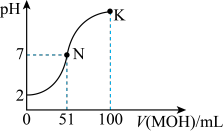
 ,则a
,则a
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】回答下列问题:
(1)在周期表中,与Li的化学性质最相似的邻族元素是_______ ,该元素基态原子核外M层电子的自旋状态_______ (填“相同”或“相反”)。
(2)基态K原子中,核外电子占据的最高能层的符号是_______ ,占据该能层电子的电子云轮廓图形状为_______ 。
(3)基态硅原子最外层的电子排布图为_______ 。
(4)写出基态As原子的核外电子排布式:_______ 。
(5)已知 与
与 结构相似,则NaCN的电子式为
结构相似,则NaCN的电子式为_______ 。
(1)在周期表中,与Li的化学性质最相似的邻族元素是
(2)基态K原子中,核外电子占据的最高能层的符号是
(3)基态硅原子最外层的电子排布图为
(4)写出基态As原子的核外电子排布式:
(5)已知
 与
与 结构相似,则NaCN的电子式为
结构相似,则NaCN的电子式为
您最近半年使用:0次
【推荐1】回答下列问题
(1)写出基态As原子的核外电子排布式___________ 、基态碳原子的电子排布图___________ ,根据元素周期律,原子半径Ga___________ As,第一电离能Ga___________ As。(填“大于”或“小于”)
(2)镍元素基态原子的电子排布式为___________ ,3d能级上的未成对电子数为___________ ;①C、N、O;②N、S、P;③C 、N、Si;④N、 O、F的第一电离能由大到小的顺序为___________ ;电负性:H、O、S电负性由大到小的顺序是___________ 。B和N相比,电负性较大的是___________ ;BN中B元素的化合价为___________ ;从电负性角度分析,C、Si和O元素的非金属活泼性由强至弱的顺序为___________ 。
(3)铬、铜、铁、锰等原子的基态电子排布式___________ ,氯元素的基态原子的价电子层排布式是___________ ,与铬同周期的所有元素的基态原子中最外层电子数与铬原子相同的元素有___________ (填元素符号),第一电离能I1(C)、I1(N)、I1(O)由大到小的顺序为___________ 。
(4)基态Co原子核外电子排布式为___________ ,C、N、O三种元素的第一电离能由大到小的顺序为___________ (用具体元素符号表示)。
(5)基态Fe3+的M层电子排布式为___________ ,铝原子核外自旋方向相同的电子最多有___________ 个,与铝同族的第四周期元素原子的价电子排布式为___________ ,基态磷原子的核外电子运动状态共有___________ 种,其价电子排布式为___________ 。在硼、氧、氟、氮中第一电离能由大到小的顺序是___________ (用元素符号表示)。
(6)基态Ge原子的核外电子排布式为[Ar]___________ ,有___________ 个未成对电子。光催化还原CO2制备CH4反应中,带状纳米Zn2GeO4是该反应的良好催化剂。Zn、Ge、O电负性由大至小的顺序是___________ 。
(1)写出基态As原子的核外电子排布式
(2)镍元素基态原子的电子排布式为
(3)铬、铜、铁、锰等原子的基态电子排布式
(4)基态Co原子核外电子排布式为
(5)基态Fe3+的M层电子排布式为
(6)基态Ge原子的核外电子排布式为[Ar]
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】氯酸镁[ ]常用作催熟剂、除草剂等,可用
]常用作催熟剂、除草剂等,可用 和
和 反应制备。完成下列填空:
反应制备。完成下列填空:
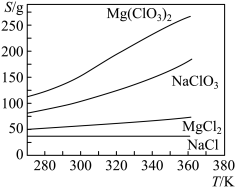
(1)已知四种物质的溶解度如图,写出向 溶液中加入饱和
溶液中加入饱和 溶液制备
溶液制备 的化学反应方程式
的化学反应方程式_______ 。
(2)上述反应能够发生的原因是_______ 。
(3)氧原子最外层电子排布的轨道表达式为_______ ,镁原子核外共有_______ 种能量不同的电子。
(4)组成 和
和 的元素中,处于同周期元素的离子半径由大到小的顺序为
的元素中,处于同周期元素的离子半径由大到小的顺序为_______ 。
(5)氯与溴在同一主族,下列能说明氯的非金属性强于溴的事实是_______ (选填编号)。
a. 氧化性强于
氧化性强于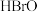
b. 的分解温度低于
的分解温度低于
c.向溴化亚铁溶液中滴入少量氯水,溶液颜色变黄
d. 是非氧化还原反应
是非氧化还原反应
(6)氯气与碱液反应时,产物受温度和浓度的影响。在低温和稀碱液中主要产物是 和
和 ,在75℃以上和浓碱液中主要产物是
,在75℃以上和浓碱液中主要产物是 和
和 。
。
①室温下,向含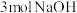 的稀碱液中通入
的稀碱液中通入 氯气,充分反应后,溶液中离子按浓度由大到小的顺序排列为:
氯气,充分反应后,溶液中离子按浓度由大到小的顺序排列为:_______ 。
②一定温度下,向 溶液中通入氯气至恰好完全反应,配平下列化学方程式。
溶液中通入氯气至恰好完全反应,配平下列化学方程式。______

每生成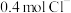 ,转移的电子数目为
,转移的电子数目为_______ 。
 ]常用作催熟剂、除草剂等,可用
]常用作催熟剂、除草剂等,可用 和
和 反应制备。完成下列填空:
反应制备。完成下列填空:
(1)已知四种物质的溶解度如图,写出向
 溶液中加入饱和
溶液中加入饱和 溶液制备
溶液制备 的化学反应方程式
的化学反应方程式(2)上述反应能够发生的原因是
(3)氧原子最外层电子排布的轨道表达式为
(4)组成
 和
和 的元素中,处于同周期元素的离子半径由大到小的顺序为
的元素中,处于同周期元素的离子半径由大到小的顺序为(5)氯与溴在同一主族,下列能说明氯的非金属性强于溴的事实是
a.
 氧化性强于
氧化性强于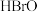
b.
 的分解温度低于
的分解温度低于
c.向溴化亚铁溶液中滴入少量氯水,溶液颜色变黄
d.
 是非氧化还原反应
是非氧化还原反应(6)氯气与碱液反应时,产物受温度和浓度的影响。在低温和稀碱液中主要产物是
 和
和 ,在75℃以上和浓碱液中主要产物是
,在75℃以上和浓碱液中主要产物是 和
和 。
。①室温下,向含
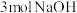 的稀碱液中通入
的稀碱液中通入 氯气,充分反应后,溶液中离子按浓度由大到小的顺序排列为:
氯气,充分反应后,溶液中离子按浓度由大到小的顺序排列为:②一定温度下,向
 溶液中通入氯气至恰好完全反应,配平下列化学方程式。
溶液中通入氯气至恰好完全反应,配平下列化学方程式。
每生成
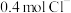 ,转移的电子数目为
,转移的电子数目为
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】新质生产力的底色是绿色低碳。而化学,在绿色低碳方面当仁不让,新质生产力涵盖的产业链很多与化学化工相关,合成氨是人类科学技术上的一项重大突破,在很大程度上解决了地球上因粮食不足而导致的饥饿问题,是化学和技术对社会发展与进步的巨大贡献。
(1)自然界中的氮元素主要以分子的形式存在于空气中,是固氮的主要来源。
①基态氮原子的价电子轨道表示式为___________ 。
②自然固氮过程中生成的NO 的VSEPR模型名称为
的VSEPR模型名称为___________ 。
(2)铁触媒是普遍使用的人工合成氨的催化剂,以铁为主体通常还含有Al2O3、K2O、CaO、MgO、Cr2O3等氧化物。
①上述氧化物所涉及的元素中,处于元素周期表中p区的元素是___________ 。
②基态铬原子的电子排布式为___________ 。
③下列比较正确的是___________ 。
A.第一电离能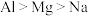 B.熔点:
B.熔点: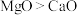
C.离子半径: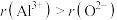 D.键角:
D.键角: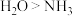
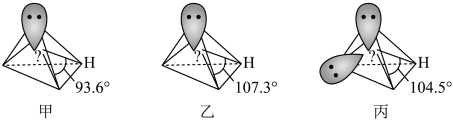
④NH3、H2O和PH3分子的空间结构和相应的键角如图所示,则甲、乙对应的分子分别是___________ 、___________ 。
(1)自然界中的氮元素主要以分子的形式存在于空气中,是固氮的主要来源。
①基态氮原子的价电子轨道表示式为
②自然固氮过程中生成的NO
 的VSEPR模型名称为
的VSEPR模型名称为(2)铁触媒是普遍使用的人工合成氨的催化剂,以铁为主体通常还含有Al2O3、K2O、CaO、MgO、Cr2O3等氧化物。
①上述氧化物所涉及的元素中,处于元素周期表中p区的元素是
②基态铬原子的电子排布式为
③下列比较正确的是
A.第一电离能
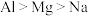 B.熔点:
B.熔点: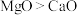
C.离子半径:
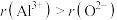 D.键角:
D.键角: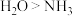
④NH3、H2O和PH3分子的空间结构和相应的键角如图所示,则甲、乙对应的分子分别是
您最近半年使用:0次




