硫代硫酸钠(Na2S2O3)俗名为大苏打或海波,在碱性条件下稳定,遇酸易分解。将SO2通入按一定比例配成的Na2S和Na2CO3的混合溶液中,便可得到Na2S2O3,同时生成CO2。
已知:①SO2+2H2S=3S↓+2H2O;②CuSO4+H2S=CuS↓(黑色)+H2SO4。请回答下列问题:
(1)Na2S2O3中S元素的化合价为______ 价。
(2)Na2S2O3与稀H2SO4反应的离子方程式为__________ 。
(3)制备Na2S2O3的化学方程式为_________________ ,在制备过程中通入的SO2不能过量,原因为__________ 。
(4)在配制混合溶液前先将蒸馏水加热煮沸一段时间后再用,其目的是__________________ 。
(5)制得的Na2S2O3晶体中常混有Na2S杂质,某同学取少量制得的晶体溶于足量稀H2SO4中,并将产生的气体通入CuSO4溶液中,未见黑色沉淀,据此该同学认为制得的晶体中不含Na2S杂质。你认为其结论是否合理?_____ (填“合理”或“不合理"),理由为__________________ 。
已知:①SO2+2H2S=3S↓+2H2O;②CuSO4+H2S=CuS↓(黑色)+H2SO4。请回答下列问题:
(1)Na2S2O3中S元素的化合价为
(2)Na2S2O3与稀H2SO4反应的离子方程式为
(3)制备Na2S2O3的化学方程式为
(4)在配制混合溶液前先将蒸馏水加热煮沸一段时间后再用,其目的是
(5)制得的Na2S2O3晶体中常混有Na2S杂质,某同学取少量制得的晶体溶于足量稀H2SO4中,并将产生的气体通入CuSO4溶液中,未见黑色沉淀,据此该同学认为制得的晶体中不含Na2S杂质。你认为其结论是否合理?
更新时间:2020-08-02 13:49:18
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】硫酸是重要的化工产品,可用于生产化肥、农药、炸药、染料等。工业制硫酸的原理示意图(反应条件和部分生成物已略去)如下:

(1)质量相同的 和
和 的物质的量之比为
的物质的量之比为_______ 。
(2)黄铁矿制硫酸产生的废气中含有 ,可用双脱硫法处理,过程如下图所示,其中可循环使用的试剂是
,可用双脱硫法处理,过程如下图所示,其中可循环使用的试剂是_______ ,写出双碱法脱硫法的总反应方程式:_______ 。

(3)甲、乙两位同学用铜和硫酸作原料,设计了两种制取硫酸铜的方案。
方案甲:铜与浓硫酸加热直接反应,即Cu→ 。
。
方案乙:Cu→CuO→ 。
。
①方案甲中,铜和浓硫酸发生反应的化学方程式是_______ 。该反应体现了浓硫酸的_______ 。
②这两种方案,你认为哪一种方案更合理?_______ 。理由是_______ 。

(1)质量相同的
 和
和 的物质的量之比为
的物质的量之比为(2)黄铁矿制硫酸产生的废气中含有
 ,可用双脱硫法处理,过程如下图所示,其中可循环使用的试剂是
,可用双脱硫法处理,过程如下图所示,其中可循环使用的试剂是
(3)甲、乙两位同学用铜和硫酸作原料,设计了两种制取硫酸铜的方案。
方案甲:铜与浓硫酸加热直接反应,即Cu→
 。
。方案乙:Cu→CuO→
 。
。①方案甲中,铜和浓硫酸发生反应的化学方程式是
②这两种方案,你认为哪一种方案更合理?
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】物质的类别和核心元素的化合价是研究物质化学性质的两个重要角度。硫元素的价类二维图如图所示(其中h、g的阳离子均为 ),请回答下列问题:
),请回答下列问题:

(1)e的化学式是___________ 。
(2)实验室常用g和f的浓溶液制备气体c,写出其化学方程式___________ 。
(3)将气体c通入a的水溶液,溶液变浑浊,用化学方程式解释___________ ,体现了c的___________ 性。
(4)过量的铜与f的浓溶液在加热条件下可以发生,化学方程式为___________ ,反应后铜片有剩余,为使剩余的铜片继续溶解,可在其中加入硝酸盐溶液(如 溶液),则该反应的离子方程式为
溶液),则该反应的离子方程式为___________ 。
 ),请回答下列问题:
),请回答下列问题:
(1)e的化学式是
(2)实验室常用g和f的浓溶液制备气体c,写出其化学方程式
(3)将气体c通入a的水溶液,溶液变浑浊,用化学方程式解释
(4)过量的铜与f的浓溶液在加热条件下可以发生,化学方程式为
 溶液),则该反应的离子方程式为
溶液),则该反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】下图表示的是用明矾[KAl(SO4)2·12H2O]制取硫酸铝和硫酸钾的操作流程图,请根据此图回答有关问题。

进行操作②时,加入的试剂是___________ ,从反应混合物中分离A所进行的实验操作是_______ ,
其反应的离子方程式为______________________ 。

进行操作②时,加入的试剂是
其反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】含氯消毒剂和过氧化物消毒剂均可有效灭杀新冠病毒。
Ⅰ.过碳酸钠(2Na2CO3·3H2O2)俗称固态双氧水,具有去污、杀菌等功效。其制备原理为:2Na2CO3(aq)+3H2O2(aq)=2Na2CO3·3H2O2(aq) △H<0。
(1)结合过氧化氢和碳酸钠的性质,推测制备过碳酸钠的过程中,碳酸钠与过氧化氢的物质的量之比应小于2:3,且加入Na2CO3溶液速率不能过快的原因是_______ 。
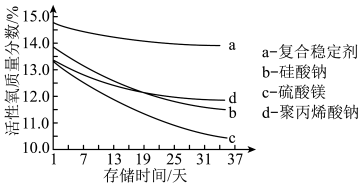
(2)过碳酸钠的储存稳定性是重要的品质指标。以不同种类的稳定剂制备的过碳酸钠产品,测得其活性氧的质量分数随时间变化如图所示。由图可知,制备过碳酸钠时应选择的稳定剂是_______ 。(填图中字母)
Ⅱ.NaClO2是一种更为安全有效的清洗﹑杀菌剂,特别是在NaClO使用受限制的场合,NaClO3是NaClO的安全代用品。
(3)工业上用石墨电极电解ClO2、NaCl溶液制备NaClO3。写出该反应的离子方程式:_______ 。
Ⅰ.过碳酸钠(2Na2CO3·3H2O2)俗称固态双氧水,具有去污、杀菌等功效。其制备原理为:2Na2CO3(aq)+3H2O2(aq)=2Na2CO3·3H2O2(aq) △H<0。
(1)结合过氧化氢和碳酸钠的性质,推测制备过碳酸钠的过程中,碳酸钠与过氧化氢的物质的量之比应小于2:3,且加入Na2CO3溶液速率不能过快的原因是
(2)过碳酸钠的储存稳定性是重要的品质指标。以不同种类的稳定剂制备的过碳酸钠产品,测得其活性氧的质量分数随时间变化如图所示。由图可知,制备过碳酸钠时应选择的稳定剂是

Ⅱ.NaClO2是一种更为安全有效的清洗﹑杀菌剂,特别是在NaClO使用受限制的场合,NaClO3是NaClO的安全代用品。
(3)工业上用石墨电极电解ClO2、NaCl溶液制备NaClO3。写出该反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】二氧化氯(ClO2)是一种黄绿色气体,易溶于水,在混合气体中的体积分数大于10%就可能发生爆炸,在工业上常用作水处理剂、漂白剂。回答下列问题:
(1)若以单位质量的氧化剂所得到的电子数来表示消毒效率,则ClO2、Cl2两种消毒剂的消毒效率较大的是哪种_____ 。(填化学式)
(2)某小组设计了如图所示的实验装置用于制备ClO2。

①装置A三颈烧瓶中,通入氮气的主要作用有两个,其一是可以起到搅拌作用,其二是_____ 。
②装置B的作用是_____ 。
③装置A用于生成ClO2气体,该反应的离子方程式为_____ 。
④当看到装置C中导管液面上升时应进行的操作是_____ 。
(1)若以单位质量的氧化剂所得到的电子数来表示消毒效率,则ClO2、Cl2两种消毒剂的消毒效率较大的是哪种
(2)某小组设计了如图所示的实验装置用于制备ClO2。

①装置A三颈烧瓶中,通入氮气的主要作用有两个,其一是可以起到搅拌作用,其二是
②装置B的作用是
③装置A用于生成ClO2气体,该反应的离子方程式为
④当看到装置C中导管液面上升时应进行的操作是
您最近一年使用:0次



 。
。


