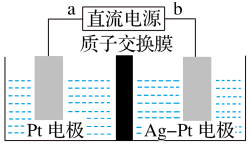
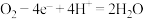全钒液流电池是一种以钒为活性物质呈循环流动液态的氧化还原电池,适合用作电动汽车的动力电源,其工作原理如图所示。已知充电过程中V3+发生还原反应。下列说法不正确的是
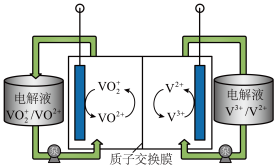

A.质子交换膜可阻止VO 与V2+直接发生反应 与V2+直接发生反应 |
| B.充电时,阴极的电极反应为:V2+-e-=V3+ |
| C.充电时,氢离子通过交换膜移向右侧 |
D.放电时,正极的电极反应为:VO +e-+H2O=VO2++2OH- +e-+H2O=VO2++2OH- |
更新时间:2020/08/05 13:58:38
|
相似题推荐
多选题
|
适中
(0.65)
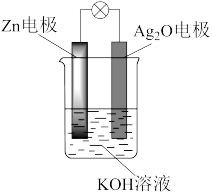
【推荐1】银锌电池是一种常见化学电源,其反应原理:Zn+Ag2O+H2O Zn(OH)2+2Ag,其工作示意图如图。下列说法正确的是
Zn(OH)2+2Ag,其工作示意图如图。下列说法正确的是
 Zn(OH)2+2Ag,其工作示意图如图。下列说法正确的是
Zn(OH)2+2Ag,其工作示意图如图。下列说法正确的是
| A.Zn电极是正极 |
| B.Ag2O电极上发生氧化反应 |
C.Zn电极的电极反应式:Zn-2e-+2OH- Zn(OH)2 Zn(OH)2 |
| D.放电一段时间后溶液的pH变大 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
解题方法
【推荐2】燃料敏化太阳能电池因其工艺简单、性能稳定等特点深受科学家的青睐。一种钌基配合物作为光敏剂(S)的太阳能电池的工作原理如图所示,其中一个电极可表示为TiO2/S,电极反应为TiO2/S*→TiO2/S++e-。下列有关说法错误的是
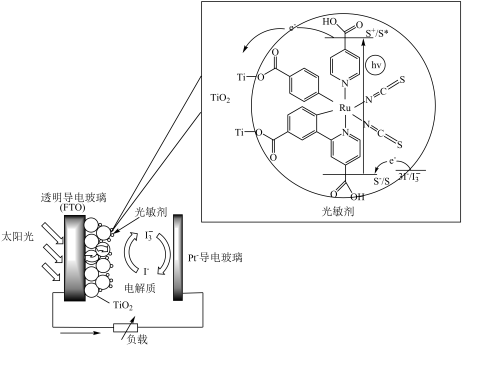

| A.该电池工作时,光能→化学能→电能 |
B.电池的正极反应为I +2e-→3I- +2e-→3I- |
C.电解质溶液中可发生反应TiO2/S++3I-→TiO2/S+I |
D.电池的电解质溶液中I-和I 的浓度不会减少 的浓度不会减少 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
解题方法
【推荐1】由相同金属电极及其不同浓度的盐溶液组成的电池,称浓差电池,电子由溶液浓度较小的一极经外电路流向浓度较大的一极。如图所示装置中,X电极与Y电极初始质量相等。进行实验时,先闭合 ,断开
,断开 ,一段时间后,再断开
,一段时间后,再断开 ,闭合
,闭合 ,即可形成浓差电池,电流表指针偏转。下列不正确的是
,即可形成浓差电池,电流表指针偏转。下列不正确的是
 ,断开
,断开 ,一段时间后,再断开
,一段时间后,再断开 ,闭合
,闭合 ,即可形成浓差电池,电流表指针偏转。下列不正确的是
,即可形成浓差电池,电流表指针偏转。下列不正确的是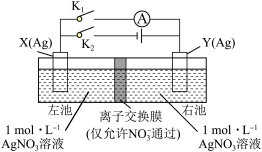
| A.充电前,该电池两电极存在电势差 |
B.放电时,右池中的 通过离子交换膜移向左池 通过离子交换膜移向左池 |
| C.充电时,当外电路通过0.1mol电子时,两电极的质量差为10.8g |
| D.放电时,电极Y为电池的正极 |
您最近一年使用:0次
多选题
|
适中
(0.65)
解题方法
【推荐2】电解处理垃圾渗液是一项重要的环保课题,研究小组用右图装置进行渗液(pH=6.5-8)处理,可以实现其中的NH3和有机物COD的转化,下列说法错误的是
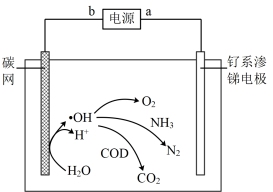

| A.a为电源负极 |
| B.阳极反应式为H2O-e-=·OH+H+ |
| C.电解后的废液呈强酸性 |
| D.电路中每转移3mole-一定生成标准状况下11.2LN2 |
您最近一年使用:0次
多选题
|
适中
(0.65)
解题方法
【推荐1】南京大学研究发现电化学“大气固碳”有效方法,电池工作原理示意图如图所示。充电时,利用催化剂的选择性,阳极电极反应式为:2Li2CO3-4e-=2CO2+O2+4Li+,下列有关说法正确的是
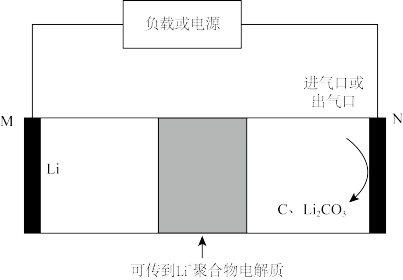

| A.放电时,M电极的电势比N电极的高 |
| B.放电时,正极电极反应式:3CO2+4e-+4Li+=C+2Li2CO3 |
| C.充电时,M电极接外电源负极,电解质可选含Li+水溶液 |
| D.该电池每放电、充电一次,若均转移2mol电子,理论上能固定标准状况下11.2LCO2 |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐2】在电解水制取H2和O2时,为了增强导电性,常常要加入一些电解质,最好选用
| A.H2SO4 | B.HCl |
| C.NaCl | D.NaOH |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
【推荐1】利用电解法制备Ca(H2PO4)2并得到副产物NaOH和Cl2。下列说法正确的是


| A.C膜可以为质子交换膜 |
| B.阴极室的电极反应式为2H2O-4e-=O2↑+4H+ |
| C.可用铁电极替换阴极的石墨电极 |
| D.每转移2 mol e-,阳极室溶液质量减少111 g |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐2】金属镍(Ni)有广泛的用途。粗镍中含有少量Fe、Zn、Cu、Pt等杂质,可用电解法制备高纯度的镍(已知氧化性:Fe2+<Ni2+<Cu2+)。下列叙述中不正确的是
| A.电解过程中,阳极质量的减少与阴极质量的增加相等 |
| B.阴极发生还原反应,其电极反应为Ni2++2e-=Ni |
| C.电解后,溶液中存在的金属阳离子只有Zn2+、Fe2+ |
| D.电解后,电解槽底部的阳极泥中一定有Cu和Pt |
您最近一年使用:0次

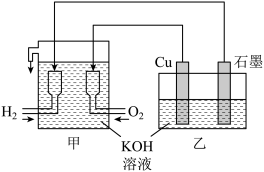
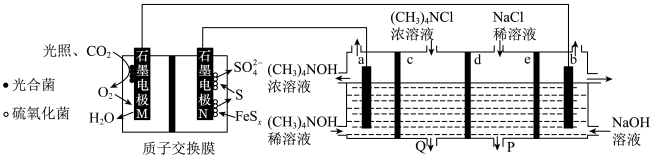
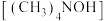 ,采用微生物燃料电池电渗析法合成
,采用微生物燃料电池电渗析法合成 的工作原理如图所示,下列说法正确的是
的工作原理如图所示,下列说法正确的是