某化学课外活动小组设计了如图所示的装置(图中夹持装置未画出,“Δ”表示酒精灯热源)来研究乙醇催化氧化的实验。已知:无水乙醇的沸点为78℃,新制氢氧化铜悬浊液可用于验证乙醇催化氧化反应的氧化产物。

(1)发生反应时,装置A中反应的还原剂是____________ (填化学式,下同),D中反应的氧化剂是____________ 。
(2)装置B的作用是____________ ;装置C中热水的作用是____________ 。
(3)装置D中发生的氧化反应的化学方程式为____________ 。
(4)实验一段时间后,若撤掉装置D中的酒精灯,则反应____________ (填“能”或“不能”)继续进行,原因是____________ 。

(1)发生反应时,装置A中反应的还原剂是
(2)装置B的作用是
(3)装置D中发生的氧化反应的化学方程式为
(4)实验一段时间后,若撤掉装置D中的酒精灯,则反应
更新时间:2020-08-09 19:31:31
|
相似题推荐
解答题-有机推断题
|
较易
(0.85)
解题方法
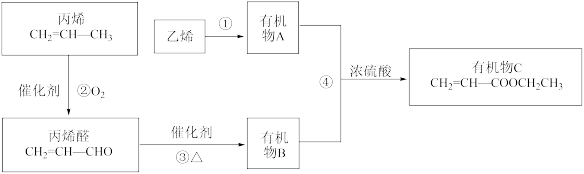
【推荐1】现有A、B、C、D、E、F六种有机物,它们的转化关系如图所示(图中部分反应条件及生成物没有全部写出)。已知:液体B能发生银镜反应,气体D的相对分子质量为28。
(1)A、B、C的结构简式分别是____ 、___ 、____ 。
(2)B、C中所含官能团的名称分别是___ 、____ 。
(3)A到D的反应类型为____ 。
(4)C→A的反应条件是____ 。
(5)D→F反应的化学方程式是____ 。

(1)A、B、C的结构简式分别是
(2)B、C中所含官能团的名称分别是
(3)A到D的反应类型为
(4)C→A的反应条件是
(5)D→F反应的化学方程式是
您最近一年使用:0次
解答题-有机推断题
|
较易
(0.85)
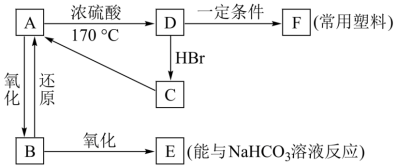
【推荐2】物质A是石油化学工业重要的基础原料,A的产量可以用来衡量一个国家石油化工发展水平。E是具有果香味的有机物,F是一种高聚物,可制成多种包装材料。各物质间的转化关系如图所示。
(1)A的结构式为___________ ,C中所含官能团为___________ 。
(2)写出下列反应的反应类型:①___________ ;②___________ 。
(3)写出反应②、④的化学方程式:②___________ 、④___________ 。

(1)A的结构式为
(2)写出下列反应的反应类型:①
(3)写出反应②、④的化学方程式:②
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐3】某实验小组用如图装置进行乙醇催化氧化的实验。
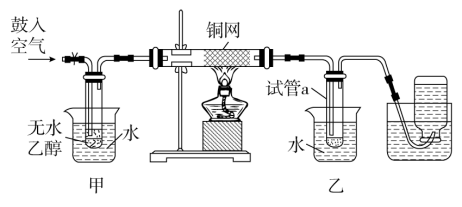
(1)实验过程中铜网出现红色和黑色交替的现象,请按先后顺序写出相应的化学反应方程式_______ 。
(2)在不断鼓入空气的情况下,熄灭酒精灯,反应仍能继续进行,说明该乙醇氧化反应是_______ 反应。
(3)甲和乙两个装置均用水浴加热,作用_______ 相同(填写“是”或“否”),甲的作用是_______ 。
(4)若试管a中收集到的液体用紫色石蕊试纸检验,试纸显红色,说明液体中还含有_______ 。要除去该物质,可先在混合液中加入_______ (填字母),然后,再通过_______ (填实验操作名称)即可除去。
a.氯化钠溶液 b.苯 c.碳酸氢钠溶液 d.四氯化碳

(1)实验过程中铜网出现红色和黑色交替的现象,请按先后顺序写出相应的化学反应方程式
(2)在不断鼓入空气的情况下,熄灭酒精灯,反应仍能继续进行,说明该乙醇氧化反应是
(3)甲和乙两个装置均用水浴加热,作用
(4)若试管a中收集到的液体用紫色石蕊试纸检验,试纸显红色,说明液体中还含有
a.氯化钠溶液 b.苯 c.碳酸氢钠溶液 d.四氯化碳
您最近一年使用:0次
解答题-有机推断题
|
较易
(0.85)
解题方法
【推荐1】化合物M是一种具有茉莉花香味的无色油状液体,结构简式是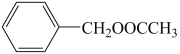 ,其合成路线如图(部分反应条件未注明):
,其合成路线如图(部分反应条件未注明):
(1)烃A的结构简式是___ ,G所含官能团的名称是___ 。
(2)写出F与新制氢氧化铜悬浊液反应的化学方程式___ 。
(3)B→C反应的化学方程式是___ 。
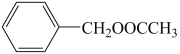 ,其合成路线如图(部分反应条件未注明):
,其合成路线如图(部分反应条件未注明):
(1)烃A的结构简式是
(2)写出F与新制氢氧化铜悬浊液反应的化学方程式
(3)B→C反应的化学方程式是
您最近一年使用:0次
解答题-有机推断题
|
较易
(0.85)
名校
解题方法
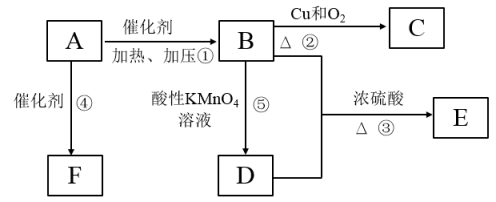
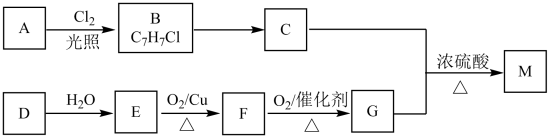
【推荐2】A—E为常见的有机物。以A为原料合成化合物E,其合成路线如图1所示。已知:A的产量通常用来衡量一个国家的石油化工水平;2CH3CHO+O2 2CH3COOH。
2CH3COOH。
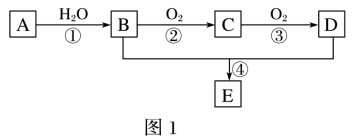
(1)A的分子式______ 。
(2)A中官能团的名称是_____ ;B中官能团的结构简式是_____ 。
(3)反应①的反应类型为_____ ;反应④的反应类型为_____ 。
(4)反应④的化学方程式为_____ 。
(5)某学习小组设计B催化氧化的实验装置如图,根据图2装置回答问题。
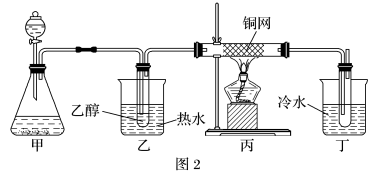
①装置甲锥形瓶中盛放的固体为过氧化钠,请写出甲中反应的化学方程式_____ 。
②B催化氧化的产物与葡萄糖具有相同的特征反应,将所得的氧化产物滴加到新制氢氧化铜悬浊液中加热,现象为_____ 。
③实验过程中,丙装置硬质玻璃管中发生反应的化学方程式为_____ 。
 2CH3COOH。
2CH3COOH。
(1)A的分子式
(2)A中官能团的名称是
(3)反应①的反应类型为
(4)反应④的化学方程式为
(5)某学习小组设计B催化氧化的实验装置如图,根据图2装置回答问题。

①装置甲锥形瓶中盛放的固体为过氧化钠,请写出甲中反应的化学方程式
②B催化氧化的产物与葡萄糖具有相同的特征反应,将所得的氧化产物滴加到新制氢氧化铜悬浊液中加热,现象为
③实验过程中,丙装置硬质玻璃管中发生反应的化学方程式为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐1】某研究小组制备氯气并对产生氯气的条件进行探究。
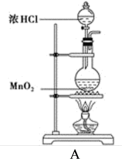
(1)装置A中用MnO2与浓盐酸反应制取Cl2,利用了浓HCl的_______ (填“氧化性”或“还原性”)。
(2)A中产生的气体不纯,含有的杂质可能是_______ 。(填写化学式)
(3)装置B用于吸收多余的Cl2,B中发生反应的离子方程式是_______ 。
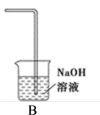
(4)该小组欲研究盐酸的浓度对制Cl2的影响,设计实验进行探究:
①已知MnO2呈弱碱性。Ⅰ中溶液呈浅棕色是由于MnO2与浓盐酸发生了复分解反应,化学方程式是_______ 。
②Ⅱ中发生了分解反应,反应的化学方程式是_______ 。
③Ⅲ中无明显现象的原因,可能是c(H+)或c(Cl-)较低,设计实验Ⅳ进行探究:
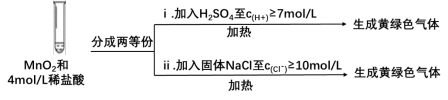
将实验Ⅲ、Ⅳ作对比,得出的结论是_______ ;
将ⅰ、ⅱ作对比,得出的结论是_______ 。

(1)装置A中用MnO2与浓盐酸反应制取Cl2,利用了浓HCl的
(2)A中产生的气体不纯,含有的杂质可能是
(3)装置B用于吸收多余的Cl2,B中发生反应的离子方程式是

(4)该小组欲研究盐酸的浓度对制Cl2的影响,设计实验进行探究:
| 实验 | 操作 | 现象 |
| Ⅰ | 常温下将MnO2和12mol/L浓盐酸混合 | 溶液呈浅棕色,略有刺激性气味 |
| Ⅱ | 将Ⅰ中混合物过滤,加热滤液 | 生成大量黄绿色气体 |
| Ⅲ | 加热MnO2和4mol/L稀盐酸混合物 | 无明显现象 |
②Ⅱ中发生了分解反应,反应的化学方程式是
③Ⅲ中无明显现象的原因,可能是c(H+)或c(Cl-)较低,设计实验Ⅳ进行探究:

将实验Ⅲ、Ⅳ作对比,得出的结论是
将ⅰ、ⅱ作对比,得出的结论是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐2】某实验小组为了探究铝与盐酸反应过程中的速率变化,分两组做了以下实验。
(1)甲小组同学用足量的铝与50 mL盐酸发生反应,并用排水集气法收集反应放出的氢气,实验记录如下:
①哪一时间段(即0~1、1~2、2~3、3~4、4~5 min)反应速率最大__ ,原因是____ ;
②反应进行到10 min时,便不再有气泡产生,该盐酸中HCl的物质的量浓度是__ ,整个反应过程中HCl的反应速率为____ ;
(2)乙小组学生也做了同样的实验,但由于反应太快,不好测量氢气体积,他事先在盐酸中加入等体积的下列液体:A.蒸馏水、B.KCl溶液、C.KNO3溶液、D.CuSO4溶液,以减慢反应速率,你认为可行的是____ ,不可行的理由是_________ 。
(1)甲小组同学用足量的铝与50 mL盐酸发生反应,并用排水集气法收集反应放出的氢气,实验记录如下:
| 时间/min | 1 | 2 | 3 | 4 | 5 | 反应结束时 |
| 氢气体积/mL(标准状况下) | 50 | 150 | 300 | 380 | 410 | 560 |
②反应进行到10 min时,便不再有气泡产生,该盐酸中HCl的物质的量浓度是
(2)乙小组学生也做了同样的实验,但由于反应太快,不好测量氢气体积,他事先在盐酸中加入等体积的下列液体:A.蒸馏水、B.KCl溶液、C.KNO3溶液、D.CuSO4溶液,以减慢反应速率,你认为可行的是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐3】将加热至红热的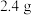 木炭投入盛有足量
木炭投入盛有足量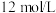 的浓
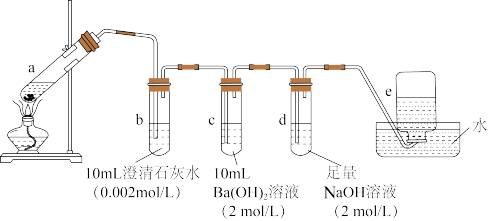
的浓 的试管中,立即塞好塞子,如图所示,连接好装置(已检查装置的气密性)。
的试管中,立即塞好塞子,如图所示,连接好装置(已检查装置的气密性)。
请回答下列问题:
(1)反应开始后撤去酒精灯,试管a中除可看到木炭剧烈反应直至消失外,还观察到的现象是________________________________________________________ 。
(2)试管b中最终____________ (填“有”或“无”)沉淀产生,原因是_____________________________________________________________ 。
(3)试管c中发生反应的化学方程式为___________________ 。
(4)集气瓶e中最后收集到的气体为______________________ (填化学式),理论上该气体的总体积为_______________ L(标准状况,结果保留小数点后2位数字)。
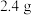 木炭投入盛有足量
木炭投入盛有足量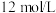 的浓
的浓 的试管中,立即塞好塞子,如图所示,连接好装置(已检查装置的气密性)。
的试管中,立即塞好塞子,如图所示,连接好装置(已检查装置的气密性)。
请回答下列问题:
(1)反应开始后撤去酒精灯,试管a中除可看到木炭剧烈反应直至消失外,还观察到的现象是
(2)试管b中最终
(3)试管c中发生反应的化学方程式为
(4)集气瓶e中最后收集到的气体为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐1】某小组在实验室探究金属钠、金属镁分别与二氧化碳的反应。
(1)用为了得到干燥纯净的 ,产生的气体应依次通过盛有
,产生的气体应依次通过盛有___________ 、___________ 的洗气瓶。
(2)实验证明 可以支持镁燃烧,写出该反应化学方程式,
可以支持镁燃烧,写出该反应化学方程式,并用单线桥法分析电子转移情况 ___________ ;该反应条件下,还原性
___________  (填“>”或“<”)。
(填“>”或“<”)。
(3)探究金属钠与二氧化碳反应的实验步骤及现象如表:
①为检验黑色固体的成分,加热条件下将其与浓硫酸反应,生成的气体能使品红褪色。该黑色固体与浓硫酸反应的化学方程式为___________ 。
②根据上述现象,金属钠与二氧化碳反应的化学方程式为___________ 。
(1)用为了得到干燥纯净的
 ,产生的气体应依次通过盛有
,产生的气体应依次通过盛有(2)实验证明
 可以支持镁燃烧,写出该反应化学方程式,
可以支持镁燃烧,写出该反应化学方程式,
 (填“>”或“<”)。
(填“>”或“<”)。(3)探究金属钠与二氧化碳反应的实验步骤及现象如表:
| 步骤 | 操作 | 现象 |
| Ⅰ | 将一小块金属钠在燃烧匙中点燃,迅速伸入盛有 的集气瓶中,充分反应后静置冷却 的集气瓶中,充分反应后静置冷却 | 产生大量白烟,集气瓶底部有黑色固体产生,瓶壁上有白色物质产生 |
| Ⅱ | 在反应后的集气瓶中加入适量蒸馏水,振荡,过滤 | 滤纸上有黑色固体,滤液无色 |
| Ⅲ | 取适量滤液于2支试管中,向一支试管中滴加1滴酚酞溶液;向第二支试管中滴加 溶液 溶液 | 第一支试管溶液变红;第二支试管溶液变浑浊 |
②根据上述现象,金属钠与二氧化碳反应的化学方程式为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐2】某学习小组用下图所示实验检验浓硫酸与铜反应产生的二氧化硫(图中夹持装置已略去)。
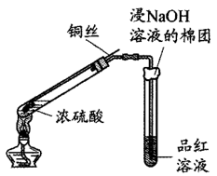
已知:浓硫酸的沸点为338℃,酒精灯外焰温度一般为500℃左右。
(1)浸有NaOH溶液的棉团作用是___________ 。
(2)能证明铜丝与浓硫酸反应产生了SO2的实验现象为___________ 。铜丝与浓硫酸反应的化学方程式为___________ 。
(3)将品红溶液换为Ba(OH)2溶液,发现其中产生白色沉淀。小组同学认为此现象不足以说明Cu和浓硫酸反应产生了SO2,其原因是___________ 。

已知:浓硫酸的沸点为338℃,酒精灯外焰温度一般为500℃左右。
(1)浸有NaOH溶液的棉团作用是
(2)能证明铜丝与浓硫酸反应产生了SO2的实验现象为
(3)将品红溶液换为Ba(OH)2溶液,发现其中产生白色沉淀。小组同学认为此现象不足以说明Cu和浓硫酸反应产生了SO2,其原因是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐3】某学习小组探究氨的还原性及检验产物的性质,按下图装置进行实验(图中夹持装置已略去),并做喷泉实验。将B处的三氧化二铬加热至红热,再鼓入空气,已知:无水氯化钙可吸收氨气和水。回答下列问题:

(1)B中发生反应的化学方程式是___________ 。
(2)证明氨气发生了催化氧化的现象是___________ 。
(3)写出(2)中反应的化学方程式___________ 。
(4)装置E作用是___________ 。
(5)引发装置F的喷泉实验的操作是___________ 。
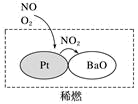
(6)大量行驶的机动车是污染源之一、汽车发动机废气稀燃控制系统主要工作原理如图所示;写出稀燃过程中NO发生的主要反应的方程式___________ 。

(1)B中发生反应的化学方程式是
(2)证明氨气发生了催化氧化的现象是
(3)写出(2)中反应的化学方程式
(4)装置E作用是
(5)引发装置F的喷泉实验的操作是
(6)大量行驶的机动车是污染源之一、汽车发动机废气稀燃控制系统主要工作原理如图所示;写出稀燃过程中NO发生的主要反应的方程式

您最近一年使用:0次