工业是制取高铁酸钾(K2FeO4),是先制取高铁酸钠,然后在低温下,往高铁酸钠溶液中加入KOH至饱和就可以析出高铁酸钾。湿法制备Na2FeO4的主要反应为:2Fe(OH)3+3ClO-+4OH﹣=2 +3Cl﹣+5H2O;干法备Na2FeO4的主要反应为:2FeSO4+6Na2O2=2Na2FeO4+2Na2SO4+O2↑。下列有关说法不正确的是
+3Cl﹣+5H2O;干法备Na2FeO4的主要反应为:2FeSO4+6Na2O2=2Na2FeO4+2Na2SO4+O2↑。下列有关说法不正确的是
 +3Cl﹣+5H2O;干法备Na2FeO4的主要反应为:2FeSO4+6Na2O2=2Na2FeO4+2Na2SO4+O2↑。下列有关说法不正确的是
+3Cl﹣+5H2O;干法备Na2FeO4的主要反应为:2FeSO4+6Na2O2=2Na2FeO4+2Na2SO4+O2↑。下列有关说法不正确的是| A.湿法和干法制备中,生成1 mol Na2FeO4转移电子数目不相同 |
| B.高铁酸钾在低温下的溶解度比高铁酸钠的溶解度小 |
| C.干法制备的主要反应中Na2O2只做氧化剂 |
| D.K2FeO4处理水时,既能杀菌消毒,生成的Fe(OH)3胶体还能吸附水中的悬浮杂质 |
2020高三·全国·专题练习 查看更多[2]
更新时间:2020-08-10 12:38:44
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】为达到实验目的,下列实验设计正确的是
| A | B | C | D |
 |  | 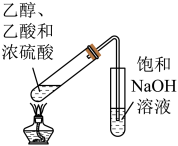 |  |
| 制备氢氧化铁胶体 | 验证 的漂白性 的漂白性 | 制取少量乙酸乙酯 | 分离乙醇和水 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】NaCl是中学阶段常见的物质,下列涉及NaCl的实验描述不正确的是
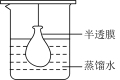 | 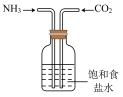 | 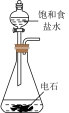 | 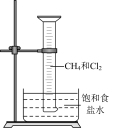 |
| 甲 | 乙 | 丙 | 丁 |
| A.用图甲所示装置除去淀粉溶液中混有的NaCl |
| B.用图乙所示装置在实验室模拟侯式制碱法 |
| C.图丙装置中饱和食盐水可以减缓反应速率 |
| D.图丁装置中反应后量筒中液面会升高,且析出晶体 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】氨水可以用于SCR和SNCR工艺。是用NH3还原剂喷入炉内或烟道内与NOx进行选择性反应,主要反应为:8NH3+6NO2→7N2+12H2O。下列说法错误的是
| A.NH3是还原剂 | B.H2O是氧化产物 |
| C.消除1molNO2转移电子为4mol | D.NO2是氧化剂 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】工业上以铬铁矿(主要成分为FeO·Cr2O3)、碳酸钠、氧气和硫酸为原料生产重铬酸钠(Na2Cr2O7),其主要反应为
①4FeO·Cr2O3+8Na2CO3+7O2 8Na2CrO4+2Fe2O3+8CO2
8Na2CrO4+2Fe2O3+8CO2
②2Na2CrO4+H2SO4 Na2SO4+Na2Cr2O7+H2O
Na2SO4+Na2Cr2O7+H2O
下列说法中正确的是( )
①4FeO·Cr2O3+8Na2CO3+7O2
 8Na2CrO4+2Fe2O3+8CO2
8Na2CrO4+2Fe2O3+8CO2②2Na2CrO4+H2SO4
 Na2SO4+Na2Cr2O7+H2O
Na2SO4+Na2Cr2O7+H2O下列说法中正确的是( )
| A.反应①和②均为氧化还原反应 |
| B.反应①,转移4 mol电子时,被氧化的为O2为1mol |
| C.反应①的氧化剂是O2,还原剂是FeO·Cr2O3 |
| D.生成1 mol Na2Cr2O7时共转移5 mol电子 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】高铁酸钾(K2FeO4)是种环保、高效、多功能饮用水处理剂,制备流程如图所示:
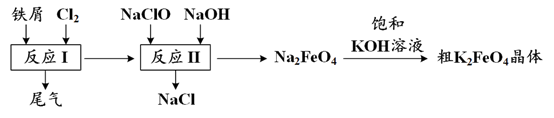
下列叙述错误的是

下列叙述错误的是
| A.反应I不能在常温下进行 |
| B.“尾气”可用FeCl2溶液吸收,其离子方程式为:2Fe2++Cl2=2Fe3++2Cl— |
| C.反应II中氧化剂与还原剂的物质的量之比为2:3 |
| D.最后一步能制取K2FeO4的原因可能是相同温度下K2FeO4的溶解度小于Na2FeO4 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】对下列现象或事实的解释正确的是
| 现象或事实 | 解释 | |
| A | SO2在工业上常用来漂白纸浆、毛丝、草帽辫等 | SO2具有还原性 |
| B | K2FeO4用于自来水的消毒和净化 | Fe3+水解生成胶状物,有消毒和净化作用 |
| C | Na2O2用于呼吸面具中作为O2的来源 | Na2O2是强氧化剂,能氧化CO2生成O2 |
| D | 常温下可用铁、铝制容器盛装浓硫酸或浓硝酸 | 铁、铝表面被氧化为致密的氧化物薄膜,阻止了酸与内层金属的进一步反应 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次



