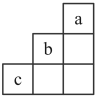
以下有关元素性质的说法不正确的是
A.① ,K,Rb② ,K,Rb② ,P,As③ ,P,As③ ,S,Se④ ,S,Se④ ,P,S元素的电负性随原子序数增大而递增的是④ ,P,S元素的电负性随原子序数增大而递增的是④ |
B.下列原子中,① ② ②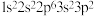 ③ ③ ④ ④ ,对应的第一电离能最大的是④ ,对应的第一电离能最大的是④ |
| C.某元素的逐级电离能分别为738、1451、7733、10540、13630、17995、21703,该元素可能在第三周期第IIA族 |
D.以下原子中,①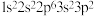 ② ② ③ ③ ④ ④ 半径最大的是① 半径最大的是① |
更新时间:2020-08-11 10:59:25
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】下列事实不能用元素周期律解释的是
| A.气态氢化物的稳定性:HBr>HI | B.在短周期中,金属性最强的元素是钠,非金属性最强的元素是氟 |
| C.向Na2SO3溶液中加盐酸,有气泡产生 | D.镁条、铝片分别与同浓度盐酸反应,Mg的反应更容易 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】已知X、Y、Z、W四种短周期元素在元素周期表中的相对位置如表。下列有关这四种元素的性质的描述不正确的是


| A.与水反应,X比Y剧烈 |
| B.与H2化合,W单质比Z单质容易 |
| C.X形成的碱比Y形成的碱的碱性强 |
| D.W的最高价含氧酸比Z的最高价含氧酸酸性强 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】 是短周期主族元素,
是短周期主族元素, 与其他元素不在同一周期,
与其他元素不在同一周期, 是地壳中含量最多的元素,
是地壳中含量最多的元素, 的基态原子中单电子与成对电子个数比为3:4,Z原子电子总数与
的基态原子中单电子与成对电子个数比为3:4,Z原子电子总数与 原子的最外层电子数相同。下列说法不正确的是
原子的最外层电子数相同。下列说法不正确的是
 是短周期主族元素,
是短周期主族元素, 与其他元素不在同一周期,
与其他元素不在同一周期, 是地壳中含量最多的元素,
是地壳中含量最多的元素, 的基态原子中单电子与成对电子个数比为3:4,Z原子电子总数与
的基态原子中单电子与成对电子个数比为3:4,Z原子电子总数与 原子的最外层电子数相同。下列说法不正确的是
原子的最外层电子数相同。下列说法不正确的是A. 的空间构型为平面三角形 的空间构型为平面三角形 |
B.键角: |
C.第一电离能: |
D.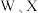 可能形成离子化合物,也可能形成共价化合物 可能形成离子化合物,也可能形成共价化合物 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列说法不正确的是
| A.向配合物[TiCl(H2O)5]Cl2•H2O溶液中加入足量的AgNO3溶液,所有Cl-均被完全沉淀 |
| B.某元素X气态基态原子的逐级电离能(kJ•mol-1)分别为738、1451、7733、10540、13630、17995、21703,当它与氯气反应时可能生成的阳离子是X2+ |
| C.区别晶体与非晶体最科学的方法是对固体进行X射线衍射实验 |
D.PO 的空间结构与VSEPR模型相同 的空间结构与VSEPR模型相同 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列说法正确的是
| A.可以利用质谱仪测得某未知物的结构 |
| B.Cl、Br、Se(硒)的电负性依次减小 |
| C.可燃冰(CH4•8H2O)中甲烷分子和水分子间形成了氢键 |
| D.臭氧分子是非极性分子 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】W、X、Y、Z是原子序数依次增大的短周期主族元素,其中Z元素基态原子L层电子数是电子层数的3倍。这四种元素组成的化合物(结构如图)可用于合成超分子聚合物。下列说法错误的是


| A.XZ2晶体属于共价晶体 | B.元素W、X、Y都可以与Z形成多种化合物 |
| C.电负性:Z>Y>X>W | D.超分子具有自组装和分子识别的特征 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】下列事实的解释不正确的是
| 事实 | 解释 | |
| A | 晶体熔点:HF>HCl | HF分子内H-F键能大于HCl分子内H-Cl键能 |
| B | 向2.0mL浓度均为0.1mol/L的KCl、KI混合溶液中滴加1-2滴0.01mol/LAgNO3溶液,振荡,沉淀呈黄色 | Ksp:AgCl>AgI |
| C | CH 中H-C-H键角比CH 中H-C-H键角比CH 中的大 中的大 | 中心原子的孤电子对数目CH >CH >CH ,孤电子对与成键电子对之间的斥力>成键电子对之间的斥力 ,孤电子对与成键电子对之间的斥力>成键电子对之间的斥力 |
| D | 酸性:CF3COOH>CCl3COOH | 氟的电负性大于氯的电负性,F-C的极性大于Cl-C的性,使-CF3的极性大于-CCl3的极性,导致CF3COOH的羧基中的羟基的极性更大,更易电离出H+ |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次