下表是元素周期表的一部分,请针对表中所列标号为①~⑩的元素回答下列问题。
(1)写出下列元素的符号②____ ③____ ⑥____ ⑧___ ⑩___ 。
(2)非金属性最强的元素是___ ,化合物种类最多的元素是___ 。(填元素符号)
(3)第三周期元素除⑩外原子半径最小的是___ ,元素①-⑨中原子半径最大的是___ 。(填元素符号)
(4)这些元素的最高价氧化物对应水化物中碱性最强的是___ ,具有两性的是___ 。(填化学式)
(5)写出⑤的最高价氧化物对应的水化物与⑧的最高价氧化物的水化物反应的化学反应方程式___ 。
| 族 周期 | IA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ① | ② | ③ | ④ | ||||
| 三 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
(1)写出下列元素的符号②
(2)非金属性最强的元素是
(3)第三周期元素除⑩外原子半径最小的是
(4)这些元素的最高价氧化物对应水化物中碱性最强的是
(5)写出⑤的最高价氧化物对应的水化物与⑧的最高价氧化物的水化物反应的化学反应方程式
更新时间:2020-08-18 17:19:40
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】如图是元素周期表的一部分,主族元素A、B、C、D、E在元素周期表中的位置如图,A元素的单质在空气中含量最高(请用相应的元素符号或化学式作答)。
(1)A简单离子结构示意图_______ 。
(2)C、D、B氢化物的稳定性由大到小排序为_______ 。
(3)设计实验比较D与E非金属性强弱(用离子方程式表示)_______ 。
(4)下列说法不正确的是_______ 。
①C的最高价氧化物能溶于B的氢化物水溶液
②元素A、E的气态氢化物相遇会产生白烟
③B元素形成的其中一种18电子分子,能与A元素形成的一种10电子分子发生氧化还原反应
④原子得电子能力D>E>A
(5)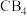 的电子式为
的电子式为_______ ,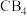 溶于
溶于 溶液的化学方程式
溶液的化学方程式_______ 。
| A | B | ||
| C | D | E |
(2)C、D、B氢化物的稳定性由大到小排序为
(3)设计实验比较D与E非金属性强弱(用离子方程式表示)
(4)下列说法不正确的是
①C的最高价氧化物能溶于B的氢化物水溶液
②元素A、E的气态氢化物相遇会产生白烟
③B元素形成的其中一种18电子分子,能与A元素形成的一种10电子分子发生氧化还原反应
④原子得电子能力D>E>A
(5)
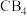 的电子式为
的电子式为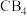 溶于
溶于 溶液的化学方程式
溶液的化学方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】下表是元素周期表短周期的一部分
(1)①~⑦元素中金属性最强的元素是___________ (用元素符号表示)。
(2)④与⑤形成的化合物的电子式为____________ 。
(3)表中元素②、③、⑦最高价含氧酸的酸性由强到弱的顺序是___________ (填化学式)。
(4)第116号元素(元素符号Lv)被中国科学技术名词审定委员会命名为“ ”,该元素在元素周期表中的位置是
”,该元素在元素周期表中的位置是_____________ 。
(5)核内中子数为N的R2+,质量数为A,则ng它的相同价态氧化物中所含的电子的物质的量约为________ mol。
| ① | ||||||||
| ② | ③ | ④ | ||||||
| ⑤ | ⑥ | ⑦ | ⑧ | |||||
(1)①~⑦元素中金属性最强的元素是
(2)④与⑤形成的化合物的电子式为
(3)表中元素②、③、⑦最高价含氧酸的酸性由强到弱的顺序是
(4)第116号元素(元素符号Lv)被中国科学技术名词审定委员会命名为“
 ”,该元素在元素周期表中的位置是
”,该元素在元素周期表中的位置是(5)核内中子数为N的R2+,质量数为A,则ng它的相同价态氧化物中所含的电子的物质的量约为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】表中列出了第三周期几种元素的部分性质:
请按要求回答下列问题:
(1)表中元素原子半径最大的是(写元素符号)___________ 。
(2)a、b、c三种元素形成的氢化物中,其稳定性由强到弱的顺序是(用化学式表示)___________ 。
(3)d、e最高价氧化物对应水化物相互反应的离子方程式为___________ 。
(4)某化学兴趣小组为探究元素性质的递变规律,设计了以下系列实验。
①甲同学为探究同主族元素金属性的递变规律,取绿豆粒大小的钠、钾分别放入到盛有水的烧杯(滴有几滴酚酞溶液)中,通过观察现象得出的结论是___________ 。
②乙同学利用现有药品: 溶液、
溶液、 固体、浓盐酸、
固体、浓盐酸、 ,设计如图装置探究第三周期部分元素非金属性的递变规律。M中所装药品为
,设计如图装置探究第三周期部分元素非金属性的递变规律。M中所装药品为___________ ,装置N中的实验现象为有淡黄色沉淀生成,离子方程式为___________ ,所得结论为___________ 。

| 元素编号 | a | b | c | d | e |
| 电负性 | 3.0 | 2.5 | 2.1 | 1.5 | 0.9 |
| 主要化合价 | -1,+7 | -2,+6 | -3,+5 | +3 | +1 |
(1)表中元素原子半径最大的是(写元素符号)
(2)a、b、c三种元素形成的氢化物中,其稳定性由强到弱的顺序是(用化学式表示)
(3)d、e最高价氧化物对应水化物相互反应的离子方程式为
(4)某化学兴趣小组为探究元素性质的递变规律,设计了以下系列实验。
①甲同学为探究同主族元素金属性的递变规律,取绿豆粒大小的钠、钾分别放入到盛有水的烧杯(滴有几滴酚酞溶液)中,通过观察现象得出的结论是
②乙同学利用现有药品:
 溶液、
溶液、 固体、浓盐酸、
固体、浓盐酸、 ,设计如图装置探究第三周期部分元素非金属性的递变规律。M中所装药品为
,设计如图装置探究第三周期部分元素非金属性的递变规律。M中所装药品为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】A、B、C、D、E为原子序数依次增大的短周期主族元素,其中A原子的最外层电子数是电子层数的2倍,各元素在周期表中的相对位置如图所示:
请回答下列问题:
(1)B在元素周期表中的位置为___________ 。
(2)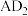 属于火车严禁携带的易燃易爆液体,已知
属于火车严禁携带的易燃易爆液体,已知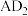 的燃烧热
的燃烧热 为
为 ,写出表示
,写出表示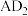 燃烧热的热化学方程式:
燃烧热的热化学方程式:___________ 。
(3)D、E的最高价氧化物对应水化物的酸性由强到弱的顺序为___________ (用化学式表示),结合元素周期律解释其原因:___________ 。
(4)最新合成的 分子结构完美对称(只含单键),具有极强的热稳定性和化学惰性,试画出
分子结构完美对称(只含单键),具有极强的热稳定性和化学惰性,试画出 的结构式:
的结构式:___________ 。
| A | B | C | |
| D | E |
(1)B在元素周期表中的位置为
(2)
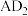 属于火车严禁携带的易燃易爆液体,已知
属于火车严禁携带的易燃易爆液体,已知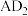 的燃烧热
的燃烧热 为
为 ,写出表示
,写出表示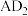 燃烧热的热化学方程式:
燃烧热的热化学方程式:(3)D、E的最高价氧化物对应水化物的酸性由强到弱的顺序为
(4)最新合成的
 分子结构完美对称(只含单键),具有极强的热稳定性和化学惰性,试画出
分子结构完美对称(只含单键),具有极强的热稳定性和化学惰性,试画出 的结构式:
的结构式:
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】按要求填空:
(1)在第二周期中(稀有气体除外),第一电离能最大的元素的原子结构示意图是_______ 。
(2)第四周期元素中,4p轨道半充满的元素符号是_______ ,价电子层中s电子数与d电子数相同的元素名称是_______ 。
(3)中国古代四大发明之一的黑火药,它的爆炸反应方程式为: (未配平)
(未配平)
①写出配平的化学方程式_______ 。
②用电子式表示 的形成过程
的形成过程_______ 。
③除K、S外,由上述方程式中出现的元素形成的简单氢化物的稳定性从大到小依次为_______ 。
④写出K的基态电子排布式_______ 。
(1)在第二周期中(稀有气体除外),第一电离能最大的元素的原子结构示意图是
(2)第四周期元素中,4p轨道半充满的元素符号是
(3)中国古代四大发明之一的黑火药,它的爆炸反应方程式为:
 (未配平)
(未配平)①写出配平的化学方程式
②用电子式表示
 的形成过程
的形成过程③除K、S外,由上述方程式中出现的元素形成的简单氢化物的稳定性从大到小依次为
④写出K的基态电子排布式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】X、Y、Z、W为短周期的四种元素,其最高正价依次为+1、+4、+5、+7,核电荷数按照Y、Z、X、W的顺序增大。已知Y与Z的原子次外层的电子数均为2,W、X的原子次外层的电子数均为8。
(1)写出W元素在周期表中的位置_______ 。写出Z元素在周期表中的位置_________ 。
(2)写出X的最高价氧化物与Z的最高价氧化物对应水化物反应的化学方程式_______ 。
(3)X元素与氧元素形成的两种化合物分别为________________ (填化学式)。
(4)Y和Z元素最高价氧化物对应水化物的酸性强弱顺序为(用化学式表示):_______ 。
(1)写出W元素在周期表中的位置
(2)写出X的最高价氧化物与Z的最高价氧化物对应水化物反应的化学方程式
(3)X元素与氧元素形成的两种化合物分别为
(4)Y和Z元素最高价氧化物对应水化物的酸性强弱顺序为(用化学式表示):
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】W、X、Y、Z、M五种主族元素,它们在周期表中位置如图所示,
(1)Z在元素周期表中的位置:___________ 。
(2)以上元素中金属性最强的为___________ (用元素符号表示);最高价氧化物对应水化物酸性最强的为___________ (用化学式表示)。
(3)X、W形成的化合物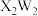 中存在的化学键类型有:
中存在的化学键类型有:___________
(4)比较X、Y的简单离子的半径大小:___________ (用离子符号表示)。
| W | |||||||
| X | Y | Z | M |
(2)以上元素中金属性最强的为
(3)X、W形成的化合物
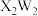 中存在的化学键类型有:
中存在的化学键类型有:(4)比较X、Y的简单离子的半径大小:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】X、Y、Z、W为1~18号中的四种元素,其最高正价依次为+1、+4、+5、+7,核电荷数按照Y、Z、X、W的顺序增大。已知Y与Z的原子次外层的电子数均为2,W、X的原子次外层的电子数均为8。
(1)写出元素的名称:X_____ ,Z_____ 。
(2)写出X的最高价氧化物与Z的最高价氧化物对应水化物反应的化学方程式:_____ 。
(3)按碱性减弱、酸性增强的顺序写出各元素最高价氧化物对应水化物的化学式:_____ 、_____ 、_____ 、_____ 。
(1)写出元素的名称:X
(2)写出X的最高价氧化物与Z的最高价氧化物对应水化物反应的化学方程式:
(3)按碱性减弱、酸性增强的顺序写出各元素最高价氧化物对应水化物的化学式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】4种相邻主族短周期元素的相对位置如下表,元素x的原子核外电子数是m的2倍,y的氧化物具有两性。
回答下列问题:
(1)元素x在周期表中的位置是_______________________ ,其单质可采用电解法方法制备,其反应方程式为_________________________________ 。
(2)m、n、y三种元素最高价氧化物的水化物中,酸性最强的是___________ ,碱性最强的是________________ 。 填化学式
填化学式
(3)气体分子 的电子式为
的电子式为___________________________ , 称为拟卤素,性质与卤素类似,其与氢氧化钠溶液反应的化学方程式为
称为拟卤素,性质与卤素类似,其与氢氧化钠溶液反应的化学方程式为_________________ 。
| m | n | ||
| x | y |
(1)元素x在周期表中的位置是
(2)m、n、y三种元素最高价氧化物的水化物中,酸性最强的是
 填化学式
填化学式
(3)气体分子
 的电子式为
的电子式为 称为拟卤素,性质与卤素类似,其与氢氧化钠溶液反应的化学方程式为
称为拟卤素,性质与卤素类似,其与氢氧化钠溶液反应的化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】X、Y、Z三种常见的短周期元素可以形成XY2、Z2Y、XY3、Z2Y2、Z2X等化合物,已知Y的离子和Z的离子有相同的电子层结构,X离子比Y离子多一个电子层。试回答:
(1)写出X、Y、Z三种元素的符号和名称:_____________ 、_______ 、_______ ;
(2)分析Z2Y2中含有的化学键类型:_______ ;
(3)写出Z2Y2与二氧化碳反应的方程式:_____________________ ;
(4)用电子式表示X和Z两元素形成化合物的过程:__________________ 。
(1)写出X、Y、Z三种元素的符号和名称:
(2)分析Z2Y2中含有的化学键类型:
(3)写出Z2Y2与二氧化碳反应的方程式:
(4)用电子式表示X和Z两元素形成化合物的过程:
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】短周期主族元素X、Y、Z、M、W的原子序数依次递增,X的简单阴离子与He原子具有相同的电子层结构,Y基态原子未成对电子数在所处周期中最多,M是地壳中含量最多的金属元素,W原子最外层电子数是K层电子数的3倍,Z、W同主族。
(1)下列说法正确的是______ 。
A.原子半径: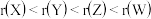
B.X、Y、Z三种元素只能形成共价化合物
C.W的简单气态氢化物的热稳定性比Z的强
D.M的单质能溶于W的最高氧化物对应水化物的稀溶液
(2)X、Y、Z、M、W五种元素中:
①电负性最小的元素是______  填元素的符号,下同
填元素的符号,下同 ,第一电离能最大的元素是
,第一电离能最大的元素是______ 。
②Z原子的电子排布图 轨道表示式
轨道表示式 为
为______ ,W的电子排布式为______ 。
③如图可以表示Y单质分子中电子云重叠方式的是______ 。
A. B.
B.  C.
C.  D.
D. 
1mol Y单质分子中含有 键的数目为
键的数目为______ 。
④Y的简单气态氢化物极易溶于水,其原因是______ ;一种含碳元素的阴离子R与Y的简单气态氢化物互为等电子体,写出R的电子式:______ 。
⑤向W的简单气态氢化物的水溶液中通入Z的单质,有W的单质析出,可以验证Z 的非金属性强于W,该反应的离子方程式为______ 。
(3)向含有M简单离子的溶液中加入过量NaOH溶液,可生成 。
。
①不考虑空间构型 要标出配位键,M要用元素符号表示
要标出配位键,M要用元素符号表示 ,
, 的结构可用示意图表示为
的结构可用示意图表示为______ 。
② 的空间构型为
的空间构型为______ ,其M原子轨道的杂化类型为______ 。
(4)铁、铜和Y元素可生成晶胞结构图1 所示的化合物,该化合物的化学式为______ 。
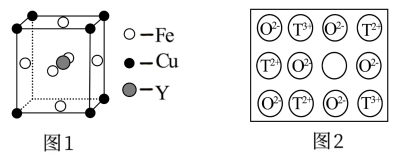
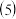 天然的和绝大部分人工制备的晶体都存在各种缺陷。如某过渡元素T的基态原子中的未成对电子数恰好等于最外层电子数;而其3d能级上的电子数等于最外层电子数的4倍。这种T的氧化物的晶胞结构就存在缺陷
天然的和绝大部分人工制备的晶体都存在各种缺陷。如某过渡元素T的基态原子中的未成对电子数恰好等于最外层电子数;而其3d能级上的电子数等于最外层电子数的4倍。这种T的氧化物的晶胞结构就存在缺陷 如图2所示
如图2所示 。
。
①基态 的外围电子排布式为
的外围电子排布式为______ ;若该T的氧化物晶体中每有1个 空缺,则应有
空缺,则应有______ 个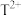 倍
倍 所取代,才能使晶体仍呈电中性。
所取代,才能使晶体仍呈电中性。
②若某T的氧化物晶体样品中 与
与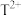 的离子数之比为1:11,则该晶体的化学式为
的离子数之比为1:11,则该晶体的化学式为______ 。
(1)下列说法正确的是
A.原子半径:
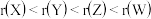
B.X、Y、Z三种元素只能形成共价化合物
C.W的简单气态氢化物的热稳定性比Z的强
D.M的单质能溶于W的最高氧化物对应水化物的稀溶液
(2)X、Y、Z、M、W五种元素中:
①电负性最小的元素是
 填元素的符号,下同
填元素的符号,下同 ,第一电离能最大的元素是
,第一电离能最大的元素是②Z原子的电子排布图
 轨道表示式
轨道表示式 为
为③如图可以表示Y单质分子中电子云重叠方式的是
A.
 B.
B.  C.
C.  D.
D. 
1mol Y单质分子中含有
 键的数目为
键的数目为④Y的简单气态氢化物极易溶于水,其原因是
⑤向W的简单气态氢化物的水溶液中通入Z的单质,有W的单质析出,可以验证Z 的非金属性强于W,该反应的离子方程式为
(3)向含有M简单离子的溶液中加入过量NaOH溶液,可生成
 。
。①不考虑空间构型
 要标出配位键,M要用元素符号表示
要标出配位键,M要用元素符号表示 ,
, 的结构可用示意图表示为
的结构可用示意图表示为②
 的空间构型为
的空间构型为(4)铁、铜和Y元素可生成晶胞结构图1 所示的化合物,该化合物的化学式为

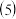 天然的和绝大部分人工制备的晶体都存在各种缺陷。如某过渡元素T的基态原子中的未成对电子数恰好等于最外层电子数;而其3d能级上的电子数等于最外层电子数的4倍。这种T的氧化物的晶胞结构就存在缺陷
天然的和绝大部分人工制备的晶体都存在各种缺陷。如某过渡元素T的基态原子中的未成对电子数恰好等于最外层电子数;而其3d能级上的电子数等于最外层电子数的4倍。这种T的氧化物的晶胞结构就存在缺陷 如图2所示
如图2所示 。
。①基态
 的外围电子排布式为
的外围电子排布式为 空缺,则应有
空缺,则应有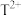 倍
倍 所取代,才能使晶体仍呈电中性。
所取代,才能使晶体仍呈电中性。②若某T的氧化物晶体样品中
 与
与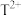 的离子数之比为1:11,则该晶体的化学式为
的离子数之比为1:11,则该晶体的化学式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】有U、V、W、X四种前三周期元素,原子序数依次增大,其相关信息如下表:
请回答下列问题:
(1)U、V两种元素组成的一种化合物甲是重要的化工原料,常把它的产量作为衡量石油化工发展水平的标志,则甲分子的空间构型为________ 。
(2)写出W单质的结构式___________ ,其化学键为________ 性共价键:W最简单气态氢化物的电子式为___________ ,分子的空间构型是___________ ,其化学键为___________ 性共价键。
(3)X在周期表中的位置是_______ ,该主族元素的气态氢化物中,沸点最低的是__________ (填化学式)
(4)乙和丙分别是V和X的某种氢化物,这两种氢化物分子中含有有18个电子。乙和丙的化学式分别是________ 、________ 。
| 元素编号 | 相关信息 |
| U | 所处的周期数、族序数分别与其原子序数相等 |
| V | 外层电子数是最内层电子数的两倍 |
| W | 单质中有三对共用电子对 |
| X | 是地壳中含量最多的元素 |
请回答下列问题:
(1)U、V两种元素组成的一种化合物甲是重要的化工原料,常把它的产量作为衡量石油化工发展水平的标志,则甲分子的空间构型为
(2)写出W单质的结构式
(3)X在周期表中的位置是
(4)乙和丙分别是V和X的某种氢化物,这两种氢化物分子中含有有18个电子。乙和丙的化学式分别是
您最近一年使用:0次



