按要求回答下列问题:
I.某温度时,在2L密闭容器中某一反应中气体A、B的物质的量随时间变化的曲线如下图所示,回答下列问题:
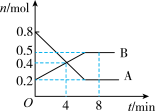
(1)该反应的化学方程式为________ 。
(2)0~4min内,用A表示反应速率v(A)=______ 。
(3)反应达平衡时容器内混合气体的平均相对分子质量比起始时______ (填“变大”、“变小”或“相等”)。
(4)下列措施能加快反应速率的是_______ 。
A.缩小体积,使压强增大 B.恒温恒容充入He气 C.恒温恒压充入He气 D.使用催化剂
Ⅱ.化学能与电能之间可以相互转化。
(1)直接提供电能的反应一般是放热反应,下列反应能设计成原电池的是_________
A.Ba(OH)2·8H2O与NH4Cl反应 B.氢氧化钠与稀盐酸反应
C.灼热的炭与CO2反应 D.H2与Cl2燃烧反应
(2)氢氧燃料电池是符合绿色化学理念的新型发电装置。下图为电池示意图,该电池电极表面镀了一层细小的铂粉,铂吸附气体的能力强,性质稳定。请回答:
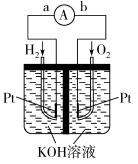
①电池的负极反应式为:_______ 。
②电池工作时OH-向移动_______ (填“正极”或“负极”)。
③正极上消耗标况下4.48L气体时,转移电子的数目为________ 。
I.某温度时,在2L密闭容器中某一反应中气体A、B的物质的量随时间变化的曲线如下图所示,回答下列问题:

(1)该反应的化学方程式为
(2)0~4min内,用A表示反应速率v(A)=
(3)反应达平衡时容器内混合气体的平均相对分子质量比起始时
(4)下列措施能加快反应速率的是
A.缩小体积,使压强增大 B.恒温恒容充入He气 C.恒温恒压充入He气 D.使用催化剂
Ⅱ.化学能与电能之间可以相互转化。
(1)直接提供电能的反应一般是放热反应,下列反应能设计成原电池的是
A.Ba(OH)2·8H2O与NH4Cl反应 B.氢氧化钠与稀盐酸反应
C.灼热的炭与CO2反应 D.H2与Cl2燃烧反应
(2)氢氧燃料电池是符合绿色化学理念的新型发电装置。下图为电池示意图,该电池电极表面镀了一层细小的铂粉,铂吸附气体的能力强,性质稳定。请回答:

①电池的负极反应式为:
②电池工作时OH-向移动
③正极上消耗标况下4.48L气体时,转移电子的数目为
更新时间:2020-08-21 17:42:01
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】下图表示8000C时A、B、C三种气体的物质的量浓度随时间变化的情况,t时各组分浓度不再变化。试回答:
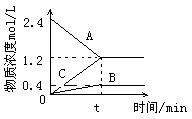
(1)该反应的反应物是___________________ ,达平衡时其转化率是______________
(2)该反应的化学方程式是___________________________________________
(3)若t是2min,A物质的平均反应速率是_________________ ,B的反应速率是__________

(1)该反应的反应物是
(2)该反应的化学方程式是
(3)若t是2min,A物质的平均反应速率是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】与研究物质变化一样,研究化学反应中的能量变化,同样具有重要意义。请回答:
(1)已知二甲醚(CH3OCH3,常温下呈气态),H2的燃烧热分别为1455kJ/mol、286kJ/mol。请写出表示二甲醚燃烧热的热化学方程式____ 。利用二甲醚制取H2,总反应为CH3OCH3(g)+3H2O(g) 6H2(g)+2CO2(g)。已知H2O(g)=H2O(l) △H=-44kJ/mol,则总反应的△H=
6H2(g)+2CO2(g)。已知H2O(g)=H2O(l) △H=-44kJ/mol,则总反应的△H=___ 。总反应能自发进行的条件是___ (选填“高温”“低温”或“任意温度”)。
(2)二甲醚制H2的总反应分两步完成:
二甲醚水解:CH3OCH3(g)+H2O(g) 2CH3OH(g) 活化能Ea1
2CH3OH(g) 活化能Ea1
甲醇与水蒸气重整:CH3OH(g)+H2O(g) CO2(g)+3H2(g) 活化能Ea2
CO2(g)+3H2(g) 活化能Ea2
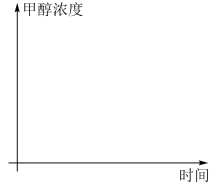
已知Ea1远小于Ea2。在恒温恒容容器内,一甲醚与水按1∶3投料进行制氢,请在图中画出甲醇(CH3OH)浓度随时间变化的曲线图___ 。___ 。
(1)已知二甲醚(CH3OCH3,常温下呈气态),H2的燃烧热分别为1455kJ/mol、286kJ/mol。请写出表示二甲醚燃烧热的热化学方程式
 6H2(g)+2CO2(g)。已知H2O(g)=H2O(l) △H=-44kJ/mol,则总反应的△H=
6H2(g)+2CO2(g)。已知H2O(g)=H2O(l) △H=-44kJ/mol,则总反应的△H=(2)二甲醚制H2的总反应分两步完成:
二甲醚水解:CH3OCH3(g)+H2O(g)
 2CH3OH(g) 活化能Ea1
2CH3OH(g) 活化能Ea1甲醇与水蒸气重整:CH3OH(g)+H2O(g)
 CO2(g)+3H2(g) 活化能Ea2
CO2(g)+3H2(g) 活化能Ea2已知Ea1远小于Ea2。在恒温恒容容器内,一甲醚与水按1∶3投料进行制氢,请在图中画出甲醇(CH3OH)浓度随时间变化的曲线图

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】NH3和O2可以形成碱性燃料电池,结构如图所示。
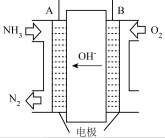
(1)电极A是_______ (填“正极”或“负极”),其电极反应式为_______ 。
(2)若反应生成28 gN2,则该燃料电池理论上消耗的O2的体积(在标准状况下)为_______ L。
(3)若用该电池电解精炼铜,通氧气一端的电极应接_______ (填“纯铜”或“粗铜”)。若用CuSO4溶液做电解液电解精练铜,则电解一段时间后CuSO4溶液的浓度_______ (填增大、变小、不变)。

(1)电极A是
(2)若反应生成28 gN2,则该燃料电池理论上消耗的O2的体积(在标准状况下)为
(3)若用该电池电解精炼铜,通氧气一端的电极应接
您最近一年使用:0次
【推荐2】(1)肼(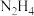 )-空气燃料电池是一种碱性电池,该电池放电时,负极的反应式为
)-空气燃料电池是一种碱性电池,该电池放电时,负极的反应式为_____________________ 。
(2)科研人员新近开发一种由甲醇和氧气为燃料,强碱溶液作电解质溶液的新型手机电池,可供手机连续使用一个月。则通入甲醇的是_______ 填(“正”或“负”)极,写出该电池的负极反应式:_____________________ 。
(3)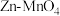 干电池应用广泛,电解质溶液是
干电池应用广泛,电解质溶液是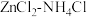 混合溶液。
混合溶液。
①该电池的负极材料是______ 。电池工作时,电子流向__________ 填(“正”或“负”)极。
②若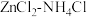 混合溶液中含有杂质
混合溶液中含有杂质 ,会加速某电极的腐蚀,其主要原因是
,会加速某电极的腐蚀,其主要原因是_______ 。
③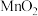 的生产方法之一是以石墨为电极,电解酸化的
的生产方法之一是以石墨为电极,电解酸化的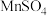 溶液。阳极的主要电极反应式是
溶液。阳极的主要电极反应式是_____________________ 。若电路中通过4mol电子,标准状况下产生气体的物质的量为_________ 。
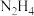 )-空气燃料电池是一种碱性电池,该电池放电时,负极的反应式为
)-空气燃料电池是一种碱性电池,该电池放电时,负极的反应式为(2)科研人员新近开发一种由甲醇和氧气为燃料,强碱溶液作电解质溶液的新型手机电池,可供手机连续使用一个月。则通入甲醇的是
(3)
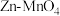 干电池应用广泛,电解质溶液是
干电池应用广泛,电解质溶液是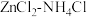 混合溶液。
混合溶液。①该电池的负极材料是
②若
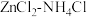 混合溶液中含有杂质
混合溶液中含有杂质 ,会加速某电极的腐蚀,其主要原因是
,会加速某电极的腐蚀,其主要原因是③
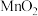 的生产方法之一是以石墨为电极,电解酸化的
的生产方法之一是以石墨为电极,电解酸化的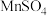 溶液。阳极的主要电极反应式是
溶液。阳极的主要电极反应式是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】科学家发明的一种光化学电池可充分利用南海太阳能,其结构如图所示,电池总反应为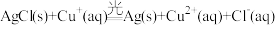

①Cl-的迁移方向为___________________ (填“正极→负极”或“负极→正极”)。
②正极的电极反应式为_________________________________ 。
③若用该电池为手机充电,该手机电池容量为3200 mA,2小时能将电池充满,则理论上消耗AgCl的质量为_______ g(保留一位小数)(已知:1库仑约为1.0×10-5mol电子所带的电量)。
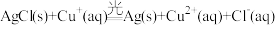

①Cl-的迁移方向为
②正极的电极反应式为
③若用该电池为手机充电,该手机电池容量为3200 mA,2小时能将电池充满,则理论上消耗AgCl的质量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】Ⅰ.“价-类”二维图是化学研究的重要手段。如图是S元素的常见化合价与部分物质类别的对应关系(G、H均为正盐)。回答下列问题:_____ (填标号)。
A.将D通入 溶液中,溶液中无明显现象,再通入
溶液中,溶液中无明显现象,再通入 ,则溶液中会出现白色沉淀
,则溶液中会出现白色沉淀
B.F的浓溶液能与B反应同时生成A和D
C.将足量的F加入含H的溶液中,可以闻到臭鸡蛋气味
(2)请写出用生石灰除去燃煤产生的D,直接生成G的化学方程式_____ 。
Ⅱ.水是生命之源,也是化学反应中的主角。
关于 的反应,已知断开
的反应,已知断开 键、
键、 键、
键、 键分别需要吸收436kJ、498kJ、463kJ的能量。
键分别需要吸收436kJ、498kJ、463kJ的能量。
(3)若有 生成,需要
生成,需要_____ 。(填“吸收”或“放出”)热量_____ kJ。
(4)化学反应过程中伴随着能量变化,下列变化中属于吸热反应的是_____ (填序号)。
①铝片与稀盐酸的反应 ②食物因氧化而腐败 ③甲烷在氧气中的燃烧反应
④ 固体溶于水⑤碳酸氢钠与盐酸的反应 ⑥
固体溶于水⑤碳酸氢钠与盐酸的反应 ⑥ 与
与 反应
反应
其中⑥中发生的化学方程式为_____ 。
Ⅲ.天然气(主要成分 )和氧气的反应为放热的氧化还原反应,可将其设计成燃料电池,构造如图所示。
)和氧气的反应为放热的氧化还原反应,可将其设计成燃料电池,构造如图所示。_____

A.将D通入
 溶液中,溶液中无明显现象,再通入
溶液中,溶液中无明显现象,再通入 ,则溶液中会出现白色沉淀
,则溶液中会出现白色沉淀B.F的浓溶液能与B反应同时生成A和D
C.将足量的F加入含H的溶液中,可以闻到臭鸡蛋气味
(2)请写出用生石灰除去燃煤产生的D,直接生成G的化学方程式
Ⅱ.水是生命之源,也是化学反应中的主角。
关于
 的反应,已知断开
的反应,已知断开 键、
键、 键、
键、 键分别需要吸收436kJ、498kJ、463kJ的能量。
键分别需要吸收436kJ、498kJ、463kJ的能量。(3)若有
 生成,需要
生成,需要(4)化学反应过程中伴随着能量变化,下列变化中属于吸热反应的是
①铝片与稀盐酸的反应 ②食物因氧化而腐败 ③甲烷在氧气中的燃烧反应
④
 固体溶于水⑤碳酸氢钠与盐酸的反应 ⑥
固体溶于水⑤碳酸氢钠与盐酸的反应 ⑥ 与
与 反应
反应其中⑥中发生的化学方程式为
Ⅲ.天然气(主要成分
 )和氧气的反应为放热的氧化还原反应,可将其设计成燃料电池,构造如图所示。
)和氧气的反应为放热的氧化还原反应,可将其设计成燃料电池,构造如图所示。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】化学电源在生产生活中有着广泛的应用,请回答下列问题:
(1)根据构成原电池的本质判断,下列化学(或离子)方程式正确且能设计成原电池的是_______(填字母,下同)。
(2)为了探究化学反应中的能量变化,某同学设计了如下两个实验(如图)。有关反应一段时间后的实验现象,下列说法正确的是_______。
(3)请利用反应“Cu+2Ag+=Cu2++2Ag”设计一个化学电池(正极材料用碳棒),该电池的负极材料是_______ ,发生的电极反应是_______ ,电解质溶液是_______ 。
(4)正极上出现的现象是_______ 。
(5)若导线上转移电子1 mol,则生成银_______  。
。
(1)根据构成原电池的本质判断,下列化学(或离子)方程式正确且能设计成原电池的是_______(填字母,下同)。
A.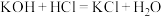 | B. |
C.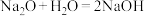 | D. |
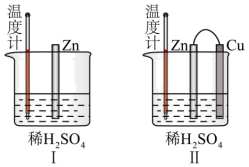
| A.图Ⅰ中温度计的示数高于图Ⅱ的示数 |
| B.图Ⅰ和图Ⅱ中温度计的示数相等,且均高于室温 |
| C.图Ⅰ和图Ⅱ的气泡均产生于锌棒表面 |
| D.图Ⅱ中产生气体的速率比Ⅰ慢 |
(4)正极上出现的现象是
(5)若导线上转移电子1 mol,则生成银
 。
。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】回答下列问题
(1)将下列物质进行分类:①CH3CH2CH2CH3和(CH3)2CHCH3;②红磷与白磷、③乙醇(CH3CH2OH)与二甲醚(CH3OCH3)、④金刚石与石墨、⑤冰与水、⑥16O与18O、⑦CH2=CH2和CH3CH=CH2;⑧CH3CH2CH2CH(C2H5)CH3和CH3CH2CH2CH(CH3)C2H5,用数字序号回答下列问题:
A.互为同素异形体的是_________________ 。
B.互为同分异构体的是_________________ 。
C.属于同位素的是_________________ 。
D.属于同一种化合物的是_________________ 。
E.互为同系物的是_________________ 。
(2)分子中含有22个共价键的烷烃为_________________ (填分子式);该物质有多种同分异构体,其中主链含有五个碳原子,有两个甲基作支链,符合条件的烷烃有_________________ 种;
(3)分析下列烃分子,完成填空。
①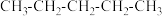 ②
②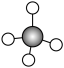
i写出①有3个-CH3的同分异构体的结构简式:_________________ 。
ii②为甲烷的_________________ 模型
(4)某种燃料电池的工作原理示意如图所示,a、b均为惰性电极。
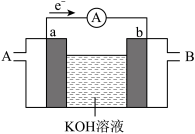
①假设使用的“燃料”是氢气(H2),则b极的电极反应式为_________________ 。
②假设使用的“燃料”是甲醇(CH3OH),则a极的电极反应式为_________________ 。
如果消耗甲醇160g,假设化学能完全转化为电能,则转移电子的数目为________ 。
(1)将下列物质进行分类:①CH3CH2CH2CH3和(CH3)2CHCH3;②红磷与白磷、③乙醇(CH3CH2OH)与二甲醚(CH3OCH3)、④金刚石与石墨、⑤冰与水、⑥16O与18O、⑦CH2=CH2和CH3CH=CH2;⑧CH3CH2CH2CH(C2H5)CH3和CH3CH2CH2CH(CH3)C2H5,用数字序号回答下列问题:
A.互为同素异形体的是
B.互为同分异构体的是
C.属于同位素的是
D.属于同一种化合物的是
E.互为同系物的是
(2)分子中含有22个共价键的烷烃为
(3)分析下列烃分子,完成填空。
①
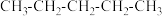 ②
②
i写出①有3个-CH3的同分异构体的结构简式:
ii②为甲烷的
(4)某种燃料电池的工作原理示意如图所示,a、b均为惰性电极。

①假设使用的“燃料”是氢气(H2),则b极的电极反应式为
②假设使用的“燃料”是甲醇(CH3OH),则a极的电极反应式为
如果消耗甲醇160g,假设化学能完全转化为电能,则转移电子的数目为
您最近一年使用:0次

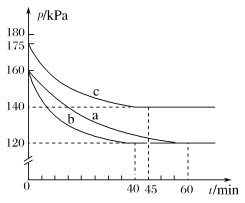
 AX5(g)在容积为10 L的密闭容器中进行。起始时AX3和X2均为0.2 mol。反应在不同条件下进行,反应体系总压强随时间的变化如图所示。
AX5(g)在容积为10 L的密闭容器中进行。起始时AX3和X2均为0.2 mol。反应在不同条件下进行,反应体系总压强随时间的变化如图所示。