H2S燃料电池示意图如图所示,其工作原理为2H2S(g)+O2(g)=S2(s)+2H2O(l) △H=-632kJ/mol。下列说法错误的是( )
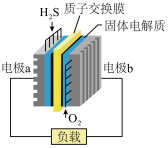

| A.电路中每通过4mol电子,电池会产生632kJ热量 |
| B.电池工作时,电子从电极a经导线流向电极b |
| C.电极a上发生的电极反应为2H2S-4e-=S2+4H+ |
| D.每32gO2参与反应,有4molH+经质子交换膜进入正极区 |
更新时间:2020-08-28 10:43:25
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】将锌片和铜片插入稀硫酸,构成的电池工作原理如图所示,电池工作时,有关说法正确的是
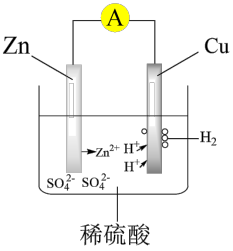

| A.将电能转化为化学能 |
| B.锌片和铜片质量均逐渐减小 |
| C.电子从铜片经导线流向锌片 |
| D.铜是正极,电极反应:2H++2e-=H2↑ |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列有关原电池原理的叙述正确的是
| A.原电池工作时,活泼金属一定作负极 |
| B.原电池工作时,阳离子向负极移动 |
| C.原电池工作时,电解质溶液不一定参加电极反应 |
| D.原电池工作时,电子由负极经电解质溶液流向正极 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】流动电池是一种新型电池,其主要特点是可以通过电解质溶液的循环流动,在电池外部调节电解质溶液,以保持电池内部电极周围溶液浓度的稳定。某种流动电池装置如图所示,电池总反应为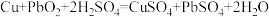 。下列说法不正确的是
。下列说法不正确的是
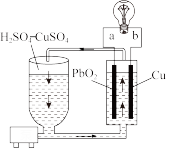
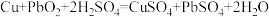 。下列说法不正确的是
。下列说法不正确的是
| A.a为正极,b为负极 |
B.该电池工作时 电极附近溶液的pH增大 电极附近溶液的pH增大 |
C.b极的电极反应为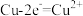 |
| D.电流由b极流出,经导线流向a极 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】微生物脱盐电池是一种高效、经济的能源装置,利用微生物处理有机废水获得电能,同时可实现海水淡化。现以NaCl溶液模拟海水,采用惰性电极,用如图装置处理有机废水(以含 的溶液为例)。下列说法不正确的是
的溶液为例)。下列说法不正确的是
 的溶液为例)。下列说法不正确的是
的溶液为例)。下列说法不正确的是
A.负极反应为 |
| B.隔膜1为阴离子交换膜,隔膜2为阳离子交换膜 |
| C.当电路中转移2mol电子时,模拟海水理论上除盐58.5g |
| D.电池工作一段时间后,正、负极产生气体在同温同压下的体积之比为2:1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】研究发现,在酸性乙醇燃料电池中加入硝酸,可使电池持续大电流放电,其工作原理如图所示。下列说法错误的是(已知F=96500C·mol-1)


| A.X为质子交换膜 |
| B.加入HNO3可降低正极反应的活化能 |
C.正极区反应为4 +12e-+16H+=4NO↑+8H2O、 4NO +3O2 + 2H2O=4HNO3 +12e-+16H+=4NO↑+8H2O、 4NO +3O2 + 2H2O=4HNO3 |
| D.若该电池以电流强度IA持续放电20 min,则理论上消耗C2H5OH约0. 002 mol |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列原电池装置中,正极发生为O2+2H2O+4e-=4OH-反应的是
A. | B. |
C. | D.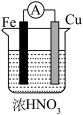 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】一种硝酸盐还原制 的装置如图,初始时离子交换膜两侧溶液质量相同,查阅资料得知阴离子交换膜只允许阴离子通过,不允许阳离子和其他分子通过。下列说法正确的是
的装置如图,初始时离子交换膜两侧溶液质量相同,查阅资料得知阴离子交换膜只允许阴离子通过,不允许阳离子和其他分子通过。下列说法正确的是
 的装置如图,初始时离子交换膜两侧溶液质量相同,查阅资料得知阴离子交换膜只允许阴离子通过,不允许阳离子和其他分子通过。下列说法正确的是
的装置如图,初始时离子交换膜两侧溶液质量相同,查阅资料得知阴离子交换膜只允许阴离子通过,不允许阳离子和其他分子通过。下列说法正确的是
A.石墨电极发生的反应为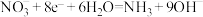 |
B.锌电极表面的电极反应式为 |
C.电路中每转移 的同时有1mol阴离子通过离子交换膜 的同时有1mol阴离子通过离子交换膜 |
| D.电路中转移0.8mol电子时,负极增加26g |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】一种新型中温全瓷铁-空气电池,其结构如图所示。下列有关该电池放电时的说法错误的是


| A.a电极上发生还原反应 |
B.负极的电极反应式为 |
C.铁表面发生的反应为 |
| D.若标准状况下33.6L空气参与反应,电路中理论上有6mol电子转移 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】“除氢气外,烃、肼、甲醇、氨、煤气等液体或气体,均可作燃料电池的燃料”。已知肼燃烧时发生下列反应,N2H4+O2 N2+2H2O。以Pt为电极,以硫酸为电解质溶液组成肼燃料电池,下列关于肼燃料电池的说法中不正确的是 )
N2+2H2O。以Pt为电极,以硫酸为电解质溶液组成肼燃料电池,下列关于肼燃料电池的说法中不正确的是 )
 N2+2H2O。以Pt为电极,以硫酸为电解质溶液组成肼燃料电池,下列关于肼燃料电池的说法中不正确的是 )
N2+2H2O。以Pt为电极,以硫酸为电解质溶液组成肼燃料电池,下列关于肼燃料电池的说法中不正确的是 )| A.肼是燃料电池的负极反应物,O2是正极反应物 |
| B.肼燃料电池的正极反应为 O2 + 2H2O + 4e-= 4OH- |
| C.肼燃料电池的负极反应为:N2H4 —4e—=N2↑+4H+ |
| D.电池工作过程中H+向正极移动,但H+物质的量不变 |
您最近一年使用:0次

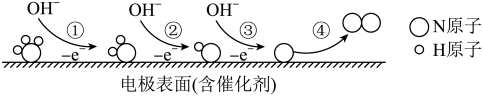
 键断裂
键断裂
 ,电解质为熔融的
,电解质为熔融的 ,工作温度为600~700℃。已知该电池的总反应为
,工作温度为600~700℃。已知该电池的总反应为 ,负极的电极反应为
,负极的电极反应为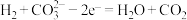 。下列推断正确的是
。下列推断正确的是
 向负极移动
向负极移动

