如图是实验室所用盐酸试剂瓶上标签的部分内容,请仔细阅读后计算:

(1)欲配制溶质质量分数为5%的稀盐酸溶液200g,需要溶质质量分数为37%的浓盐酸________ 毫升(结果保留小数点后一位) 。
(2)若该试剂瓶中HCl的物质的量n=5.9mol,试求该溶液中溶质的质量为__________ 。

(1)欲配制溶质质量分数为5%的稀盐酸溶液200g,需要溶质质量分数为37%的浓盐酸
(2)若该试剂瓶中HCl的物质的量n=5.9mol,试求该溶液中溶质的质量为
更新时间:2020-09-02 07:51:20
|
相似题推荐
计算题
|
适中
(0.65)
解题方法
【推荐1】将32g铜与100mL一定浓度的硝酸反应,铜完全溶解,产生的NO和NO2混合气体在标准状况下的体积为11.2L。
请回答:
(1)NO气体与NO2气体体积比为___ 。
(2)将产生的气体全部逸出后向溶液中加入VmLamol/LNaOH溶液,恰好使溶液中的铜离子全部转化为沉淀,则原硝酸溶液的浓度为__ mol/L(用V和a表示)。
请回答:
(1)NO气体与NO2气体体积比为
(2)将产生的气体全部逸出后向溶液中加入VmLamol/LNaOH溶液,恰好使溶液中的铜离子全部转化为沉淀,则原硝酸溶液的浓度为
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】现有碳酸钠和氯化钠的混合物15g,将其放入烧杯中加入100g水,使其完全溶解。向所得溶液中加入溶质质量分数为9.8%的稀硫酸,烧杯中溶液的质量与加入稀硫酸的质量关系如图所示,请回答下列问题。

(1)B点时烧杯中溶液含有的阳离子是_______ (填离子符号)。
(2)恰好完全反应时加入稀硫酸的质量为_______ g。
(3)混合物中氯化钠的质量是_______ 克(写出具体计算过程)?

(1)B点时烧杯中溶液含有的阳离子是
(2)恰好完全反应时加入稀硫酸的质量为
(3)混合物中氯化钠的质量是
您最近一年使用:0次
【推荐3】用NA表示阿伏加德罗常数的值。则:
(1)0.5molCO2的质量为________ ,其中含有______ 个CO2分子,共有______ 个原子,共有______ 个电子。
(2)质量都是100g的H2S、CH4、CO2、N2四种气体中,在相同条件下体积最小的是_______ ,含有原子数目最多的是_______ 。
(3)在标准状况下,由CO和CO2组成的混合气体为4.48L,质量为7.2g,此混合物中C和O原子个数比是___________ 。
(4)欲配制 100mL 1mol/L CuSO4溶液,需称量CuSO4·5H2O_______ g 。
(5)高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂,制备高铁酸钠的主要反应为:2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑,该反应中的还原剂是_________________ ,氧化产物是___________ ,每生成1 mol Na2FeO4转移_______ mol电子。
(1)0.5molCO2的质量为
(2)质量都是100g的H2S、CH4、CO2、N2四种气体中,在相同条件下体积最小的是
(3)在标准状况下,由CO和CO2组成的混合气体为4.48L,质量为7.2g,此混合物中C和O原子个数比是
(4)欲配制 100mL 1mol/L CuSO4溶液,需称量CuSO4·5H2O
(5)高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂,制备高铁酸钠的主要反应为:2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑,该反应中的还原剂是
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐1】(1)0.5mol C2H2O4的质量是_______ g,约含______ 个C2H2O4分子,含______ mol氧原子。
(2)38.4g SO2在标准状况下的体积为___________ L,该气体在标准状况下的密度是______________ 。
(3)在标准状况下,将_______ L NH3溶于水得到0.5 mol·L-1的氨水250 mL;配制100 mL 0.2 mol·L-1CuSO4溶液,需要CuSO4·5H2O________ g。
(4)液态化合物XY2在一定量O2中恰好完全燃烧(XY2(液)+ 3O2(气)= XO2(气)+ 2YO2(气)),冷却后,在标准状况下测得生成物的体积是672mL,密度是2.56g/L,则:
①反应前O2的体积是___________ mL。 ②化合物XY2的摩尔质量是___________ 。
③若XY2分子中X、Y两元素的质量之比为3:16,则X、Y两元素分别是_________ 和________ 。(写元素符号)。
(2)38.4g SO2在标准状况下的体积为
(3)在标准状况下,将
(4)液态化合物XY2在一定量O2中恰好完全燃烧(XY2(液)+ 3O2(气)= XO2(气)+ 2YO2(气)),冷却后,在标准状况下测得生成物的体积是672mL,密度是2.56g/L,则:
①反应前O2的体积是
③若XY2分子中X、Y两元素的质量之比为3:16,则X、Y两元素分别是
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】在标准状况下:
(1)0.5 mol HCl占有的体积是__________ L。
(2)33.6 L H2的摩尔质量是__________ 。
(3)在9.5 g某二价金属的氯化物固体中含有0.2 mol Cl-,将此固体加水溶解稀释为100毫升,则此氯化物的摩尔质量为_________ 此氯化物溶液的物质的量浓度为___________ 。
(1)0.5 mol HCl占有的体积是
(2)33.6 L H2的摩尔质量是
(3)在9.5 g某二价金属的氯化物固体中含有0.2 mol Cl-,将此固体加水溶解稀释为100毫升,则此氯化物的摩尔质量为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】测定 溶液的浓度。准确量取
溶液的浓度。准确量取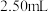 除去
除去 的
的 溶液于
溶液于 容量瓶中,加水稀释至刻度;准确量取
容量瓶中,加水稀释至刻度;准确量取 稀释后的溶液于锥形瓶中,滴加氨水调节溶液
稀释后的溶液于锥形瓶中,滴加氨水调节溶液 ,用
,用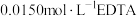
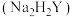 溶液滴定至终点(滴定反应为
溶液滴定至终点(滴定反应为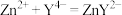 ),平行滴定3次,平均消耗EDTA溶液
),平行滴定3次,平均消耗EDTA溶液 。计算
。计算 溶液的物质的量浓度
溶液的物质的量浓度_______ 。(写出计算过程)。
 溶液的浓度。准确量取
溶液的浓度。准确量取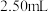 除去
除去 的
的 溶液于
溶液于 容量瓶中,加水稀释至刻度;准确量取
容量瓶中,加水稀释至刻度;准确量取 稀释后的溶液于锥形瓶中,滴加氨水调节溶液
稀释后的溶液于锥形瓶中,滴加氨水调节溶液 ,用
,用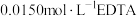
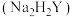 溶液滴定至终点(滴定反应为
溶液滴定至终点(滴定反应为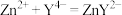 ),平行滴定3次,平均消耗EDTA溶液
),平行滴定3次,平均消耗EDTA溶液 。计算
。计算 溶液的物质的量浓度
溶液的物质的量浓度
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】某种胃药的有效成分为碳酸钙,某实验小组为测定其中碳酸钙的含量,取10粒药片(0.1 g/粒)研碎后溶解。加入25.00 mL 1.0 mol/L的稀盐酸反应,最后用1.0 mol/LNaOH溶液中和过量的盐酸,测定所消耗的NaOH的溶液体积如下:
(1)配制100 mL 1.0 mol/L的稀盐酸,需要2.5 mol/L的盐酸的体积为___________ mL。
(2)药片中碳酸钙的质量分数为___________ 。
| 测定次数 | 第1次 | 第2次 | 第3次 | 第4次 |
| V(NaOH)/mL | 13.00 | 12.90 | 11.40 | 13.10 |
(1)配制100 mL 1.0 mol/L的稀盐酸,需要2.5 mol/L的盐酸的体积为
(2)药片中碳酸钙的质量分数为
您最近一年使用:0次



