已知热化学方程式 2H2(g)+O2(g)=2H2O(l) ΔH1=-571.6 kJ∙mol−1,则关于热化学方程式2H2O(l)= 2H2(g)+O2(g) ΔH2 的说法中正确的是( )
| A.方程式中物质前的系数表示分子数 | B.该反应ΔH2>0 |
| C.该反应ΔH2=+571.6 kJ·mol-1 | D.该反应与上述反应属于可逆反应 |
14-15高二上·黑龙江·期中 查看更多[5]
(已下线)1.2.1 反应热的测量和热化学方程式-【帮课堂】2022-2023学年高二化学同步精品讲义(沪科版2020选择性必修第一册)山东省济宁市曲阜市第一中学2020-2021学年高二上学期阶段性检测(9月月考)化学试题山东省滕州市第一中学2020-2021学年高二9月开学收心考试化学试题山西运城盐湖五中2018-2019学年高二第一学期9月月考化学试题2014-2015学年黑龙江省伊春市伊春二中高二上学期期中化学试卷
更新时间:2020-09-09 13:56:33
|
相似题推荐
【推荐1】利用含碳化合物合成燃料是解决能源危机的重要方法,已知煤液化过程中有反应CO(g)+2H2(g)=CH3OH(g),其反应过程中的能量变化情况如图所示,曲线Ⅰ和曲线Ⅱ分别表示不使用催化剂和使用催化剂的两种情况。下列判断正确的是( )
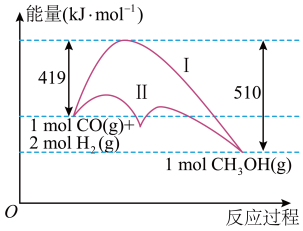

| A.该反应的反应热ΔH=+91kJ·mol-1 |
| B.加入催化剂后,该反应的ΔH变小 |
| C.反应物的总能量大于生成物的总能量 |
| D.从图中可以看出,使用催化剂降低了该反应的活化能 |
您最近半年使用:0次
多选题
|
较易
(0.85)
【推荐2】一种利用热化学循环制氢的原理如图所示。下列关于该循环的说法正确的是( )
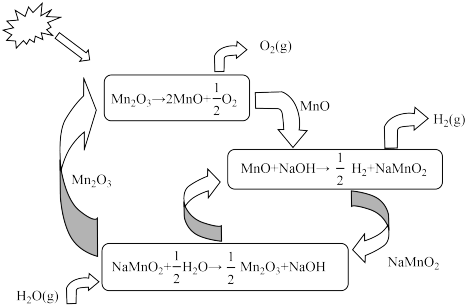

| A.能量转化形式为化学能→太阳能 |
| B.取之不尽的太阳能是可再生能源 |
| C.Mn元素表现出三种化合价 |
| D.总反应的热化学方程式为:2H2O(l)=O2(g)+2H2(g)△H>0 |
您最近半年使用:0次
多选题
|
较易
(0.85)
名校
【推荐1】已知:2H2(g)+ O2(g)=2H2O(l) ΔH=-571.6 kJ· mol-1
CH4(g)+ 2O2(g)=CO2(g)+2H2O(l) ΔH=-890 kJ· mol-1
现有H2与CH4的混合气体112 L(标准状况),使其完全燃烧生成CO2和H2O(l),若实验测得反应放热3695 kJ,则原混合气体中H2的物质的量及原混合气体的平均相对分子质量是
CH4(g)+ 2O2(g)=CO2(g)+2H2O(l) ΔH=-890 kJ· mol-1
现有H2与CH4的混合气体112 L(标准状况),使其完全燃烧生成CO2和H2O(l),若实验测得反应放热3695 kJ,则原混合气体中H2的物质的量及原混合气体的平均相对分子质量是
| A.1.25 | B.1.75 | C.11.6 | D.12.5 |
您最近半年使用:0次
多选题
|
较易
(0.85)
解题方法
【推荐2】图像可直观地表现化学变化中的物质变化和能量变化。下列判断错误的是


| A.图甲所示反应为放热反应,且△H=(Ek-Ek′)kJ•mol-1 |
| B.已知石墨比金刚石稳定,则石墨转化为金刚石过程中的能量变化如图乙 |
| C.图丙所示反应的热化学方程式为N2(g)+O2(g)=2NO(g) △H=-bkJ•mol-1 |
D.若2A(g) B(g)的能量变化如图丁,则2A(g) B(g)的能量变化如图丁,则2A(g) B(l) △H<-akJ•mol-1 B(l) △H<-akJ•mol-1 |
您最近半年使用:0次
多选题
|
较易
(0.85)
名校
【推荐1】 分子结构为正四面体形(如图所示)。已知:断裂
分子结构为正四面体形(如图所示)。已知:断裂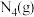 中
中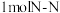 键吸收
键吸收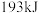 能量,形成
能量,形成 中
中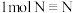 键放出
键放出 能量。下列说法正确的是
能量。下列说法正确的是
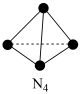
 分子结构为正四面体形(如图所示)。已知:断裂
分子结构为正四面体形(如图所示)。已知:断裂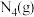 中
中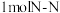 键吸收
键吸收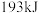 能量,形成
能量,形成 中
中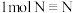 键放出
键放出 能量。下列说法正确的是
能量。下列说法正确的是
A. |
B. 比 比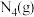 更稳定 更稳定 |
C.形成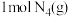 中的化学键放出 中的化学键放出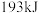 的能量 的能量 |
D.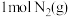 完全转化为 完全转化为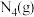 ,体系的能量增加 ,体系的能量增加 |
您最近半年使用:0次
多选题
|
较易
(0.85)
解题方法
【推荐1】下列描述中正确的是
| A.反应2H2(g)+O2(g) =2H2O(g)的ΔH可通过下式估算: ∆H=反应中断裂旧共价键的键能之和-反应中形成新共价键的键能之和 |
| B.在25 ℃、101 kPa时,1 mol碳燃烧所放出的热量为碳的标准燃烧热 |
| C.从C(石墨,s) = C(金刚石,s) ΔH=+1.9 kJ·mol-1,可知石墨比金刚石更稳定 |
| D.同温同压下,反应H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件下的ΔH不同 |
您最近半年使用:0次
多选题
|
较易
(0.85)
名校
【推荐2】4P(红磷s)→P4(白磷s);△H=+17kJ•mol-1.根据以上方程式,下列推论正确的是
| A.当lmol白磷转变成红磷时放出17kJ热量 |
| B.当4g红磷转变成白磷时吸收17kJ热量 |
| C.正反应是一个放热反应 |
| D.白磷热稳定性比红磷小 |
您最近半年使用:0次

 、
、 、
、 的氧化性依次减弱
的氧化性依次减弱 CH3CH2OH(g)+3H2O(g)需在300℃进行可推测该反应是吸热反应
CH3CH2OH(g)+3H2O(g)需在300℃进行可推测该反应是吸热反应 (x=1,2,3,4)的能量(kJ)相对大小如图所示。下列有关说法正确的是
(x=1,2,3,4)的能量(kJ)相对大小如图所示。下列有关说法正确的是 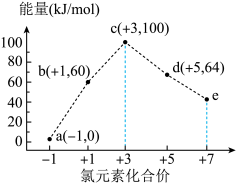

 (aq)+2Cl-(aq) △H= -116kJ•mol-1
(aq)+2Cl-(aq) △H= -116kJ•mol-1
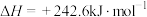 ,则等质量
,则等质量 的总能量比
的总能量比 的总能量低
的总能量低
 ,则稀
,则稀 溶液和稀
溶液和稀 完全反应生成
完全反应生成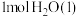 时,放出57.3kJ的热量
时,放出57.3kJ的热量
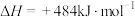 ,则
,则 的燃烧热是
的燃烧热是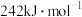
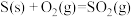
 ,
,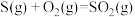
 ,则
,则


