已知在25 ℃、1.01×105 Pa下,1mol氢气在氧气中燃烧生成气态水的能量变化如下图所示,下列有关说法不正确的是( )
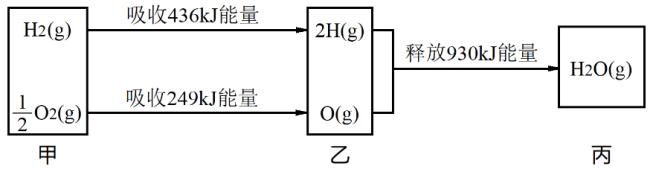

| A.热化学方程式可表示为:2H2(g)+O2(g)=2H2O(g) ΔH = -490 kJ·mol-1 |
| B.乙→丙的过程中若生成液态水,释放的能量将小于930 kJ |
| C.H2O分解为H2与O2时吸收热量 |
| D.甲、乙、丙中物质所具有的总能量大小关系为乙>甲>丙 |
20-21高三上·浙江·阶段练习 查看更多[2]
更新时间:2020-09-24 18:53:36
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】下列关于热化学反应的描述中正确的是( )
| A.HCl和NaOH反应的中和热△H=-57.3 kJ·mol-1,则1 mol硫酸与足量氢氧化钡溶液反应放热为114.6 kJ |
| B.H2(g)的燃烧热是285.8 kJ·mol-1,则2H2O(1)=2H2(g)+O2(g)反应的△H=+571.6kJ·mol-1 |
| C.反应物的热效应与是否使用催化剂有关 |
| D.500℃、30 MPa下,将0.5 mol N2和1.5 mol H2置于密闭的容器中充分反应生成NH3(g),放热19.3 kJ,其热化学方程式为:N2(g) + 3H2(g) ⇌ 2NH3(g) △H= -38.6 kJ·mol-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列依据热化学方程式得出的结论正确的是
| 选项 | 热化学方程式 | 结论 |
| A | 2C(s)+2O2(g)=2CO2(g) ΔH1 2C(s)+O2(g)=2CO(g) ΔH2 | ΔH1>ΔH2 |
| B | Sn(s,灰)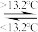 Sn(s,白) ΔH=+2.1kJ·mol-1(灰锡为粉末状,白锡为块状) Sn(s,白) ΔH=+2.1kJ·mol-1(灰锡为粉末状,白锡为块状) | 锡制品在炎热的夏天更容易损坏 |
| C | P4(s,白磷)=4P(s,红磷) ΔH=-29.2kJ·mol-1 | 常温下,红磷比白磷稳定 |
| D | 2H2(g)+O2(g)=2H2O(g) ΔH=-483.6kJ·mol-1 | H2的燃烧热ΔH=-241.8kJ·mol-1 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】已知辛烷的燃烧热为5518kJ·mol-1,强酸与强碱在稀溶液中发生反应时的中和热为57.3kJ·mol-1,则下列热化学方程式书写正确的是
①C8H18(l)+25/2O2(g)=8CO2(g)+9H2O(g);△H=-5518kJ·mol-1
②2C8H18(l)+25O2(g)=16CO2(g)+18H2O(l);△H=-11036kJ·mol-1
③H+(aq) + OH-(aq) =H2O(l); △H= +57.3kJ·mol-1
④2NaOH(aq) +H2SO4(aq)=Na2SO4(aq) + 2H2O(l);△H=-57.3kJ·mol-1
①C8H18(l)+25/2O2(g)=8CO2(g)+9H2O(g);△H=-5518kJ·mol-1
②2C8H18(l)+25O2(g)=16CO2(g)+18H2O(l);△H=-11036kJ·mol-1
③H+(aq) + OH-(aq) =H2O(l); △H= +57.3kJ·mol-1
④2NaOH(aq) +H2SO4(aq)=Na2SO4(aq) + 2H2O(l);△H=-57.3kJ·mol-1
| A.①③ | B.②③ | C.②④ | D.只有② |
您最近一年使用:0次
【推荐1】将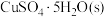 溶于水会使溶液温度降低,将
溶于水会使溶液温度降低,将 溶于水会使溶液温度升高,则下列能量转化关系的判断正确的是
溶于水会使溶液温度升高,则下列能量转化关系的判断正确的是
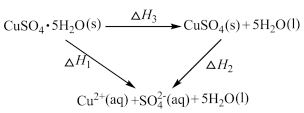
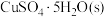 溶于水会使溶液温度降低,将
溶于水会使溶液温度降低,将 溶于水会使溶液温度升高,则下列能量转化关系的判断正确的是
溶于水会使溶液温度升高,则下列能量转化关系的判断正确的是
A.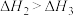 | B. | C.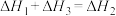 | D.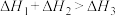 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列反应属于吸热反应的是
| A.生石灰与水的反应 | B.乙醇燃烧 |
| C.铝粉与氧化铁粉末反应 | D.BA(OH)2·8H2O与NH4Cl的反应 |
您最近一年使用:0次
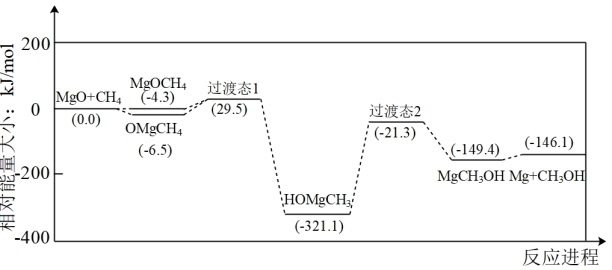
【推荐1】研究表明:MgO基催化剂广泛应用于 的转化过程,图是我国科研工作者研究MgO与
的转化过程,图是我国科研工作者研究MgO与 作用最终生成Mg与
作用最终生成Mg与 的物质相对能量-反应进程曲线。下列说法
的物质相对能量-反应进程曲线。下列说法不正确 的是
 的转化过程,图是我国科研工作者研究MgO与
的转化过程,图是我国科研工作者研究MgO与 作用最终生成Mg与
作用最终生成Mg与 的物质相对能量-反应进程曲线。下列说法
的物质相对能量-反应进程曲线。下列说法
| A.反应中甲烷被氧化 |
B.中间体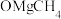 比 比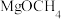 更稳定 更稳定 |
| C.该反应的速率控制步骤对应的活化能是29.5kJ/mol |
D.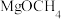 转化为 转化为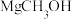 的焓变为-145.1 kJ/mol 的焓变为-145.1 kJ/mol |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】反应A→C分两步进行:①A→B,②B→C。反应过程能量变化曲线如图所示(E1、E2、E3、E4表示活化能)。下列说法正确的是
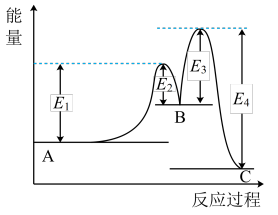

| A.两步反应的ΔH均大于0 | B.加入催化剂能改变反应的焓变 |
| C.三种物质中C最稳定 | D.A→C反应的ΔH=E4-E1 |
您最近一年使用:0次
【推荐3】已知:①298K 时,相关物质的相对能量如下表所示:
②H2O(g)=H2O(l) ΔH1=-286kJ•mol-1-(-242kJ•mol-1)=-44kJ•mol-1
有研究表明,在催化剂存在下,C2H6(g)+CO2(g) C2H4(g)+CO(g)+H2O(g),该反应分两步进行,如下图所示。
C2H4(g)+CO(g)+H2O(g),该反应分两步进行,如下图所示。

下列说法不正确 的是 ( )
| 物质 | C2H4(g) | H2(g) | C2H6(g) | CO(g) | H2O(g) | H2O(l) | CO2(g) |
| 相对能量 /kJ·mol-1 | 52 | 0 | -84 | -110 | -242 | -286 | -393 |
有研究表明,在催化剂存在下,C2H6(g)+CO2(g)
 C2H4(g)+CO(g)+H2O(g),该反应分两步进行,如下图所示。
C2H4(g)+CO(g)+H2O(g),该反应分两步进行,如下图所示。
下列说法
| A.E[C2H6(g)+CO2(g)] = -477 kJ•mol-1 | B.第 2 步反应∆H= 41kJ•mol-1 |
| C.第 2 步正反应活化能为 210 kJ•mol-1 | D.第 1 步反应比第 2 步反应慢 |
您最近一年使用:0次



