题型:未知-未知
难度:0.85
引用次数:266
题号:11190245
已知:C(s)+H2O(g)=CO(g)+H2(g) ΔH=akJ·mol-1;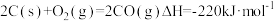 ,
,  、
、 和
和 键的键能(
键的键能( )分别为436、496和462,则a为( )
)分别为436、496和462,则a为( )
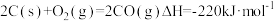 ,
,  、
、 和
和 键的键能(
键的键能( )分别为436、496和462,则a为( )
)分别为436、496和462,则a为( )A.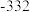 | B.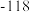 | C.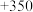 | D.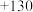 |
更新时间:2020-09-26 08:46:15
|
相似题推荐
未知-未知
|
较易
(0.85)
【推荐1】通过乙醇制取氢气通常有如下两条途径:
a.CH3CH2OH(g)+H2O(g)=4H2(g)+2CO(g) ΔH1=+256.6 kJ·mol-1
b.2CH3CH2OH(g)+O2(g)=6H2(g)+4CO(g) ΔH2=+27.6 kJ·mol-1
则下列说法正确的是
a.CH3CH2OH(g)+H2O(g)=4H2(g)+2CO(g) ΔH1=+256.6 kJ·mol-1
b.2CH3CH2OH(g)+O2(g)=6H2(g)+4CO(g) ΔH2=+27.6 kJ·mol-1
则下列说法正确的是
| A.升高a的反应温度,乙醇的转化率增大 |
| B.由b可知:乙醇的燃烧热为13.8 kJ·mol-1 |
| C.2H2(g)+O2(g)=2H2O(g) ΔH=+485.6 kJ·mol-1 |
| D.制取等量的氢气,途径b消耗的能量更多 |
您最近一年使用:0次



