将Ce(SO4)2·4H2O(摩尔质量为404 g·mol-1)在空气中加热,样品的固体残留率(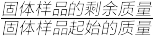 ×100%)随温度的变化如下图所示。
×100%)随温度的变化如下图所示。
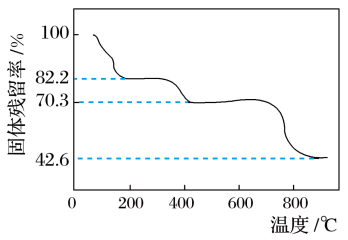
当固体残留率为70.3%时,所得固体可能为
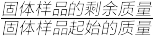 ×100%)随温度的变化如下图所示。
×100%)随温度的变化如下图所示。
当固体残留率为70.3%时,所得固体可能为
| A.Ce(SO4)2 | B.Ce2(SO4)3 | C.CeOSO4 | D.无法计算 |
20-21高三上·安徽阜阳·阶段练习 查看更多[3]
安徽省太和第一中学2021届高三上学期第一次校本教材反馈测试化学试题(已下线)专题讲座(三) 热重分析中的物质成分的判断(精练)-2022年高考化学一轮复习讲练测黑龙江省齐齐哈尔市普高联谊校2022-2023学年高三上学期期中考试化学试题
更新时间:2020-10-08 17:13:31
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】在容积为2L的密闭容器中发生反应: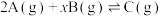 。图甲表示200℃时容器中A、B、C物质的量随时间的变化,图乙表示温度100℃和200℃平衡时C的体积分数随起始
。图甲表示200℃时容器中A、B、C物质的量随时间的变化,图乙表示温度100℃和200℃平衡时C的体积分数随起始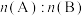 的变化关系,下列说法正确的是
的变化关系,下列说法正确的是

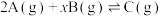 。图甲表示200℃时容器中A、B、C物质的量随时间的变化,图乙表示温度100℃和200℃平衡时C的体积分数随起始
。图甲表示200℃时容器中A、B、C物质的量随时间的变化,图乙表示温度100℃和200℃平衡时C的体积分数随起始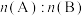 的变化关系,下列说法正确的是
的变化关系,下列说法正确的是
A.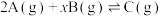 中, 中, |
B.200℃,反应从开始到平衡的平均速率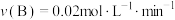 |
C.由图乙可知,反应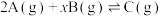 的 的 ,且 ,且 |
| D.当外界条件由200℃降温到100℃,原平衡一定被破坏,且正、逆反应速率均增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】向某恒容密闭容器中充入一定量CO2和H2,发生反应: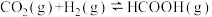 ,测得平衡体系中CO2的物质的量分数与反应温度的关系如图所示。下列物理量中,a点大于b点的是( )
,测得平衡体系中CO2的物质的量分数与反应温度的关系如图所示。下列物理量中,a点大于b点的是( )
①正反应速率②逆反应速率③HCOOH(g)的浓度④对应温度的平衡常数

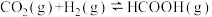 ,测得平衡体系中CO2的物质的量分数与反应温度的关系如图所示。下列物理量中,a点大于b点的是( )
,测得平衡体系中CO2的物质的量分数与反应温度的关系如图所示。下列物理量中,a点大于b点的是( )①正反应速率②逆反应速率③HCOOH(g)的浓度④对应温度的平衡常数

| A.①② | B.①③ | C.②④ | D.③④ |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】在测定硫酸铜晶体结晶水含量的实验中,会导致测定结果偏低的是( )
| A.加热后固体发黑 |
| B.坩埚沾有受热不分解的杂质 |
| C.加热时有少量晶体溅出 |
| D.晶体中混有受热不分解的杂质 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】测定胆矾晶体结晶水含量时,若测定的相对误差大于零,则产生误差的原因可能是
| A.加热后容器未放入干燥器中冷却 | B.最后两次加热后的质量相差较大 |
| C.加热前称量时容器未完全干燥 | D.胆矾晶体中混有加热不分解的杂质 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】某兴趣小组同学为研究Cu与Fe3+的反应进行如下实验(已知CuCl为白色固体,微溶于水):
下列说法不正确的是
| 序号 | I | II | III |
| 实验 步骤 | 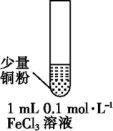 充分振荡,加入2mL蒸馏水 | 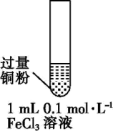 充分振荡,加入2mL蒸馏水 | 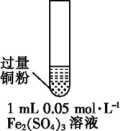 充分振荡,加入2mL蒸馏水 |
| 实验 现象 | 铜粉消失,溶液黄色变浅,加入蒸馏水后无明显现象 | 铜粉有剩余,溶液黄色褪去,加入蒸馏水后生成白色沉淀 | 铜粉有剩余,溶液黄色褪去,变成蓝色,加入蒸馏水后无白色沉淀 |
| A.3个实验中消耗的铜粉的量不完全一样 |
| B.实验I、II、III中均发生了反应2Fe3++Cu=Cu2++2Fe2+ |
| C.II中加水后的离子反应可能是Cu2++Cu+2Cl-=2CuCl↓ |
| D.上述实验表明能否形成白色沉淀主要取决于加入Cu的量 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】为确定试样Fe2O3、Cu、Fe混合物中铜的质量分数,某同学取质量为ag的试样进行下列实验,所得气体数据在标准状况下测得,所涉及的过程如下:

注:已知:Fe3+、Fe2+、Cu2+转化为相应的氢氧化物,开始沉淀和沉淀完全时的pH如下表:
下列说法不正确的是

注:已知:Fe3+、Fe2+、Cu2+转化为相应的氢氧化物,开始沉淀和沉淀完全时的pH如下表:
| 氢氧化物 | Fe3+ | Fe2+ | Cu2+ |
| 开始沉淀PH | 2.5 | 7.0 | 4.7 |
| 完全沉淀PH | 3.7 | 9.0 | 6.7 |
| A.气体B为氢气 |
| B.溶液A中所含的阳离子可能是H+、 Fe3+、 Fe2+、 Cu2+ |
| C.加入过氧化氢溶液时发生的反应:2Fe2++H2O2+2H+=2Fe3++2H2O |
| D.若沉淀E经洗涤、烘干、灼烧后得到固体mg,则试样中Cu的质量分数=(a-0.56)/a×100% |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】某有机物样品4.6g完全燃烧,将燃烧后的产物通入足量石灰水中完全吸收,经过滤得到沉淀20克,滤液质量比原石灰水减少5.8克,该有机样品可能是
| A.C2H6O2 | B.CH4和C2H6的混合物 |
| C.CH4O和C3H8O的混合物 | D.C2H6O和C3H8O3的混合物 |
您最近一年使用:0次