过氧化钠保存不当容易变质,某课外活动小组为了粗略测定样品中过氧化钠的质量分数,他们称取10.0g样品,并设计用如图装置来测定过氧化钠的质量分数。
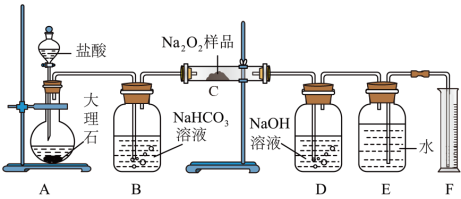
上图中的E和F构成量气装置,用来测定 的体积。
的体积。
(1)写出以下装置中发生反应的化学方程式。
装置A:__________ 。装置B:__________ 。
(2)D中NaOH溶液的作用是___________ 。
(3)为准确读出氧气的体积需进行以下操作,正确的顺序为_________ 。
A.调整量筒高度,使广口瓶E与量筒F内液面相平
B.将气体冷却至室温
C.平视,使凹液面最低点与视线水平相切再读数
(4)读出量筒内水的体积后,折算成标准状况下氧气的体积为1.12L,则样品中过氧化钠的质量分数为________ 。

上图中的E和F构成量气装置,用来测定
 的体积。
的体积。(1)写出以下装置中发生反应的化学方程式。
装置A:
(2)D中NaOH溶液的作用是
(3)为准确读出氧气的体积需进行以下操作,正确的顺序为
A.调整量筒高度,使广口瓶E与量筒F内液面相平
B.将气体冷却至室温
C.平视,使凹液面最低点与视线水平相切再读数
(4)读出量筒内水的体积后,折算成标准状况下氧气的体积为1.12L,则样品中过氧化钠的质量分数为
更新时间:2020-10-07 11:28:45
|
相似题推荐
解答题-实验探究题
|
较易
(0.85)
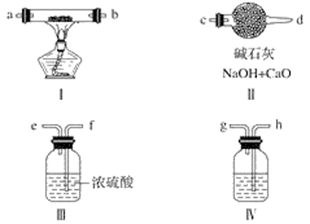
【推荐1】现用金属钠和空气制备纯度较高的过氧化钠,可利用的装置如下图所示。
请回答下列问题:
(1)装置Ⅳ中盛放的药品是______________ ,其作用是______________ 。
(2)若规定气体的气流方向从左到右,则组合实验装置时各件仪器的正确连接顺序为(按从左到右顺序写明仪器的编号Ⅰ、Ⅱ……)______________ ,各仪器接口的标号字母(a、b……)顺序是空气进入__________,接__________,接__________,接__________。______________
(3)装置Ⅱ的作用是______________________________________ 。

请回答下列问题:
(1)装置Ⅳ中盛放的药品是
(2)若规定气体的气流方向从左到右,则组合实验装置时各件仪器的正确连接顺序为(按从左到右顺序写明仪器的编号Ⅰ、Ⅱ……)
(3)装置Ⅱ的作用是
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐2】根据如图转化关系以及实验现象填写空白。

(1)固体X是_______ ,固体Y是_______ ,产物A是_______ 。(填写化学式)。
(2)反应①的化学方程式是_______ 。
(3)反应②的化学方程式是_______ 。
(4)反应③的化学方程式是_______ 。

(1)固体X是
(2)反应①的化学方程式是
(3)反应②的化学方程式是
(4)反应③的化学方程式是
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
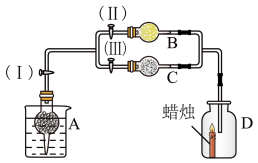
【推荐3】在干燥管A中为块状白色固体,B中为淡黄色粉末,C中为白色固体,并将A、B、C按如图所示装置连接,当打开活塞(I)(II)时,D中蜡烛火焰明亮;打开活塞(I)(III)时,D中蜡烛火焰熄灭;关闭活塞(I),A中反应自行停止。
试根据上述实验事实,回答以下各问题:
(1)A中发生反应的离子方程式是_______ 。
(2)在装置B中的淡黄色粉末是_______ ,其发生反应的化学方程式为_______ 。
(3)在干燥管C中的白色固体应为_______ (填一种即可)。

试根据上述实验事实,回答以下各问题:
(1)A中发生反应的离子方程式是
(2)在装置B中的淡黄色粉末是
(3)在干燥管C中的白色固体应为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐1】成人牙膏中摩擦剂的主要成分是碳酸钙,现通过以下实验装置测定碳酸钙的质量分数(假设牙膏的其他成分与盐酸不反应)。

(1)乙装置中发生反应的化学方程式为____ 。
(2)甲装置中NaOH溶液的作用___ 。若无装置甲,则会使得碳酸钙质量分数测定___ (填“偏高”“偏低”或“无影响”)。
(3)若称取的牙膏样品为ag,丙装置中的沉淀经干燥后质量为bg,则样品中碳酸钙的质量分数为___ (用含a,b的代数式表示)。
(4)若不测定丙装置中沉淀的质量,而通过测定丙装置在实验前后的质量差来计算碳酸钙的质量分数,会使得碳酸钙质量分数测定___ (填“偏高”“偏低”或“无影响”),原因是___ 。

(1)乙装置中发生反应的化学方程式为
(2)甲装置中NaOH溶液的作用
(3)若称取的牙膏样品为ag,丙装置中的沉淀经干燥后质量为bg,则样品中碳酸钙的质量分数为
(4)若不测定丙装置中沉淀的质量,而通过测定丙装置在实验前后的质量差来计算碳酸钙的质量分数,会使得碳酸钙质量分数测定
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐2】SO2的污染防治与利用对于环境保护意义重大。某化学小组在实验室中对SO2的制备、性质及回收利用等相关问题进行探究。请回答下列问题:
(1)制备并收集纯净的SO2

①用上图装置制备纯净的SO2,发生装置中反应的化学方程式为_______ 。
②装置的连接顺序为:a→_______ (按气流方向,用字母标号表示)。
(2)设计实验探究SO2中+4价S的性质
限选试剂:NaOH溶液、稀H2SO4、H2O2溶液、FeCl3溶液、淀粉KI溶液、新制H2S溶液
填写表格中相应内容:
①_______ ; ②_______ ;③_______ ; ④_______ 。
(3)设计回收利用SO2的途径: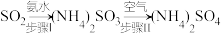 。该小组欲测定步骤II中(NH4)2SO3的转化率(α),设计如下实验方案:一定条件下,向100mLcmol/L的(NH4)2SO3溶液中通入空气,向反应后的溶液中加入过量的盐酸,再加入足量的氯化钡溶液,生成沉淀,将沉淀过滤、洗涤、干燥、称量,质量为mg。
。该小组欲测定步骤II中(NH4)2SO3的转化率(α),设计如下实验方案:一定条件下,向100mLcmol/L的(NH4)2SO3溶液中通入空气,向反应后的溶液中加入过量的盐酸,再加入足量的氯化钡溶液,生成沉淀,将沉淀过滤、洗涤、干燥、称量,质量为mg。
①检验沉淀是否洗净的方法是_______ 。
②α=_______ ×100%(用含c、m的代数式表示)。

(1)制备并收集纯净的SO2

①用上图装置制备纯净的SO2,发生装置中反应的化学方程式为
②装置的连接顺序为:a→
(2)设计实验探究SO2中+4价S的性质
限选试剂:NaOH溶液、稀H2SO4、H2O2溶液、FeCl3溶液、淀粉KI溶液、新制H2S溶液
| 实验操作 | 实验现象 | 实验结论 | |
| 实验一 | 将SO2通入新制H2S溶液中 | 溶液变浑浊 | SO2中+4价S具有________性 |
| 实验二 | 将SO2通入_________中 | ________ | SO2中+4价S具有还原性,反应的离子方程式为_______ |
①
(3)设计回收利用SO2的途径:
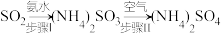 。该小组欲测定步骤II中(NH4)2SO3的转化率(α),设计如下实验方案:一定条件下,向100mLcmol/L的(NH4)2SO3溶液中通入空气,向反应后的溶液中加入过量的盐酸,再加入足量的氯化钡溶液,生成沉淀,将沉淀过滤、洗涤、干燥、称量,质量为mg。
。该小组欲测定步骤II中(NH4)2SO3的转化率(α),设计如下实验方案:一定条件下,向100mLcmol/L的(NH4)2SO3溶液中通入空气,向反应后的溶液中加入过量的盐酸,再加入足量的氯化钡溶液,生成沉淀,将沉淀过滤、洗涤、干燥、称量,质量为mg。①检验沉淀是否洗净的方法是
②α=

您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐3】三氯化铬(CrCl3)在工业上主要用作媒染剂和催化剂,实验室模拟工业上以BaCrO4为原料制备CrCl3。
(1)制备CrCl3
取一定质量的BaCrO4和对应量的水加入到三预瓶中,水浴加热并搅拌,一段时间后同时加入过量浓盐酸和无水乙醇(C2H5OH)充分反应,生成CrC13并放出CO2气体。
①上述反应的化学方程式为__________ 。
②上述反应中的乙醇与BaCrO4投料的物质的量比例大约为3:8,原因是__________ 。
(2)测定CrCl3的质量分数。
Ⅰ.称取样品0.3300g,加水溶解并配成250.0mL的溶液。
Ⅱ.移取25.00mL样品溶液于带塞的锥形瓶中,加热至沸后加入稍过量的Na2O2,稀释并加热煮沸,再加入过量的硫酸酸化,将Cr3+氧化为Cr2O ;再加入过量KI固体,加塞揺匀。使铬元素完全以Cr3+的形式存在。
;再加入过量KI固体,加塞揺匀。使铬元素完全以Cr3+的形式存在。
Ⅲ.加入少量淀粉溶液,用0.0500mol·L-1标准Na2S2O3溶液滴定至终点,平行测定3次。平均消耗标准Na2S2O3溶液12.00mL。
已知反应: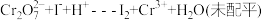 ;
;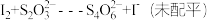
①滴定终点的现象是__________ 。
②计算CrC13的质量分数(写出计算过程,结果保留3位有效数字)__________
③在上述实验中,下列操作(其他操作正确)会造成测定结果偏低的有__________ (填字母)
A.碱式滴定管使用前,水洗后未用标准Na2S2O3溶液润洗
B.锥形瓶水洗后未干燥
C滴定终点读数时俯视读数
D.滴定前碱式滴定管尖嘴部分有气泡,滴定后消失
(3)CrC13样品中C1-含量测定
实验室可用AgNO3标准溶液测定CrCl3样品中C1-的含量,请补充完成相应的实验步骤:准确量取25.00mL待测样品溶液于锥形瓶中,__________ ,进行数据处理。(终点反应为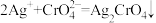 砖红色)。实验中须使用的试剂有:K2CO3溶液、AgNO3标准溶液:除常用仪器外须使用的仪器有:棕色酸式滴定管)
砖红色)。实验中须使用的试剂有:K2CO3溶液、AgNO3标准溶液:除常用仪器外须使用的仪器有:棕色酸式滴定管)
(1)制备CrCl3
取一定质量的BaCrO4和对应量的水加入到三预瓶中,水浴加热并搅拌,一段时间后同时加入过量浓盐酸和无水乙醇(C2H5OH)充分反应,生成CrC13并放出CO2气体。
①上述反应的化学方程式为
②上述反应中的乙醇与BaCrO4投料的物质的量比例大约为3:8,原因是
(2)测定CrCl3的质量分数。
Ⅰ.称取样品0.3300g,加水溶解并配成250.0mL的溶液。
Ⅱ.移取25.00mL样品溶液于带塞的锥形瓶中,加热至沸后加入稍过量的Na2O2,稀释并加热煮沸,再加入过量的硫酸酸化,将Cr3+氧化为Cr2O
 ;再加入过量KI固体,加塞揺匀。使铬元素完全以Cr3+的形式存在。
;再加入过量KI固体,加塞揺匀。使铬元素完全以Cr3+的形式存在。Ⅲ.加入少量淀粉溶液,用0.0500mol·L-1标准Na2S2O3溶液滴定至终点,平行测定3次。平均消耗标准Na2S2O3溶液12.00mL。
已知反应:
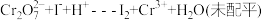 ;
;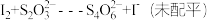
①滴定终点的现象是
②计算CrC13的质量分数(写出计算过程,结果保留3位有效数字)
③在上述实验中,下列操作(其他操作正确)会造成测定结果偏低的有
A.碱式滴定管使用前,水洗后未用标准Na2S2O3溶液润洗
B.锥形瓶水洗后未干燥
C滴定终点读数时俯视读数
D.滴定前碱式滴定管尖嘴部分有气泡,滴定后消失
(3)CrC13样品中C1-含量测定
实验室可用AgNO3标准溶液测定CrCl3样品中C1-的含量,请补充完成相应的实验步骤:准确量取25.00mL待测样品溶液于锥形瓶中,
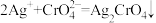 砖红色)。实验中须使用的试剂有:K2CO3溶液、AgNO3标准溶液:除常用仪器外须使用的仪器有:棕色酸式滴定管)
砖红色)。实验中须使用的试剂有:K2CO3溶液、AgNO3标准溶液:除常用仪器外须使用的仪器有:棕色酸式滴定管)
您最近一年使用:0次



