在干燥管A中为块状白色固体,B中为淡黄色粉末,C中为白色固体,并将A、B、C按如图所示装置连接,当打开活塞(I)(II)时,D中蜡烛火焰明亮;打开活塞(I)(III)时,D中蜡烛火焰熄灭;关闭活塞(I),A中反应自行停止。
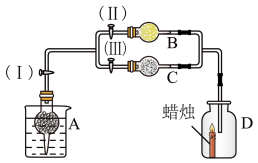
试根据上述实验事实,回答以下各问题:
(1)A中发生反应的离子方程式是_______ 。
(2)在装置B中的淡黄色粉末是_______ ,其发生反应的化学方程式为_______ 。
(3)在干燥管C中的白色固体应为_______ (填一种即可)。

试根据上述实验事实,回答以下各问题:
(1)A中发生反应的离子方程式是
(2)在装置B中的淡黄色粉末是
(3)在干燥管C中的白色固体应为
更新时间:2022/12/13 21:44:06
|
相似题推荐
解答题-无机推断题
|
较易
(0.85)
名校
【推荐1】A、B、C、D 四种可溶性盐,其阳离子分别是 Na+、Ba2+、Cu2+、Ag+中的某一种,阴离子分别是 Cl-、SO 、CO
、CO 、NO
、NO 中的某一种。现做以下实验:①将四种盐各取少量,分别溶于盛有 5 mL 蒸馏水的 4 支试管中,只有 B 盐溶液呈蓝色。②分别向 4 支试管中加入 2 mL 稀盐酸,发现 A 盐溶液中产生白色沉淀,C 盐溶液中有较多气泡产生,而 D 盐溶液无明显现象。
中的某一种。现做以下实验:①将四种盐各取少量,分别溶于盛有 5 mL 蒸馏水的 4 支试管中,只有 B 盐溶液呈蓝色。②分别向 4 支试管中加入 2 mL 稀盐酸,发现 A 盐溶液中产生白色沉淀,C 盐溶液中有较多气泡产生,而 D 盐溶液无明显现象。
(1)根据上述实验事实,推断这四种盐的化学式分别为:A___________ B___________ ; C___________ ;D___________ 。
(2)写出下列反应的离子方程式:
①B+D→:_____
②C+HCl→气体:_____
 、CO
、CO 、NO
、NO 中的某一种。现做以下实验:①将四种盐各取少量,分别溶于盛有 5 mL 蒸馏水的 4 支试管中,只有 B 盐溶液呈蓝色。②分别向 4 支试管中加入 2 mL 稀盐酸,发现 A 盐溶液中产生白色沉淀,C 盐溶液中有较多气泡产生,而 D 盐溶液无明显现象。
中的某一种。现做以下实验:①将四种盐各取少量,分别溶于盛有 5 mL 蒸馏水的 4 支试管中,只有 B 盐溶液呈蓝色。②分别向 4 支试管中加入 2 mL 稀盐酸,发现 A 盐溶液中产生白色沉淀,C 盐溶液中有较多气泡产生,而 D 盐溶液无明显现象。(1)根据上述实验事实,推断这四种盐的化学式分别为:A
(2)写出下列反应的离子方程式:
①B+D→:
②C+HCl→气体:
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐2】木材的深加工能有效提高其经济效益。工业上将木材进行干馏 隔绝空气加强热
隔绝空气加强热 可得到木煤气
可得到木煤气 含
含 、
、 、
、 等
等 、木焦油、焦木酸木炭等产品。
、木焦油、焦木酸木炭等产品。
请回答下列问题:
(1)木炭中一定含有______ 元素
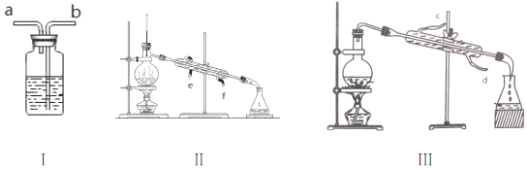
(2)下列装置可对木柴干馏后的产品进一步加工。
①用 装置可除去木煤气中的少量
装置可除去木煤气中的少量 ,混合器应从
,混合器应从______ 口通入 填仪器口字母
填仪器口字母 ,广口瓶中所盛试剂是
,广口瓶中所盛试剂是______ ,有关反应的离子方程式是______ 。
②木焦油和焦木酸中含有苯、乙酸和甲醛等,他们的部分性质如表所示。
若从苯、乙酸和甲醇的混合液中将三者一一分离,可选用上述装置中的______  填装置序号
填装置序号 ,盛装混合液的仪器名称是
,盛装混合液的仪器名称是______ ,该试验的原理是利用了三种物质的______ 不同。实验时冷凝水的进水口是______  填仪器口字母
填仪器口字母 。为保证实验安全,还需要注意的一项操作是
。为保证实验安全,还需要注意的一项操作是______ 。
 隔绝空气加强热
隔绝空气加强热 可得到木煤气
可得到木煤气 含
含 、
、 、
、 等
等 、木焦油、焦木酸木炭等产品。
、木焦油、焦木酸木炭等产品。请回答下列问题:

(1)木炭中一定含有
(2)下列装置可对木柴干馏后的产品进一步加工。
①用
 装置可除去木煤气中的少量
装置可除去木煤气中的少量 ,混合器应从
,混合器应从 填仪器口字母
填仪器口字母 ,广口瓶中所盛试剂是
,广口瓶中所盛试剂是②木焦油和焦木酸中含有苯、乙酸和甲醛等,他们的部分性质如表所示。
| 物质 | 熔点 | 沸点 | 密度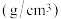 | 溶解性 |
| 苯 | 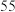 |  | 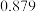 | 不溶于水 |
| 乙酸 | 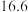 |  |  | 两者互溶且均易溶于水 |
| 甲醇 | 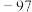 |  |  |
 填装置序号
填装置序号 ,盛装混合液的仪器名称是
,盛装混合液的仪器名称是 填仪器口字母
填仪器口字母 。为保证实验安全,还需要注意的一项操作是
。为保证实验安全,还需要注意的一项操作是
您最近一年使用:0次
【推荐3】氧化铈( )是一种广泛应用的稀土氧化物,具有吸收强紫外线的能力,可以用于光催化降解有机污染物。现以氟碳铈矿(含
)是一种广泛应用的稀土氧化物,具有吸收强紫外线的能力,可以用于光催化降解有机污染物。现以氟碳铈矿(含 、
、 、
、 等)为原料制备氧化铈,其工艺流程如图所示;
等)为原料制备氧化铈,其工艺流程如图所示; 形成复盐沉淀。
形成复盐沉淀。
步骤②中 )发生的反应为:
)发生的反应为: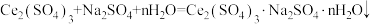
② 在空气中易被氧化为
在空气中易被氧化为 。
。
回答下列问题:
(1) 中
中 元素的化合价为
元素的化合价为___________ 。
(2)滤渣A的主要成分是___________ 。
(3)操作①所需的玻璃实验仪器有烧杯、___________ 。
(4)加入硫脲的目的是___________ 。
(5)步骤④中发生的离子方程式为___________ 。
(6)步骤④中生成的 中
中 的空间构型是
的空间构型是___________ 。
(7)氧化铈的晶体结构如图所示,其已知晶胞参数为a pm,阿伏伽德罗常数为 ,则晶胞中铈离子间最短的距离为
,则晶胞中铈离子间最短的距离为___________ ,晶体密度为___________  (写出计算式)。
(写出计算式)。
 )是一种广泛应用的稀土氧化物,具有吸收强紫外线的能力,可以用于光催化降解有机污染物。现以氟碳铈矿(含
)是一种广泛应用的稀土氧化物,具有吸收强紫外线的能力,可以用于光催化降解有机污染物。现以氟碳铈矿(含 、
、 、
、 等)为原料制备氧化铈,其工艺流程如图所示;
等)为原料制备氧化铈,其工艺流程如图所示; 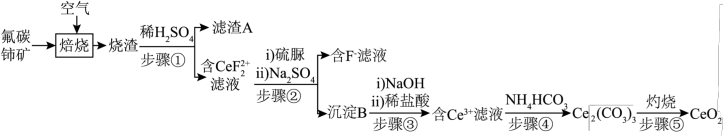
 形成复盐沉淀。
形成复盐沉淀。步骤②中
 )发生的反应为:
)发生的反应为: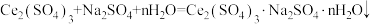
②
 在空气中易被氧化为
在空气中易被氧化为 。
。回答下列问题:
(1)
 中
中 元素的化合价为
元素的化合价为(2)滤渣A的主要成分是
(3)操作①所需的玻璃实验仪器有烧杯、
(4)加入硫脲的目的是
(5)步骤④中发生的离子方程式为
(6)步骤④中生成的
 中
中 的空间构型是
的空间构型是(7)氧化铈的晶体结构如图所示,其已知晶胞参数为a pm,阿伏伽德罗常数为
 ,则晶胞中铈离子间最短的距离为
,则晶胞中铈离子间最短的距离为 (写出计算式)。
(写出计算式)。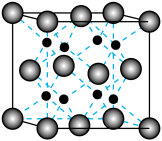
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
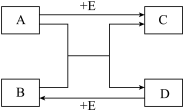
【推荐1】已知A、B、C、D为气体(D的水溶液呈碱性),E、F为固体,G是氯化钙,它们之间的转换关系如图所示:
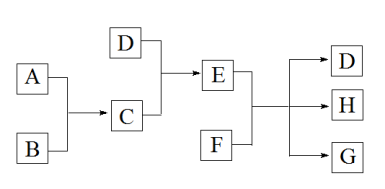
(1)D的电子式为__ ,E的化学式是__ ,H的结构式为__ 。
(2)A和B反应生成C的化学方程式是__ 。
(3)E和F反应生成D、H和G的化学方程式是__ 。
(4)现有浓度为12.5 mol·L-1的C的浓溶液,欲用此浓溶液配制500 mL 0.5 mol·L-1的稀溶液时,需取用浓溶液的体积为__ mL。

(1)D的电子式为
(2)A和B反应生成C的化学方程式是
(3)E和F反应生成D、H和G的化学方程式是
(4)现有浓度为12.5 mol·L-1的C的浓溶液,欲用此浓溶液配制500 mL 0.5 mol·L-1的稀溶液时,需取用浓溶液的体积为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐2】A~H为中学化学中常见的物质,转化关系如图所示,其中“○”代表化合物,“□”代表单质,A为医学上治疗胃酸过多的一种药剂,G为淡黄色固体,C在通常状况下为无色液体。
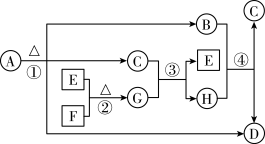
请回答下列问题:
(1)G的化学式为________ 。
(2)反应①②③④中_______ (填序号)属于氧化还原反应。
(3)写出下列反应的化学方程式:
A→B+C+D:_____________________________________ 。
F+C:_____________________________________ 。

请回答下列问题:
(1)G的化学式为
(2)反应①②③④中
(3)写出下列反应的化学方程式:
A→B+C+D:
F+C:
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐1】A、B、C、D均为中学常见物质,且均含有同一种元素,它们之间的部分转化关系如图所示(反应条件及其他物质已经略去):
A B
B C
C D
D
(1)若C为淡黄色固体化合物,且D为强碱,则:
①请写出下列物质的化学式:A____ 。
②请写出C→D的离子方程式:____ 。
(2)若液态A可作制冷剂,D的浓溶液可使铝、铁钝化,则:
①由题给条件可推测出:C____ 。(填化学式)
②写出B→C的化学方程式:____ 。
(3)若A为淡黄色固体单质,且化合物D是重要的工业原料。则:
①B物质为____ (填化学式),通常可用品红溶液来检验,反应现象为____ 。
②Cu与D的浓溶液反应可以生成B,请写出该反应的化学方程式:____ 。
A
 B
B C
C D
D(1)若C为淡黄色固体化合物,且D为强碱,则:
①请写出下列物质的化学式:A
②请写出C→D的离子方程式:
(2)若液态A可作制冷剂,D的浓溶液可使铝、铁钝化,则:
①由题给条件可推测出:C
②写出B→C的化学方程式:
(3)若A为淡黄色固体单质,且化合物D是重要的工业原料。则:
①B物质为
②Cu与D的浓溶液反应可以生成B,请写出该反应的化学方程式:
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐2】某学生为了验证Na2O2能CO2反应,设计出如下实验装置:

(1)A为(用稀盐酸与大理石)制取CO2的装置,最好应从下列图①、②、③中选哪个图:____

(2)B装置的作用是_______________
(3)C装置内可能出现的现象是_________________
(4)为了检验E中收集到的气体,在取出集气瓶后,用带火星的木条伸入集气瓶内,会出现______
(5)D装置中发生反应的方程式为:___

(1)A为(用稀盐酸与大理石)制取CO2的装置,最好应从下列图①、②、③中选哪个图:

(2)B装置的作用是
(3)C装置内可能出现的现象是
(4)为了检验E中收集到的气体,在取出集气瓶后,用带火星的木条伸入集气瓶内,会出现
(5)D装置中发生反应的方程式为:
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐3】如图实验装置用于验证某些物质的性质。在试管A中装入足量的固体NaHCO3,D为固定蚊香的硬纸片。试回答下列问题:
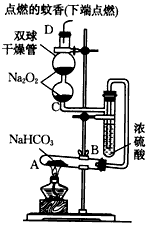
(1)A试管内发生反应________________________________ 。
(2)B装置的作用是___________________________________ 。
(3)在双球干燥管内发生反应的化学方程式为________________________________ ,若无B装置则双球干燥管中还可以发生的化学反应方程式为_______________ 。
(4)双球干燥管内观察到的实验现象是______________________ 。
(5)若将干燥管内的Na2O2换成Na2O,则双球干燥管内观察到的实验现象是__________ 。

(1)A试管内发生反应
(2)B装置的作用是
(3)在双球干燥管内发生反应的化学方程式为
(4)双球干燥管内观察到的实验现象是
(5)若将干燥管内的Na2O2换成Na2O,则双球干燥管内观察到的实验现象是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐1】某校科学兴趣小组探究二氧化碳与过氧化钠反应是否有氧气生成,设计了如图的实验装置。B中盛有饱和碳酸氢钠溶液吸收挥发出的HCI,E为收集氧气装置。
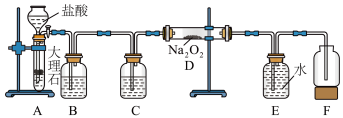
(1)C中盛有__________ ,作用是______________ 。
(2)写出装置D中发生反应的化学方程式______________ 。
(3)指出装置E的错误:________________ 。

(1)C中盛有
(2)写出装置D中发生反应的化学方程式
(3)指出装置E的错误:
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐2】过氧化钠常用作漂白剂、杀菌剂、消毒剂,能与水和二氧化碳等物质发生反应,保存不当时容易变质。某实验小组以过氧化钠为研究对象进行了如下实验。
(1)探究一包 样品是否已经变质:取少量样品,将其溶解,加入
样品是否已经变质:取少量样品,将其溶解,加入____ 溶液,充分振荡后有白色沉淀,证明 已经变质。
已经变质。
(2)该实验小组为了粗略测定过氧化钠的质量分数,称取了mg样品,并设计如图所示装置来测定过氧化钠的质量分数。
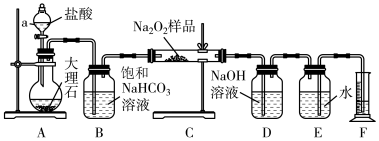
①装置中仪器a的名称是____ ,装置D的作用是____ 。
②将仪器连接好以后,必须进行的第一步操作是____ 。
③写出装置C中发生的主要反应的化学方程式:____ 。
④反应结束后,在读取实验中生成气体的体积时,你认为合理的是____ (填序号)。
A.读取气体体积前,需冷却到室温
B.调整量筒使E、F内液面高度相同
C.视线与凹液面的最低点相平时读取量筒中水的体积
⑤读出量筒内水的体积后,将其折算成氧气的质量为ng,则样品中过氧化钠的质量分数为____ ×100%。
⑥压强不变时在一个密闭容器中放入足量过氧化钠固体,然后充入等体积的 和
和 ,电火花引燃后充分反应,恢复至原温度,余下气体的体积为原体积的
,电火花引燃后充分反应,恢复至原温度,余下气体的体积为原体积的____ 。
(1)探究一包
 样品是否已经变质:取少量样品,将其溶解,加入
样品是否已经变质:取少量样品,将其溶解,加入 已经变质。
已经变质。(2)该实验小组为了粗略测定过氧化钠的质量分数,称取了mg样品,并设计如图所示装置来测定过氧化钠的质量分数。

①装置中仪器a的名称是
②将仪器连接好以后,必须进行的第一步操作是
③写出装置C中发生的主要反应的化学方程式:
④反应结束后,在读取实验中生成气体的体积时,你认为合理的是
A.读取气体体积前,需冷却到室温
B.调整量筒使E、F内液面高度相同
C.视线与凹液面的最低点相平时读取量筒中水的体积
⑤读出量筒内水的体积后,将其折算成氧气的质量为ng,则样品中过氧化钠的质量分数为
⑥压强不变时在一个密闭容器中放入足量过氧化钠固体,然后充入等体积的
 和
和 ,电火花引燃后充分反应,恢复至原温度,余下气体的体积为原体积的
,电火花引燃后充分反应,恢复至原温度,余下气体的体积为原体积的
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐3】现有一定量含有Na2O杂质的Na2O2试样,欲测定Na2O2试样的纯度。可供选用的反应物只有CaCO3固体、6mol·L-1硫酸、6mol·L-1盐酸和蒸馏水。已知:①浓硫酸有吸水性、脱水性和强氧化性,②碱石灰的成分为CaO和NaOH。实验方案为:①制备并提纯CO2。②将纯净的CO2通过试样。③测定生成O2的体积。④根据O2的体积计算Na2O2试样的纯度。实验装置如下:
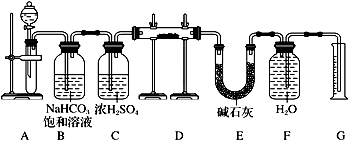
回答下列问题:
(1)装置A中发生反应的离子方程式是______________________________________ 。
(2)装置B的作用是_______________________ ,装置C的作用是_______ 。
(3)装置E的作用是__________________________________________
(4)装置D中发生反应的化学方程式是______________________________________ 。
(5)若开始时测得样品的质量为2.0g,反应结束后测得气体体积为224mL(标准状况),则Na2O2试样的纯度为________ 。

回答下列问题:
(1)装置A中发生反应的离子方程式是
(2)装置B的作用是
(3)装置E的作用是
(4)装置D中发生反应的化学方程式是
(5)若开始时测得样品的质量为2.0g,反应结束后测得气体体积为224mL(标准状况),则Na2O2试样的纯度为
您最近一年使用:0次