已知可逆反应: 。设计如图所示装置(盐桥中的阴、阳离子可以自由移动,盐桥在原电池中不参与反应,只起导电作用)。
。设计如图所示装置(盐桥中的阴、阳离子可以自由移动,盐桥在原电池中不参与反应,只起导电作用)。
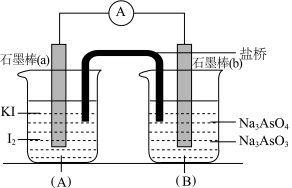
进行如下操作:
(Ⅰ)向(B)烧杯中逐滴加入浓盐酸,发现电流表指针偏转;
(Ⅱ)若改往(B)烧杯中滴加质量分数为40%的NaOH溶液,发现电流表指针向相反方向偏转。
(1)两次操作过程中电流表指针偏转方向为什么会相反?
试用电极反应和化学平衡移动的原理解释此现象:____________________________________ 。
(2)(Ⅰ)操作过程中石墨棒(a)上发生的电极反应为____________________________________ 。
(3)(Ⅱ)操作过程中石墨棒(b)上发生的电极反应为____________________________________ 。
 。设计如图所示装置(盐桥中的阴、阳离子可以自由移动,盐桥在原电池中不参与反应,只起导电作用)。
。设计如图所示装置(盐桥中的阴、阳离子可以自由移动,盐桥在原电池中不参与反应,只起导电作用)。
进行如下操作:
(Ⅰ)向(B)烧杯中逐滴加入浓盐酸,发现电流表指针偏转;
(Ⅱ)若改往(B)烧杯中滴加质量分数为40%的NaOH溶液,发现电流表指针向相反方向偏转。
(1)两次操作过程中电流表指针偏转方向为什么会相反?
试用电极反应和化学平衡移动的原理解释此现象:
(2)(Ⅰ)操作过程中石墨棒(a)上发生的电极反应为
(3)(Ⅱ)操作过程中石墨棒(b)上发生的电极反应为
更新时间:2020-10-07 10:19:55
|
相似题推荐
填空题
|
适中
(0.65)
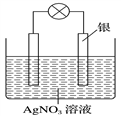
【推荐1】某学习小组依据氧化还原反应:2Ag++Cu===Cu2++2Ag设计成的原电池如图所示,则负极发生的电极反应为__________________________ ;当反应进行到一段时间后取出电极材料,测得某一电极增重了5.4g,则该原电池反应共转移了的电子数目是___________________ 。

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】下图为某化学兴趣小组探究不同条件下化学能转变为电能的装置。请根据原电池原理回答问题:

(1)若电极a为Zn。电极b为Cu。电解质溶液为稀硫酸,该装置工作时, 向
向___ 极(填a或b)移动,经过一段时间后,若导线中转移了0.4mol电子,则产生的气体在标况下的体积为____ 。如果反应太剧烈,为了减缓反应速率而又不减少产生氢气的量,该同学在烧杯中分别加入等体积的下列液体,你认为可行的是____ (填序号)。
A.蒸馏水 B.NaCl溶液 C.Na2CO3溶液 D.CuSO4溶液 E.KNO3溶液
(2)若电极a为Mg,电极b为Al,电解质溶液为氢氧化钠溶液,该原电池工作时,电子从__ 极(填a或b)流出。一段时间后,若反应转移3NA个电子,则理论上的电解质溶液质量变化是___ g。

(1)若电极a为Zn。电极b为Cu。电解质溶液为稀硫酸,该装置工作时,
 向
向A.蒸馏水 B.NaCl溶液 C.Na2CO3溶液 D.CuSO4溶液 E.KNO3溶液
(2)若电极a为Mg,电极b为Al,电解质溶液为氢氧化钠溶液,该原电池工作时,电子从
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】人们利用原电池原理制作了多种电池,以满足日常生活、生产和科学技术等方面的需要。请根据题中提供的信息,回答下列问题。
(1)铅蓄电池在放电时的电池反应为 ,则其正极上的电极反应为
,则其正极上的电极反应为_____ 。
(2) 溶液腐蚀印刷电路铜板时发生反应:
溶液腐蚀印刷电路铜板时发生反应: 。若将此反应设计成原电池,则负极所用的电极材料为
。若将此反应设计成原电池,则负极所用的电极材料为_____ ;电极反应式:____ ;当电路中转移0.2mol电子时,被腐蚀的铜的质量为_____ g。
(3)已知甲醇燃料电池的工作原理如图所示。该电池工作时,b口通入的物质为___ ,该电池正极上的电极反应式为__ ;当6.4g甲醇( )完全反应生成
)完全反应生成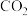 时,有
时,有___ mol电子发生转移。

(1)铅蓄电池在放电时的电池反应为
 ,则其正极上的电极反应为
,则其正极上的电极反应为(2)
 溶液腐蚀印刷电路铜板时发生反应:
溶液腐蚀印刷电路铜板时发生反应: 。若将此反应设计成原电池,则负极所用的电极材料为
。若将此反应设计成原电池,则负极所用的电极材料为(3)已知甲醇燃料电池的工作原理如图所示。该电池工作时,b口通入的物质为
 )完全反应生成
)完全反应生成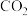 时,有
时,有
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】电化学知识与我们的生产、生活密切相关。回答下列问题:
(1)某兴趣小组同学利用氧化还原反应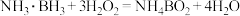 ,设计了如图所示原电池,其中甲、乙两烧杯中各物质的物质的量浓度均为
,设计了如图所示原电池,其中甲、乙两烧杯中各物质的物质的量浓度均为 ,盐桥中装有饱和KCl溶液。
,盐桥中装有饱和KCl溶液。
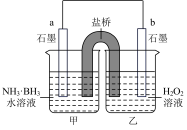
①发生氧化反应的烧杯是___________ (填“甲”或“乙”)。
②外电路的电流方向:从___________ (填“a”或“b”,下同)到___________ 。
③电池工作时,盐桥中的 移向
移向___________ (填“甲”或“乙”)烧杯。
④甲烧杯中发生的电极反应式为___________ 。
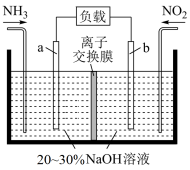
(2)利用反应 (未配平)消除
(未配平)消除 的简易装置如图所示。电极b的反应式为
的简易装置如图所示。电极b的反应式为___________ ,消耗标准状况下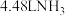 时,被消除的
时,被消除的 的物质的量为
的物质的量为___________ mol。
(1)某兴趣小组同学利用氧化还原反应
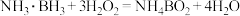 ,设计了如图所示原电池,其中甲、乙两烧杯中各物质的物质的量浓度均为
,设计了如图所示原电池,其中甲、乙两烧杯中各物质的物质的量浓度均为 ,盐桥中装有饱和KCl溶液。
,盐桥中装有饱和KCl溶液。
①发生氧化反应的烧杯是
②外电路的电流方向:从
③电池工作时,盐桥中的
 移向
移向④甲烧杯中发生的电极反应式为
(2)利用反应
 (未配平)消除
(未配平)消除 的简易装置如图所示。电极b的反应式为
的简易装置如图所示。电极b的反应式为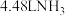 时,被消除的
时,被消除的 的物质的量为
的物质的量为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】电能是现代社会应用最广泛的能源之一、某原电池装置如图所示。其中,
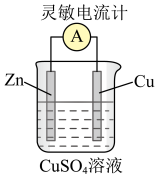
(1)Zn电极为原电池的___________ 极 (填“正” 或“负”)
(2)Cu电极上发生的电极反应式是___________ 。
(3)能证明产生电能的实验现象是___________ 。
(4)2019 年诺贝尔化学奖授予对锂离子电池研究做出突出贡献的科学家。某锂离子电池的工作原理如下。下列说法正确的是___________ (填序号)。
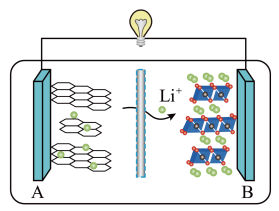
①A为电池的正极
②该装置实现了化学能转化为电能
③电池工作时,电池内部的锂离子定向移动

(1)Zn电极为原电池的
(2)Cu电极上发生的电极反应式是
(3)能证明产生电能的实验现象是
(4)2019 年诺贝尔化学奖授予对锂离子电池研究做出突出贡献的科学家。某锂离子电池的工作原理如下。下列说法正确的是

①A为电池的正极
②该装置实现了化学能转化为电能
③电池工作时,电池内部的锂离子定向移动
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】按要求完成下列问题
I.下列几种微粒或物质
①14C ②16O ③14N ④18O ⑤O2⑥O3
⑦CH3-CH3⑧C2H6⑨CH3- CH2-OH ⑩ CH3-O-CH3
(1)互为同位素的是______ ,(填序号,下同)质子数不同中子数相同的是______________
(2)互为同素异形体的是_________ , 互为同分异构体的是_____________________
II.在25 C、101 kPa的条件下,
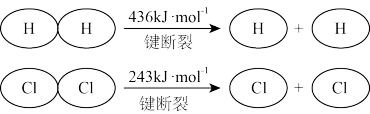
对于反应H2(g)+Cl2(g)= 2HCl(g), 测得生成2 mol HCI(g)时,反应过程中放出183 kJ的热量,则断开1 mol H- Cl键所需的能量是____ kJ.
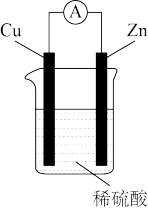
III.如图所示的原电池装置中,正极的电极反应方程式是________________________
I.下列几种微粒或物质
①14C ②16O ③14N ④18O ⑤O2⑥O3
⑦CH3-CH3⑧C2H6⑨CH3- CH2-OH ⑩ CH3-O-CH3
(1)互为同位素的是
(2)互为同素异形体的是
II.在25 C、101 kPa的条件下,

对于反应H2(g)+Cl2(g)= 2HCl(g), 测得生成2 mol HCI(g)时,反应过程中放出183 kJ的热量,则断开1 mol H- Cl键所需的能量是

III.如图所示的原电池装置中,正极的电极反应方程式是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】微生物燃料电池是一种利用微生物将有机物中的化学能直接转化成电能的装置。已知某种利用微生物的甲醇燃料电池中,电解质溶液为酸性,示意图如下:

(1)该电池外电路电子的流动方向为_______ (填“从A到B”或“从B到A”)。
(2)电池工作结束后,B电极室溶液的pH与工作前相比将_______ (填“增大”“减小”或“不变”,溶液体积变化忽略不计)。
(3)A电极附近甲醇发生的电极反应式为_______ 。

(1)该电池外电路电子的流动方向为
(2)电池工作结束后,B电极室溶液的pH与工作前相比将
(3)A电极附近甲醇发生的电极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】如图所示是原电池的装置图。请回答:

(1)若C为稀H2SO4,电流表指针发生偏转,B电极材料为Fe且作负极,则A电极上发生的电极反应式为___ ;反应进行一段时间后溶液C的pH将__ (填“升高”“降低”或“基本不变”)。
(2)若需将反应:Cu+2Fe3+=Cu2++2Fe2+设计成如图所示的原电池装置,则A(负极)极材料为__ ,B(正极)极材料为___ ;溶液C为___ 。
(3)若C为CuCl2溶液,Zn是__ 极,Cu极发生__ 反应,电极反应式为__ 反应过程溶液中c(Cu2+)___ (填“变大”“变小”或“不变”)。

(1)若C为稀H2SO4,电流表指针发生偏转,B电极材料为Fe且作负极,则A电极上发生的电极反应式为
(2)若需将反应:Cu+2Fe3+=Cu2++2Fe2+设计成如图所示的原电池装置,则A(负极)极材料为
(3)若C为CuCl2溶液,Zn是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】回答下列问题:
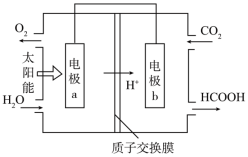
(1)将燃煤产生的二氧化碳回收利用,可达到低碳排放的目的。如图是通过人工光合作用,以CO2和H2O为原料制备HCOOH和O2的原理示意图。电极b表面发生的电极反应为______ 。
(2)浓差电池中的电动势是由于电池中存在浓度差而产生的。某浓差电池的原理如图所示,该电池从浓缩海水中提取LiCl的同时又获得了电能。
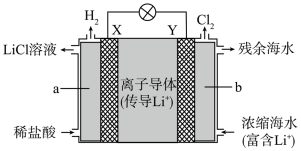
Y电极反应式为______ 。
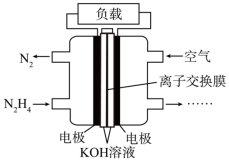
(3)一种以肼(N2H4)为液体燃料的电池装置如图所示。该电池用空气中的氧气作氧化剂,KOH作电解质。负极反应式为______ ;正极反应式为______ 。
(1)将燃煤产生的二氧化碳回收利用,可达到低碳排放的目的。如图是通过人工光合作用,以CO2和H2O为原料制备HCOOH和O2的原理示意图。电极b表面发生的电极反应为

(2)浓差电池中的电动势是由于电池中存在浓度差而产生的。某浓差电池的原理如图所示,该电池从浓缩海水中提取LiCl的同时又获得了电能。

Y电极反应式为
(3)一种以肼(N2H4)为液体燃料的电池装置如图所示。该电池用空气中的氧气作氧化剂,KOH作电解质。负极反应式为

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】以甲烷燃料电池为例来分析在不同的环境中电极反应的书写方法:
(1)酸性条件下燃料电池的负极反应:________________________ 。
(2)碱性条件下燃料电池的负极反应:________________________ 。
(3)固体电解质(高温下能传导O2-)环境中电池的负极反应:_____________________ 。
(4)熔融碳酸盐(如熔融K2CO3)环境中电池的负极反应:______________ 。
(1)酸性条件下燃料电池的负极反应:
(2)碱性条件下燃料电池的负极反应:
(3)固体电解质(高温下能传导O2-)环境中电池的负极反应:
(4)熔融碳酸盐(如熔融K2CO3)环境中电池的负极反应:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】按要求填空。
(1)分别写出下图原电池装置1和2的正极反应方程式:_______________ 。

(2)①汽车发动机工作时会引发 和
和 反应,其能量变化示意图如下。
反应,其能量变化示意图如下。
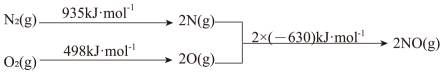
写出该反应的热化学方程式:_____ 。
②在25℃、101kpa下, 气体在足量的氧气中完全燃烧后,恢复至原状态,每转移1mol电子放出热量190kJ,写出该反应的热化学方程式:
气体在足量的氧气中完全燃烧后,恢复至原状态,每转移1mol电子放出热量190kJ,写出该反应的热化学方程式:_____ 。
(1)分别写出下图原电池装置1和2的正极反应方程式:

(2)①汽车发动机工作时会引发
 和
和 反应,其能量变化示意图如下。
反应,其能量变化示意图如下。
写出该反应的热化学方程式:
②在25℃、101kpa下,
 气体在足量的氧气中完全燃烧后,恢复至原状态,每转移1mol电子放出热量190kJ,写出该反应的热化学方程式:
气体在足量的氧气中完全燃烧后,恢复至原状态,每转移1mol电子放出热量190kJ,写出该反应的热化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】完成下列问题。
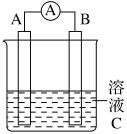
(1)若需将反应:Cu+2Fe3+=Cu2++2Fe2+设计成如下图所示的原电池装置。则A(正极)极材料为___________ ,B(负极)极材料为___________ ,溶液C为___________ ,A(正极)电极上发生反应的类型为___________ (填“氧化”或“还原”)反应,B(负极)电极上发生的电极反应为___________ ,当有1.6g铜溶解时,通过外电路的电子的物质的量为___________ 。
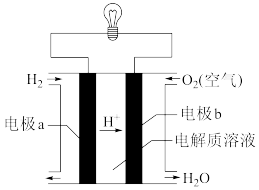
(2)某种氢氧燃料电池是用稀硫酸作电解质溶液,其装置如下图。则电极a是电池的___________ (填“正”或“负”)极,该电池正极的电极反应式为___________ 。
(1)若需将反应:Cu+2Fe3+=Cu2++2Fe2+设计成如下图所示的原电池装置。则A(正极)极材料为

(2)某种氢氧燃料电池是用稀硫酸作电解质溶液,其装置如下图。则电极a是电池的

您最近一年使用:0次



