以甲烷燃料电池为例来分析在不同的环境中电极反应的书写方法:
(1)酸性条件下燃料电池的负极反应:________________________ 。
(2)碱性条件下燃料电池的负极反应:________________________ 。
(3)固体电解质(高温下能传导O2-)环境中电池的负极反应:_____________________ 。
(4)熔融碳酸盐(如熔融K2CO3)环境中电池的负极反应:______________ 。
(1)酸性条件下燃料电池的负极反应:
(2)碱性条件下燃料电池的负极反应:
(3)固体电解质(高温下能传导O2-)环境中电池的负极反应:
(4)熔融碳酸盐(如熔融K2CO3)环境中电池的负极反应:
更新时间:2019/05/20 09:18:02
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】我国首创以铝─空气─海水电池为能源的新型海水标志灯。该灯以海水为电解质溶液,靠空气中的氧气使铝不断氧化而产生电流。只要把灯放入海水中数分钟,就会发出耀眼的白光,其能量比干电池高20─50倍(海水呈弱碱性),请回答:该电源负极材料是_____ ,正极主要的反应物质是_____ ,总反应方程为:____________________
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】氢能是发展中的新能源,它的利用包括氢的制备和储存。回答下列问题:
(1)图为碱性氢氧燃料电池的示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定。请回答:
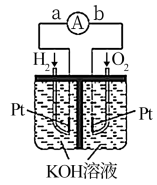
①在导线中电子流动方向为_______ (用a、b表示)
②正极反应式为_______ 。
(2)氢氧燃料电池工作时,H2和O2连续由外部供给,因此,储氢是关键技术之一。
①某些金属氢化物也可做储氢材料,在恒温恒容的密闭容器中,某储氢反应: 达到化学平衡。下列有关叙述正确的是
达到化学平衡。下列有关叙述正确的是_______ 。
a.v(放氢)=v(吸氢)
b.吸收y mol H2只需1 mol MHx
c.若通入惰性气体Ar,压强增大,反应速率增大
d.容器内气体压强保持不变
②金属锂是一种重要的储氢材料,吸氢和放氢原理如下:
I.2Li+H2 2LiH
2LiH
Ⅱ.LiH+H2O=LiOH+H2↑
用锂吸收224 L(标准状况)H2,生成的LiH与H2O作用,放出的H2用作电池燃料,若能量转化率为80%,则导线中通过电子的物质的量为_______ mol。
(3)利用太阳能直接分解水制氢,是最具吸引力的制氢途径,其能量转化形式为_______ 。
(1)图为碱性氢氧燃料电池的示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定。请回答:

①在导线中电子流动方向为
②正极反应式为
(2)氢氧燃料电池工作时,H2和O2连续由外部供给,因此,储氢是关键技术之一。
①某些金属氢化物也可做储氢材料,在恒温恒容的密闭容器中,某储氢反应:
 达到化学平衡。下列有关叙述正确的是
达到化学平衡。下列有关叙述正确的是a.v(放氢)=v(吸氢)
b.吸收y mol H2只需1 mol MHx
c.若通入惰性气体Ar,压强增大,反应速率增大
d.容器内气体压强保持不变
②金属锂是一种重要的储氢材料,吸氢和放氢原理如下:
I.2Li+H2
 2LiH
2LiH Ⅱ.LiH+H2O=LiOH+H2↑
用锂吸收224 L(标准状况)H2,生成的LiH与H2O作用,放出的H2用作电池燃料,若能量转化率为80%,则导线中通过电子的物质的量为
(3)利用太阳能直接分解水制氢,是最具吸引力的制氢途径,其能量转化形式为
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】铁及其化合物在生活、生产中有广泛应用。铁元素的价类二维图如图所示,其中的箭头表示部分物质间的转化关系。
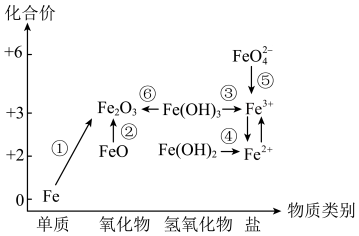
请回答下列问题:
(1)图中反应①的转化正确的是___________ (填字母)。
A.铁在氧气中燃烧
B.铁与高温水蒸气的反应
C.铁在常温下发生吸氧腐蚀生成铁锈
(2)工业上可用 氧化酸性
氧化酸性 废液制备
废液制备 。
。
①写出 氧化酸性
氧化酸性 废液制备
废液制备 的离子方程式为
的离子方程式为___________ 。
②利用上述方法制备 后,经一系列操作得
后,经一系列操作得 固体,欲检验该
固体,欲检验该 固体中是否含
固体中是否含 ,应该进行的实验操作是取少量
,应该进行的实验操作是取少量 固体于试管中,加入适量水溶解,再加入
固体于试管中,加入适量水溶解,再加入___________ (填名称)溶液,若产生蓝色沉淀,说明含有 ,否则不含
,否则不含 。
。
(3)由上图预测,下列说法正确的是___________(填字母)。
(4)黄铁矿( )是生产硫酸和冶炼钢铁的重要原料,其中一个反应为:
)是生产硫酸和冶炼钢铁的重要原料,其中一个反应为: ,反应生成的
,反应生成的 可用于炼铁。请你预测
可用于炼铁。请你预测 与
与 两种化合物中,化学键的类型
两种化合物中,化学键的类型___________ (填“相同”或“不同”)。
(5)“热电池”在航空航天领域有广泛应用。其工作原理如图所示,电池放电时,1 mol 完全反应时转移4 mol电子。下列说法正确的是___________(填字母)。
完全反应时转移4 mol电子。下列说法正确的是___________(填字母)。


请回答下列问题:
(1)图中反应①的转化正确的是
A.铁在氧气中燃烧
B.铁与高温水蒸气的反应
C.铁在常温下发生吸氧腐蚀生成铁锈
(2)工业上可用
 氧化酸性
氧化酸性 废液制备
废液制备 。
。①写出
 氧化酸性
氧化酸性 废液制备
废液制备 的离子方程式为
的离子方程式为②利用上述方法制备
 后,经一系列操作得
后,经一系列操作得 固体,欲检验该
固体,欲检验该 固体中是否含
固体中是否含 ,应该进行的实验操作是取少量
,应该进行的实验操作是取少量 固体于试管中,加入适量水溶解,再加入
固体于试管中,加入适量水溶解,再加入 ,否则不含
,否则不含 。
。(3)由上图预测,下列说法正确的是___________(填字母)。
A. 、 、 、 、 均可通过化合反应制备 均可通过化合反应制备 |
B.加热 可实现转化⑥,加水溶解可实现转化③ 可实现转化⑥,加水溶解可实现转化③ |
C. 相当于FeO和 相当于FeO和 组成的混合物 组成的混合物 |
D.高铁酸盐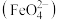 可作净水剂 可作净水剂 |
(4)黄铁矿(
 )是生产硫酸和冶炼钢铁的重要原料,其中一个反应为:
)是生产硫酸和冶炼钢铁的重要原料,其中一个反应为: ,反应生成的
,反应生成的 可用于炼铁。请你预测
可用于炼铁。请你预测 与
与 两种化合物中,化学键的类型
两种化合物中,化学键的类型(5)“热电池”在航空航天领域有广泛应用。其工作原理如图所示,电池放电时,1 mol
 完全反应时转移4 mol电子。下列说法正确的是___________(填字母)。
完全反应时转移4 mol电子。下列说法正确的是___________(填字母)。
A.电流流向:Li(Al)极→用电器→ 极 极 |
| B.负极质量减少27 g时理论上有3 mol阴离子向负极迁移 |
C.正极的电极反应式为 |
D.如果用 替代 替代 ,电极反应和电池反应都不变化 ,电极反应和电池反应都不变化 |
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】人们利用原电池原理制作了多种电池,以满足日常生活、生产和科学技术等方面的需要。请根据题中提供的信息,回答下列问题。
(1)铅蓄电池在放电时的总反应为 ,则其正极反应为
,则其正极反应为___ 。
(2)FeCl3溶液腐蚀印刷电路铜板时发生反应: ,若将此反应设计成原电池,则负极所用的电极材料为
,若将此反应设计成原电池,则负极所用的电极材料为___ ,电极反应式:___ 。
(3)已知甲醇燃料电池的工作原理如图所示,该电池工作时,b口通入的物质为___ (填化学式),该电池正极上的电极反应式为___ ;当6.4g甲醇(CH3OH)完全反应生成CO2时,有___ mol电子发生转移。若将电池的电解质溶液换为KOH溶液,则负极反应式为____ 。
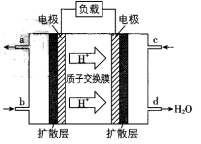
(1)铅蓄电池在放电时的总反应为
 ,则其正极反应为
,则其正极反应为(2)FeCl3溶液腐蚀印刷电路铜板时发生反应:
 ,若将此反应设计成原电池,则负极所用的电极材料为
,若将此反应设计成原电池,则负极所用的电极材料为(3)已知甲醇燃料电池的工作原理如图所示,该电池工作时,b口通入的物质为

您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】天然气的主要成分为CH4,一般还含有C2H6等烃类,是重要的燃料和化工原料。
(1)乙烷在一定条件可发生如下反应:C2H6(g)=C2H4(g)+H2(g) ΔH1,相关物质的摩尔燃烧焓数据如表所示:
则ΔH1=___________ kJ·mol-1
(2)以CH4为原料设计原电池电解下列物质,如图:
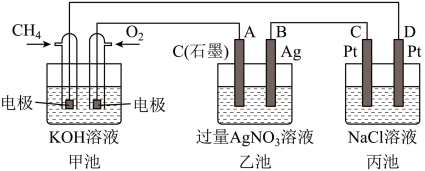
①甲池是将___________ 能转化为___________ 能的装置,乙装置中电极A的名称是___________ 。(填“正极”或“负极”或“阴极”或“阳极”)。
②甲装置中通入O2的电极反应式为___________ ,乙装置中电极B (Ag)的电极反应式为 ___________ ,丙装置中D极的产物是(写化学式) ___________ 。
③一段时间,当C极上产生5.6L(标准状况下)气体时,电路中转移___________ mol电子。若要使乙池恢复电解前的状态,应向乙池中加入 ___________ (写化学式)。
(1)乙烷在一定条件可发生如下反应:C2H6(g)=C2H4(g)+H2(g) ΔH1,相关物质的摩尔燃烧焓数据如表所示:
| 物质 | C2H6(g) | C2H4(g) | H2(g) |
| 摩尔燃烧焓ΔH/(kJ·mol-1) | -1560 | -1411 | -286 |
(2)以CH4为原料设计原电池电解下列物质,如图:

①甲池是将
②甲装置中通入O2的电极反应式为
③一段时间,当C极上产生5.6L(标准状况下)气体时,电路中转移
您最近半年使用:0次
【推荐3】(1)海水中的钠盐、镁盐等都是重要的化工原料,从海水中提取铀、重水对一个国家来说具有战略意义。
①写出氯化镁的电子式__________________________
②重水的摩尔质量为____________________________
③写出金属镁的工业冶炼方程式_____________________ 
④海水淡化的常见方法有电渗析法、离子交换法、_________________
(2)比赛中,当运动员肌肉挫伤或扭伤时,随队医生即对准受伤部位喷射氯乙烷(沸点12.27℃)进行局部冷冻麻醉应急处理。
①乙烯和氯化氢在一定条件下反应的化学方程式是____________________________
②决定氯乙烷能用于冷冻麻醉应急处理的具体性质是________ (填选项)
A.沸点低 B.沸点高 C.易挥发 D.难挥发
③甲烷与氯气光照下反应生成产物共________ 种
(3)“可燃冰”是天然气与水相互作用形成的晶体物质,若把“可燃冰”(用甲烷表示)燃烧在一定条件下改装成原电池,则在原电池的负极发生反应的物质是__________________________
四、解答题
①写出氯化镁的电子式
②重水的摩尔质量为
③写出金属镁的工业冶炼方程式

④海水淡化的常见方法有电渗析法、离子交换法、
(2)比赛中,当运动员肌肉挫伤或扭伤时,随队医生即对准受伤部位喷射氯乙烷(沸点12.27℃)进行局部冷冻麻醉应急处理。
①乙烯和氯化氢在一定条件下反应的化学方程式是
②决定氯乙烷能用于冷冻麻醉应急处理的具体性质是
A.沸点低 B.沸点高 C.易挥发 D.难挥发
③甲烷与氯气光照下反应生成产物共
(3)“可燃冰”是天然气与水相互作用形成的晶体物质,若把“可燃冰”(用甲烷表示)燃烧在一定条件下改装成原电池,则在原电池的负极发生反应的物质是
四、解答题
您最近半年使用:0次



