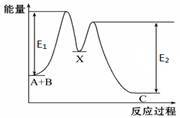
已知反应热:①25℃、101kPa时,2C(s)+O2(g) =2CO(g) ΔH=-221kJ/mol;②稀溶液中,H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3kJ/mol弱电解质电离时吸热。
下列结论正确的是
下列结论正确的是
| A.C的燃烧热大于110.5kJ/mol |
| B.①的反应热为221kJ/mol |
| C.稀硫酸与稀NaOH溶液反应的中和热为-57.3kJ/mol |
| D.稀盐酸与稀氨水反应生成1mol水,放出57.3kJ热量 |
更新时间:2020-10-09 15:44:37
|
相似题推荐
单选题
|
较易
(0.85)
名校
【推荐1】我国有较多的科研人员在研究甲醛的氧化,有人提出HCHO与O2在羟基磷灰石(HAP)表面催化氧化生成CO2、H2O的历程,该历程示意图如图(图中只画出了HAP的部分结构)。
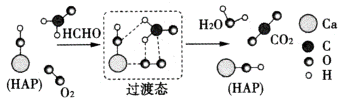
下列说法正确的是

下列说法正确的是
| A.该过程中有极性键形成 |
| B.HCHO在反应过程中有C=O键发生断裂 |
| C.根据图示信息,CO2分子中的氧原子全部来自O2 |
| D.HAP能提高HCHO与O2反应的活化能,但不改变焓变 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】乙烯与水发生加成反应制备乙醇的能量变化过程如所示,下列说法错误的是
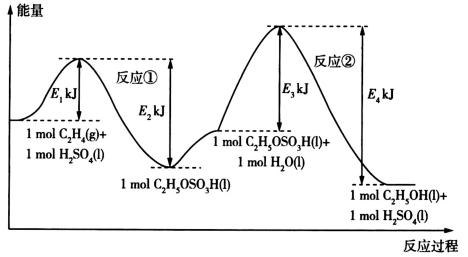

| A.乙烯与水发生加成反应制备乙醇的总反应的ΔH<0 |
| B.制备过程的速率主要由反应②决定 |
| C.由图可知1molC2H4(g)的总能量高于1molC2H5OH(l)的总能量 |
| D.C2H5OSO3H(l)+H2O(l)=C2H5OH(l)+H2SO4(l) ΔH=(E4-E3)kJ•mol-1 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】将 溶液和
溶液和 未知浓度的
未知浓度的 溶液混合均匀后测量并记录溶液温度,实验结果如图所示(实验中始终保持
溶液混合均匀后测量并记录溶液温度,实验结果如图所示(实验中始终保持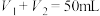 )。下列叙述正确的是
)。下列叙述正确的是

 溶液和
溶液和 未知浓度的
未知浓度的 溶液混合均匀后测量并记录溶液温度,实验结果如图所示(实验中始终保持
溶液混合均匀后测量并记录溶液温度,实验结果如图所示(实验中始终保持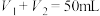 )。下列叙述正确的是
)。下列叙述正确的是
A.做该实验时环境温度为 |
| B.实验可用环形铜丝搅拌棒替代环形玻璃搅拌棒 |
C. 溶液的浓度约是 溶液的浓度约是 |
D.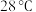 以后温度降低的原因是有一部分热量从体系散失到了环境中 以后温度降低的原因是有一部分热量从体系散失到了环境中 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】下列热化学方程式书写和表示正确的是(△H的绝对值均正确)
A.2SO2(g)+O2(g) 2SO3(g)△H=-196kJ/mol(反应热) 2SO3(g)△H=-196kJ/mol(反应热) |
| B.CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H=-890.3kJ/mol(燃烧热) |
| C.NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l)△H=+57.3kJ/mol(中和热) |
| D.2NO2=O2+2NO△H=-116.2kJ/mol(反应热) |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】下列有关热化学方程式及其叙述正确的是
| A.氢气的燃烧热为285.5 kJ·mol-1,则水分解的热化学方程式为:2H2O(l)===2H2(g)+O2(g) ΔH=+285.5 kJ·mol-1 |
| B.已知2C(石墨,s)+O2(g)===2CO(g)ΔH=-221 kJ·mol-1,则石墨的燃烧热为110.5 kJ·mol-1 |
C.已知N2(g)+3H2(g) 2NH3(g) ΔH=-92.4 kJ·mol-1,则在一定条件下将1 mol N2和3 mol H2置于一密闭容器中充分反应后,最多可放出92.4 kJ的热量 2NH3(g) ΔH=-92.4 kJ·mol-1,则在一定条件下将1 mol N2和3 mol H2置于一密闭容器中充分反应后,最多可放出92.4 kJ的热量 |
| D.已知C(石墨,s)==C(金刚石,s)ΔH>0,则石墨比金刚石稳定 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】下列有关化学用语表示正确的是
| A.潮湿空气中铁钉发生吸氧腐蚀时的负极反应为:Fe-3e-=Fe3+ |
| B.HClO的电离方程式:HClO=H++ClO- |
| C.由反应2H2(g)+O2(g)=2H2O(l) ΔH=-571.6kJ•mol-1可知,H2的燃烧热为285.8kJ•mol-1 |
D.Na2C2O4水解的离子方程式:C2O +2H2O +2H2O H2C2O4+2OH- H2C2O4+2OH- |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐3】下列关于反应能量的说法正确的是
| A.Zn(s)+CuSO4(aq)=ZnSO4(aq)+Cu(s)△H=-216kJ•mol-1,则反应物总能量大于生成物总能量 |
| B.吸热反应中由于反应物总能量小于生成物总能量,因而没有价值 |
| C.101kPa时,2H2(g)+O2(g)=2H2O(l)△H=-571.6k•mol-1,则H2的燃烧热为571.6k•mol-1 |
| D.已知H+(aq)+OH-(aq)=H2O(1)△H=-57.3kJ•mol-1,则含1 mol NaOH的溶液与含0.5molH2SO4的浓硫酸混合后放出57.3kJ的热量 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】已知反应:①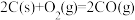
 ,②
,②
 。下列结论正确的是
。下列结论正确的是
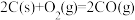
 ,②
,②
 。下列结论正确的是
。下列结论正确的是| A.碳的燃烧热大于110.5 kJ·mol−1 |
| B.①的反应热为221 kJ·mol−1 |
| C.浓硫酸与稀NaOH溶液反应生成1mol水,放出57.3 kJ热量 |
| D.稀醋酸与稀NaOH溶液反应生成1mol水,放出57.3 kJ热量 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】下列说法正确的是
A. 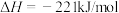 ,则碳的燃烧热等于110.5kJ/mol ,则碳的燃烧热等于110.5kJ/mol |
B.C(石墨,s)=C(金刚石,s)  ,则金刚石比石墨稳定 ,则金刚石比石墨稳定 |
C.  ,则碳酸钙常温下不稳定 ,则碳酸钙常温下不稳定 |
D.用 溶液和NaOH溶液反应测定中和热: 溶液和NaOH溶液反应测定中和热: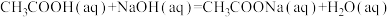 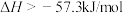 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐3】下列说法正确的是( )
| A.燃烧热和中和热的数值都会随反应物的用量不同而改变,故1molS(s)和2molS(s)的燃烧热不相等 |
| B.已知:2C(s)+2O2(g)=2CO2(g) ΔH=akJ/mol,2C(s)+O2(g)=2CO(g)ΔH=bkJ/mol,则a>b |
| C.H2(g)的燃烧热为285.8kJ/mol,则表示H2燃烧热的热化学方程式为:2H2(g)+O2(g)=2H2O(l)ΔH=-571.6kJ/mol |
| D.反应NH4HCO3(s)=NH3(g)+H2O(g)+CO2(g) ΔH=+185.57kJ/mol,在低温条件下不能自发进行,但在高温条件下能自发进行 |
您最近一年使用:0次