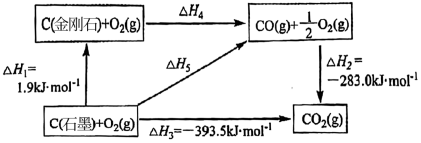
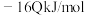下列依据热化学方程式得出的结论正确的是( )
| 选项 | 热化学方程式 | 结论 |
| A | 2C(石墨)+O2(g)=2CO(g)ΔH=-222kJ·mol-1 | 石墨的燃烧热为111kJ/mol |
| B | OH-(aq)+H+(aq)=H2O(g)△H=-57.3kJ/mol | 含1molNaOH的稀溶液与浓H2SO4完全中和,放出热量小于57.3kJ |
| C | 2C(s)+2O2(g)=2CO2(g)△H=-akJ/mol 2C(s)+O2(g)=2CO(g)△H=-bkJ/mol | b<a |
| D | C(石墨,s)=C(金刚石,s)△H=+1.5kJ/mol | 金刚石比石墨稳定 |
| A.A | B.B | C.C | D.D |
更新时间:2020-10-11 12:53:22
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】2-甲基丙烯与HCl的加成反应有两种产物,这两种加成反应过程与其相应的能量变化曲线关系如下图所示。在恒容绝热密闭容器中通入一定量的2-甲基丙烯与HCl的混合物进行有关反应。下列说法正确的是
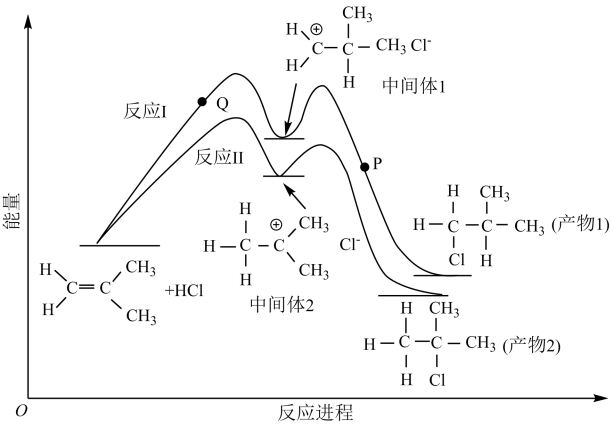

| A.产物稳定性的强弱:产物1>产物2 |
| B.反应的活化能大小:反应I>反应II |
| C.升高温度,反应I的逆反应速率变化值小于反应II的逆反应速率变化值 |
D.2-甲基丙烯与 的加成反应产物中, 的加成反应产物中,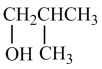 更稳定 更稳定 |
您最近一年使用:0次
【推荐2】下列依据热化学方程式得出的结论正确的是
| 选项 | 热化学方程式 | 结论 |
| A | 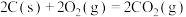    |  |
| B |  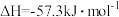 | 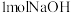 的稀溶液与稀醋酸完全中和,放出热量等于 的稀溶液与稀醋酸完全中和,放出热量等于 |
| C | 500℃、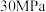 下, 下,   | 将 和过量的 和过量的 在此条件下充分反应,放出热量 在此条件下充分反应,放出热量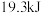 |
| D |   |  的燃烧热 的燃烧热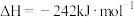 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】下列有关热化学方程式的叙述正确的是
A.在100℃、101kpa条件下,1mol液态水汽化时需要吸收40.69kJ的热量,则 的 的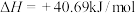 |
B.已知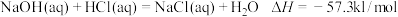 ,则含40.0gNaOH的稀溶液与稀醋酸完全中和,会放出小于57.3kJ的热量 ,则含40.0gNaOH的稀溶液与稀醋酸完全中和,会放出小于57.3kJ的热量 |
C.已知 , ,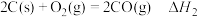 ,则 ,则 |
D.1molS完全燃烧放热297.3kJ,其热化学方程式为 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】根据对应信息书写的热化学方程式,正确的是
A.稀盐酸与NaOH稀溶液反应生成1 mol水放出57.3 kJ热量。醋酸与NaOH溶液反应的热化学方程式:  |
B.在一定条件下,0.1 mol硫粉与0.1 mol铁粉反应生成0.1 mol硫化亚铁固体时,放出9.56 kJ热量,则: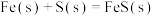 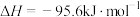 |
C.氢气的燃烧热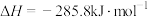 ,则: ,则: 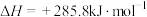 |
D.碳的燃烧热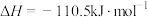 ,则: ,则: 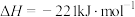 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】下列有关热化学方程式的叙述,正确的是
| A.1mol甲烷燃烧生成气态水和二氧化碳所放出的热量是甲烷的燃烧热 |
| B.由N2O4(g)⇌2NO2(g) ΔH=-56.9kJ·mol-1,可知将1molN2O4(g)置于密闭容器中充分反应后放出热量为56.9kJ |
| C.由:H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3kJ·mol-1,可知:含1molCH3COOH的溶液与含1molNaOH的溶液混合,放出热量为57.3kJ |
| D.已知101kPa时,2C(s)+O2(g)=2CO(g) ΔH=-221kJ·mol-1,则1mol碳完全燃烧放出的热量大于110.5kJ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列说法正确的是
| A.C2H5OH(l)+3O2(g)=2CO2(g)+3H2O(g) △H=-1234.8kJ·mol-1 结论:C2H5OH的燃烧热 △H=-1234.8 kJ·mol-1 |
| B.稀溶液中有H+(aq)+OH-(aq)=H2O(l) △H=-57.3 kJ·mol-1 结论:将稀醋酸与NaOH的稀溶液混合后,若有1 mol H2O生成,则放出的能量等于57.3kJ |
| C.C(s,石墨)=C(s,金刚石) △H=+1.5kJ·mol-1 结论:相同条件下金刚石比石墨稳定 |
D.Sn(s,灰)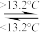 Sn(s,白) △H=+2.1kJ·mol-1(灰锡为粉末状) Sn(s,白) △H=+2.1kJ·mol-1(灰锡为粉末状)结论:锡制品在寒冷的冬天更容易损坏 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列热化学方程式中的反应热下划线处表示燃烧热 的是 ( )
A.NH3(g) + O2(g) = NO(g) + O2(g) = NO(g) +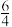 H2O(g) ΔH=-a kJ·mol-1 H2O(g) ΔH=-a kJ·mol-1 |
| B.C6H12O6(s) + 6O2(g) = 6CO2(g) + 6H2O(g) ΔH=-b kJ·mol-1 |
C.CO(g) + O2(g) = CO2(g) ΔH=-c kJ·mol-1 O2(g) = CO2(g) ΔH=-c kJ·mol-1 |
D.CH3CH2OH(l) + O2(g) = CH3CHO(l) + H2O(l) ΔH=-d kJ·mol-1 O2(g) = CH3CHO(l) + H2O(l) ΔH=-d kJ·mol-1 |
您最近一年使用:0次



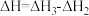
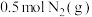 和
和 置于密闭容器中充分反应生成
置于密闭容器中充分反应生成 放热19.3kJ,其热化学方程式为:
放热19.3kJ,其热化学方程式为:

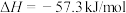 ,则
,则 和
和 反应的反应热
反应的反应热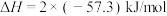
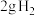 完全燃烧生成液态水放出285.8 kJ热量,氢气燃烧的热化学方程式表示为:
完全燃烧生成液态水放出285.8 kJ热量,氢气燃烧的热化学方程式表示为: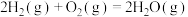
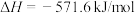
 生成正盐,需5mol/L的NaOH溶液100ml,则丁烷的燃烧热为
生成正盐,需5mol/L的NaOH溶液100ml,则丁烷的燃烧热为