下列依据热化学方程式得出的结论正确的是
| 选项 | 热化学方程式 | 结论 |
| A | 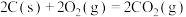    |  |
| B |  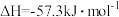 | 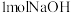 的稀溶液与稀醋酸完全中和,放出热量等于 的稀溶液与稀醋酸完全中和,放出热量等于 |
| C | 500℃、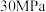 下, 下,   | 将 和过量的 和过量的 在此条件下充分反应,放出热量 在此条件下充分反应,放出热量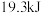 |
| D |   |  的燃烧热 的燃烧热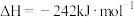 |
| A.A | B.B | C.C | D.D |
更新时间:2021-11-13 14:48:49
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】下列说法或表示法正确的是
| A.测定HCl和NaOH中和热时,每次实验均应测量三个温度,即盐酸起始温度、NaOH起始温度和反应体系的最高温度 |
| B.由“C(石墨;S)=C(金刚石;S);△H = +1.19kJ/mol ”可知金刚石比石墨稳定 |
| C.在稀溶液中: H++OH-=H2O;△H=-57.3kJ/mol,若将含0.5molH2SO4的浓硫酸与含1molNaOH的溶液混合,放出的热量等于57.3kJ |
| D.在101kPa时,2gH2完全燃烧生成液态水,放出285.8kJ热量,表示氢气燃烧热的热化学方程式为:2H2(g)+O2(g)=2H2O(l);△H= -571.6 kJ/mol |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】如图是金属镁和卤素单质(X2)反应的能量变化示意图,下列说法正确的是


| A.热稳定性:MgCl2<MgF2 |
| B.Mg(s)+X2(g)=MgX2(s) ΔH>0 |
| C.将MgCl2溶液蒸干可得到无水MgCl2 |
| D.该温度下MgI2(s)+Br2(g)=MgBr2(s)+I2(g) ΔH=+160kJ•mol-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】NA为阿伏加 德罗常数的值。下列说法正确的是
| A.H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3 kJ•mol-1,则氨水与盐酸反应生成1mol H2O(l)放热57.3 kJ |
B.S2O +2H+=S↓+SO2↑+H2O,则每生成22.4LSO2转移电子数为2NA +2H+=S↓+SO2↑+H2O,则每生成22.4LSO2转移电子数为2NA |
| C.14g乙烯和丙烯的混合物完全燃烧时,产生CO2 分子数为NA |
| D.1 molCl2溶于水,溶液中Cl-、ClO-和HClO的微粒数之和为2NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列说法或表示法不正确的是
| A.测定HCl和NaOH的中和热时,每次实验均应测量三个温度,即盐酸起始温度、NaOH起始温度和反应后的终止温度 |
| B.在101 kPa时,2 g H2完全燃烧生成液态水,放出285.8 kJ热量,氢气燃烧的热化学方程式表示为H2(g)+1/2O2(g)===H2O(l);ΔH=-285.8 kJ·mol-1 |
| C.Zn(s)+CuSO4(aq)== ZnSO4(aq)+Cu(s) ΔH=-216 kJ/mol,E反应物>E生成物 |
| D.放热反应不需要任何条件即可发生 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】下列说法或表示方法正确的是
| A.等物质的量的硫蒸气和硫固体分别完全燃烧,后者放出热量多 |
| B.由C(s,石墨)=C(s,金刚石)ΔH=+1.90kJ·mol-1可知金刚石比石墨坚硬 |
| C.在101kPa时,2gH2完全燃烧生成液态水,放出285.8kJ热量,氢气燃烧的热化学方程式表示为2H2(g)+O2(g)=2H2O(l) ΔH=-285.8kJ·mol-1 |
| D.在稀溶液中,H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3kJ·mol-1,若将含0.5molH2SO4的浓硫酸与含1molNaOH的溶液混合,放出的热量大于57.3kJ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列关于热化学反应的描述中正确的是
| A.HCl和NaOH反应的中和热ΔH=-57.3 kJ/mol,则H2SO4和Ca(OH)2反应的中和热ΔH=2×(—57.3) kJ/mol |
| B.CO(g)的燃烧热是283.0 kJ/mol,则2CO2(g)=2CO(g)+O2(g)反应的ΔH=+2×283.0 kJ/mol |
| C.需要加热才能发生的反应一定是吸热反应 |
| D.1mol NO(g)中的化学键形成时需要吸收632 kJ的能量 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列说法正确的是
| A.吸热反应一定需要加热才能进行 |
| B.只有不需要任何条件就能够自动进行的反应才是自发反应 |
C.已知 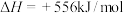 则CO的燃烧热 则CO的燃烧热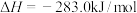 |
D.已知  ; ;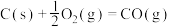  ,则 ,则 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】下列说法或表示正确的是
| A.等物质的量的硫蒸气和硫固体分别完全燃烧,后者放出热量多 |
| B.物质发生化学变化时一定伴随着放热现象 |
| C.稀溶液中:H+(aq)+OH﹣(aq)=H2O(l);△H=﹣57.3kJ/mol,若将含0.5molH2SO4的浓硫酸与含l mol NaOH的溶液混合,放出的热量大于57.3kJ |
| D.在25℃101kPa时,2gH2完全燃烧生成液态水,放出285.8kJ的热量,则H2燃烧的热化学方程式为:2H2(g)+O2(g)═2H2O(l);△H=﹣285.8kJ/mol |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】在一定条件下, 和
和 燃烧的热化学方程式分别为
燃烧的热化学方程式分别为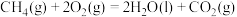
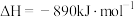 ,
,
 。若某
。若某 和CO的混合气体充分燃烧,放出的热量为262.9kJ,生成的
和CO的混合气体充分燃烧,放出的热量为262.9kJ,生成的 用过量的饱和石灰水完全吸收,得到50g白色沉淀。则混合气体中
用过量的饱和石灰水完全吸收,得到50g白色沉淀。则混合气体中 和
和 的体积比为
的体积比为
 和
和 燃烧的热化学方程式分别为
燃烧的热化学方程式分别为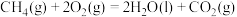
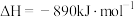 ,
,
 。若某
。若某 和CO的混合气体充分燃烧,放出的热量为262.9kJ,生成的
和CO的混合气体充分燃烧,放出的热量为262.9kJ,生成的 用过量的饱和石灰水完全吸收,得到50g白色沉淀。则混合气体中
用过量的饱和石灰水完全吸收,得到50g白色沉淀。则混合气体中 和
和 的体积比为
的体积比为| A.1:2 | B.1:3 | C.2:1 | D.2:3 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】已知可逆反应2SO2+ O2 2SO3,当生成2 mol SO3时放出热量为Q,现将1 mol SO2和0.5 mol O2在相同条件下反应生成SO3放出的热量为Q1,则( )
2SO3,当生成2 mol SO3时放出热量为Q,现将1 mol SO2和0.5 mol O2在相同条件下反应生成SO3放出的热量为Q1,则( )
 2SO3,当生成2 mol SO3时放出热量为Q,现将1 mol SO2和0.5 mol O2在相同条件下反应生成SO3放出的热量为Q1,则( )
2SO3,当生成2 mol SO3时放出热量为Q,现将1 mol SO2和0.5 mol O2在相同条件下反应生成SO3放出的热量为Q1,则( )A.Q1 < | B.Q1 =  | C.2Q1 > Q | D.无法判断 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】温度为T1时,向容积为2 L 的密闭容器甲、乙中分别充入一定量的CO(g)和H2O(g),发生反应:CO(g) + H2O(g)  CO2(g) + H2(g) ∆H = -41 kJ/mol。数据如下,下列说法
CO2(g) + H2(g) ∆H = -41 kJ/mol。数据如下,下列说法不正确 的是
 CO2(g) + H2(g) ∆H = -41 kJ/mol。数据如下,下列说法
CO2(g) + H2(g) ∆H = -41 kJ/mol。数据如下,下列说法| 容器 | 甲 | 乙 | ||
| 反应物 | CO | H2O | CO | H2O |
| 起始时物质的量(mol) | 1.2 | 0.6 | 2.4 | 1.2 |
| 平衡时物质的量(mol) | 0.8 | 0.2 | a | b |
| A.甲容器中,平衡时,反应放出的热量为16.4 kJ |
| B.T1时,反应的平衡常数K甲 = 1 |
| C.平衡时,乙中CO的浓度是甲中的2倍 |
| D.乙容器中,平衡时CO的转化率约为75% |
您最近一年使用:0次

 时,
时, 完全燃烧生成液态水,放出
完全燃烧生成液态水,放出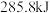 热量,氢气燃烧的热化学方程式为
热量,氢气燃烧的热化学方程式为
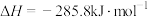
 ,则
,则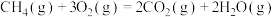

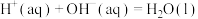
 ,若将含
,若将含 的浓硫酸与含
的浓硫酸与含 的溶液混合,放出的热量等于
的溶液混合,放出的热量等于 ,则金刚石比石墨稳定
,则金刚石比石墨稳定

