某固体化合物X由三种元素组成,室温条件下易分解。为研究它的组成和性质,进行如下实验:
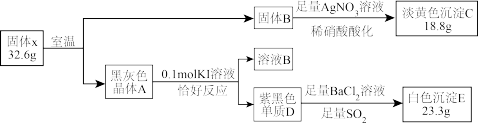
已知:固体B的化学成分与溶液B中溶质完全相同。
试根据以上内容回答下列问题:
(1)组成X的三种元素是____ 、_____ 、_____ ,X的化学式为_____ 。
(2)写出晶体A与KI反应的化学方程式:________ 。
(3)写出由紫黑色单质D生成白色沉淀E的离子方程式:_________ 。

已知:固体B的化学成分与溶液B中溶质完全相同。
试根据以上内容回答下列问题:
(1)组成X的三种元素是
(2)写出晶体A与KI反应的化学方程式:
(3)写出由紫黑色单质D生成白色沉淀E的离子方程式:
更新时间:2020-10-13 20:45:49
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
【推荐1】现有金属单质A、B和气体甲、乙、丙及物质C、D、E、F、G,它们之间能发生如图反应(图中某些反应的产物及条件没有全部标出)。
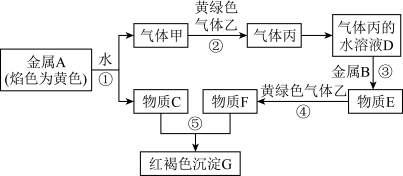
(1)丙的化学式为________ 。
(2)写出反应④的离子方程式:__________________ 。
(3)向E的溶液加入NaOH溶液并且充分搅拌,观察到的现象是___________ 。
(4)F溶液常用于腐蚀印刷电路板,请写出相关的离子方程式:______________ 。
(5)为鉴定B单质,将试样用稀盐酸溶解,取上层清液后需再加入的试剂是________ (填标号)。
a 碘水 b 氯水 c Na2SO3溶液 d KSCN溶液
(6)C溶液中加入过量Al2O3固体的离子方程式为_____________________ 。

(1)丙的化学式为
(2)写出反应④的离子方程式:
(3)向E的溶液加入NaOH溶液并且充分搅拌,观察到的现象是
(4)F溶液常用于腐蚀印刷电路板,请写出相关的离子方程式:
(5)为鉴定B单质,将试样用稀盐酸溶解,取上层清液后需再加入的试剂是
a 碘水 b 氯水 c Na2SO3溶液 d KSCN溶液
(6)C溶液中加入过量Al2O3固体的离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】已知有以下物质相互转化:
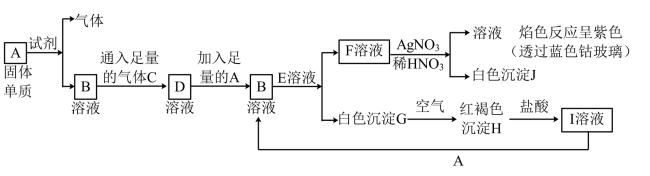
(1)A转化为B及气体这步反应中应加入的试剂是(填化学式)___________ ;
(2)写出B的化学式___ F的化学式____ ;
(3)写出由G转变成H的化学方程式___________________ ;
(4)写出检验I溶液中阳离子的试剂_____________ ;向I溶液中加入A的有关离子反应方程式是______ 。

(1)A转化为B及气体这步反应中应加入的试剂是(填化学式)
(2)写出B的化学式
(3)写出由G转变成H的化学方程式
(4)写出检验I溶液中阳离子的试剂
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】已知A、B、C为常见的单质,在一定条件下相互转化的关系如图:
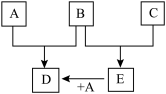
(1)若常温下,A、B均为气体,C为红色固体,E为黑色固体,则E的化学式为___________ ,写出A+E→D的化学反应方程式___________ 。
(2)若常温下B、C均为气体,A为金属单质,D为黑色晶体,则E的电子式为___________ ,写出A+E→D的化学反应方程式___________ 。
(3)若常温下B为气体,C为黑色固体,则构成金属A的原子结构示意图为___________ ,写出A+E→D的化学反应方程式___________ 。

(1)若常温下,A、B均为气体,C为红色固体,E为黑色固体,则E的化学式为
(2)若常温下B、C均为气体,A为金属单质,D为黑色晶体,则E的电子式为
(3)若常温下B为气体,C为黑色固体,则构成金属A的原子结构示意图为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】 (草酸亚铁)常用作分析试剂,受热分解后生成三种氧化物。某兴趣小组将
(草酸亚铁)常用作分析试剂,受热分解后生成三种氧化物。某兴趣小组将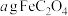 充分加热,得到
充分加热,得到 ,同时将生成的气体先缓慢通过足量的澄清石灰水,得到沉淀
,同时将生成的气体先缓慢通过足量的澄清石灰水,得到沉淀 ,逸出的气体其体积换算成标准状况为
,逸出的气体其体积换算成标准状况为 ,能使热的
,能使热的 变成红色。
变成红色。
(1) 受热分解产物除
受热分解产物除 外还有
外还有____________ 。
(2)
____________ 。
(3)为将生成的 完全溶解,需要
完全溶解,需要 的
的 溶液
溶液____________  。
。
(4)实验室由 的
的 溶液配制
溶液配制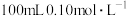 的
的 溶液,所需
溶液,所需 的
的 溶液的体积为
溶液的体积为____________  。配制所需的玻璃仪器除酸式滴定管(用于准确量取
。配制所需的玻璃仪器除酸式滴定管(用于准确量取 的
的 溶液)、烧杯、玻璃棒外还有
溶液)、烧杯、玻璃棒外还有____________ 。
(5)下列操作会使得(4)中所配 溶液物质的量浓度偏小的是
溶液物质的量浓度偏小的是____________ 。
A.量取 的
的 溶液时部分
溶液时部分 挥发
挥发
B.实验前容量瓶洗涤后,未干燥
C.转移溶液后,未洗涤烧杯和玻璃棒并将洗涤液转移到容量瓶中
D.定容时俯视刻度线
 (草酸亚铁)常用作分析试剂,受热分解后生成三种氧化物。某兴趣小组将
(草酸亚铁)常用作分析试剂,受热分解后生成三种氧化物。某兴趣小组将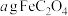 充分加热,得到
充分加热,得到 ,同时将生成的气体先缓慢通过足量的澄清石灰水,得到沉淀
,同时将生成的气体先缓慢通过足量的澄清石灰水,得到沉淀 ,逸出的气体其体积换算成标准状况为
,逸出的气体其体积换算成标准状况为 ,能使热的
,能使热的 变成红色。
变成红色。(1)
 受热分解产物除
受热分解产物除 外还有
外还有(2)

(3)为将生成的
 完全溶解,需要
完全溶解,需要 的
的 溶液
溶液 。
。(4)实验室由
 的
的 溶液配制
溶液配制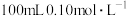 的
的 溶液,所需
溶液,所需 的
的 溶液的体积为
溶液的体积为 。配制所需的玻璃仪器除酸式滴定管(用于准确量取
。配制所需的玻璃仪器除酸式滴定管(用于准确量取 的
的 溶液)、烧杯、玻璃棒外还有
溶液)、烧杯、玻璃棒外还有(5)下列操作会使得(4)中所配
 溶液物质的量浓度偏小的是
溶液物质的量浓度偏小的是A.量取
 的
的 溶液时部分
溶液时部分 挥发
挥发B.实验前容量瓶洗涤后,未干燥
C.转移溶液后,未洗涤烧杯和玻璃棒并将洗涤液转移到容量瓶中
D.定容时俯视刻度线
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】为测定出Na2CO3和NaHCO3的混合物中Na2CO3质量分数,请你完善下列方案。
方案一:称取一定质量样品,置于坩埚中高温加热至恒重后冷却,称量剩余固体质量,进行计算。
(1)发生反应的化学方程式为:_______
(2)实验中需加热至恒重的目的是:_______
方案二:按如图所示装置进行实验
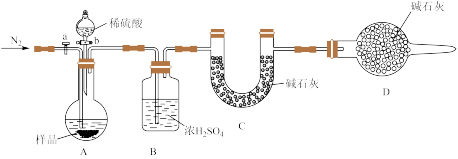
(3)B装置的作用是_______
(4)反应完毕后还要通一段时间N2的目的是_______
(5)实验前称取混合物样品19.00 g,实验后测得C装置增重8.80 g,则样品中碳酸钠的质量分数为_______ %(保留小数点后两位)。
方案一:称取一定质量样品,置于坩埚中高温加热至恒重后冷却,称量剩余固体质量,进行计算。
(1)发生反应的化学方程式为:
(2)实验中需加热至恒重的目的是:
方案二:按如图所示装置进行实验

(3)B装置的作用是
(4)反应完毕后还要通一段时间N2的目的是
(5)实验前称取混合物样品19.00 g,实验后测得C装置增重8.80 g,则样品中碳酸钠的质量分数为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】氮化铝(AlN)是一种新型非金属材料,室温下能缓慢与水反应,可由铝粉在氮气氛围中于1700℃合成,产物为白色到灰蓝色粉末。某探究小组在实验室制备AlN并测定产品纯度,设计实验如下。请回答下列问题:
(一)制备AlN
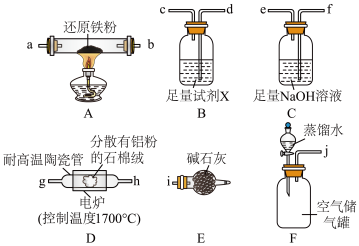
(1)按气流由左向右的方向,上述装置的正确连接顺序为:F→_________ →E。
(2)以空气为原料制备AlN,装置A中还原铁粉的作用为_________ ,装置B中试剂X为_________ 。
(二)测定产品纯度
取mg产品,用以下装置测定产品纯度(夹持装置已略去)。已知:AlN+NaOH+H2O=NaAlO2+NH3↑
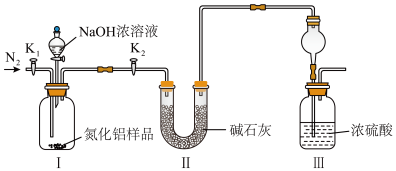
(3)实验步骤如下:在装置中加入实验药品,关闭_________ (填K1或K2,下同)打开_________ ,打开分液漏斗活塞加入NaOH浓溶液至不再产生气体。然后打开_________ ,通入氮气一段时间,目的是_________ ,测得装置Ⅲ增重ng。
(4)根据以上数据计算,该产品的纯度为_________ (用含m、n的代数式表示)。
(5)有人认为上述实验的设计仍然存在缺陷,可能会导致测定结果偏高,原因是:_________ 。
(一)制备AlN

(1)按气流由左向右的方向,上述装置的正确连接顺序为:F→
(2)以空气为原料制备AlN,装置A中还原铁粉的作用为
(二)测定产品纯度
取mg产品,用以下装置测定产品纯度(夹持装置已略去)。已知:AlN+NaOH+H2O=NaAlO2+NH3↑

(3)实验步骤如下:在装置中加入实验药品,关闭
(4)根据以上数据计算,该产品的纯度为
(5)有人认为上述实验的设计仍然存在缺陷,可能会导致测定结果偏高,原因是:
您最近一年使用:0次



