阅读下面科普信息,回答问题:
一个体重50 kg的健康人含铁2 g,这2 g铁在人体中以Fe2+和Fe3+的形式存在。亚铁离子易被吸收,给贫血者补充铁时,应给予含亚铁离子的亚铁盐,如硫酸亚铁。服用维生素C,可使食物中的铁离子还原成亚铁离子,有利于铁的吸收。
(1)以下为常见的铁元素的几种微粒,其中既有氧化性又有还原性的是____
A.Fe B.Fe2+ C.Fe3+
(2)工业盐的主要成分是NaNO2,曾多次发生过因误食NaNO2而中毒的事件,其原因是NaNO2把人体内的Fe2+转化为Fe3+而失去与O2结合的能力,这说明NaNO2具有____ 性。下列不能实现上述转化的物质是____
A.Cl2 B.O2 C.FeCl3 D.KMnO4(H+)
(3)工业盐中毒后,可服用维生素C来缓解中毒状况,这说明维生素C具有____ 性。
(4)在Fe+4HNO3(稀)=Fe(NO3)3+NO↑+2H2O的反应中,HNO3表现了____ 和____ 性。
一个体重50 kg的健康人含铁2 g,这2 g铁在人体中以Fe2+和Fe3+的形式存在。亚铁离子易被吸收,给贫血者补充铁时,应给予含亚铁离子的亚铁盐,如硫酸亚铁。服用维生素C,可使食物中的铁离子还原成亚铁离子,有利于铁的吸收。
(1)以下为常见的铁元素的几种微粒,其中既有氧化性又有还原性的是
A.Fe B.Fe2+ C.Fe3+
(2)工业盐的主要成分是NaNO2,曾多次发生过因误食NaNO2而中毒的事件,其原因是NaNO2把人体内的Fe2+转化为Fe3+而失去与O2结合的能力,这说明NaNO2具有
A.Cl2 B.O2 C.FeCl3 D.KMnO4(H+)
(3)工业盐中毒后,可服用维生素C来缓解中毒状况,这说明维生素C具有
(4)在Fe+4HNO3(稀)=Fe(NO3)3+NO↑+2H2O的反应中,HNO3表现了
更新时间:2020-10-18 11:22:42
|
相似题推荐
解答题-工业流程题
|
较易
(0.85)
名校
解题方法
【推荐1】硼镁泥是一种工业废料,主要成分是MgO(占40%),还有CaO、MnO、Fe2O3、FeO、Al2O3等杂质,以此为原料制取的硫酸镁可用于印染、造纸、医药等工业。从硼镁泥中提取MgSO4·7H2O的流程如下:
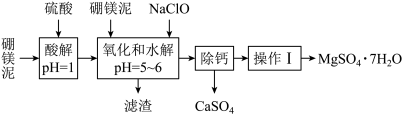
根据题意回答下列问题:
(1)实验中需用1 mol·L-1的硫酸900 mL,配制时所用的玻璃仪器除了烧杯、玻璃棒、量筒外,还需________________ 。
(2)加入的NaClO可将Mn2+氧化为MnO2 ,反应中无气体产生,反应的离子方程式为:________________ 。还有一种离子也会被NaClO氧化,反应的离子方程式为_______________________ 。
(3)在“除钙”前,需检验滤液中Fe3+是否被除尽,简述检验方法:___________________ 。
(4)已知MgSO4、CaSO4的溶解度如下表:
“除钙”是将MgSO4和CaSO4的混合溶液中的CaSO4除去,根据上表数据,可确定操作步骤为蒸发结晶、_______________________ (填操作名称)。

根据题意回答下列问题:
(1)实验中需用1 mol·L-1的硫酸900 mL,配制时所用的玻璃仪器除了烧杯、玻璃棒、量筒外,还需
(2)加入的NaClO可将Mn2+氧化为MnO2 ,反应中无气体产生,反应的离子方程式为:
(3)在“除钙”前,需检验滤液中Fe3+是否被除尽,简述检验方法:
(4)已知MgSO4、CaSO4的溶解度如下表:
温度/℃ | 40 | 50 | 60 | 70 |
S(MgSO4)/g | 30.9 | 33.4 | 35.6 | 36.9 |
S(CaSO4)/g | 0.210 | 0.207 | 0.201 | 0.193 |
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
【推荐2】研究氮的循环和转化对生产、生活有重要价值。
Ⅰ.氮是重要的化工原料。某工厂用氨制硝酸和铵盐的流程如图所示:
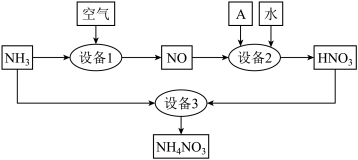
设备2中通入的物质A是___________ 。设备2、3中发生反应的化学方程式分别是___________ 、___________ ;
Ⅱ.氨氮废水的处理是当前科学研究的热点问题之一、氨氮废水中氮元素多以 和NH3·H2O的形式存在。某工厂处理氨氮废水的流程如下:
和NH3·H2O的形式存在。某工厂处理氨氮废水的流程如下:

(1)过程①的目的是将 转化成NH3,并通过鼓入大量热空气将氨吹出,写出
转化成NH3,并通过鼓入大量热空气将氨吹出,写出 转化成NH3的离子方程式:
转化成NH3的离子方程式:___________ 。
(2)过程②中加入NaClO溶液可将氨氮化合物转化为无毒物质,反应后含氮元素、氯元素的物质的化学式分别为___________ 、___________ 。
(3)图中含余氯废水中含有NaClO,则X可选用___________ (填序号)溶液达到去除余氯的目的。
a.KOH b.Na2SO3 c.KMnO4 d.NaCl
Ⅰ.氮是重要的化工原料。某工厂用氨制硝酸和铵盐的流程如图所示:

设备2中通入的物质A是
Ⅱ.氨氮废水的处理是当前科学研究的热点问题之一、氨氮废水中氮元素多以
 和NH3·H2O的形式存在。某工厂处理氨氮废水的流程如下:
和NH3·H2O的形式存在。某工厂处理氨氮废水的流程如下:
(1)过程①的目的是将
 转化成NH3,并通过鼓入大量热空气将氨吹出,写出
转化成NH3,并通过鼓入大量热空气将氨吹出,写出 转化成NH3的离子方程式:
转化成NH3的离子方程式:(2)过程②中加入NaClO溶液可将氨氮化合物转化为无毒物质,反应后含氮元素、氯元素的物质的化学式分别为
(3)图中含余氯废水中含有NaClO,则X可选用
a.KOH b.Na2SO3 c.KMnO4 d.NaCl
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐3】叠氮化钠(NaN3)是一种易溶于水的白色晶体,微溶于乙醇,不溶于乙醚,可用于合成抗生素头孢菌素药物的中间体、汽车安全气囊的药剂等。氨基钠(NaNH2)的熔点为210℃,沸点为400℃,在水溶液中易水解。实验室制取叠氮化钠的实验步骤及实验装置如下:
①打开止水夹K1,关闭止水夹K2,加热装置D一段时间;
②加热装置A中的金属钠,使其熔化并充分反应后,再停止加热装置D并关闭K1;
③向装置A中b容器内充入加热介质并加热到210~220℃,打开止水夹K2,通入N2O;
④冷却,向产物中加入乙醇,减压浓缩结晶后,再过滤,并用乙醚洗涤,晾干。
回答下列问题:
(1)装置B中盛放的药品为___________ ;装置C的主要作用是___________ 。
(2)氨气与熔化的钠反应生成NaNH2的化学方程式为___________ 。
(3)步骤③中,为了使反应受热均匀,A装置里a容器的加热方式为___________ ;生成NaN3的化学方程式为___________ ;N2O可由 在240~245℃分解制得(硝酸铵的熔点为169.6℃),则不能选择的气体发生装置是
在240~245℃分解制得(硝酸铵的熔点为169.6℃),则不能选择的气体发生装置是___________ (填序号)。

(4)图中仪器a用的是铁质而不用玻璃,其主要原因是___________ 。步骤④中用乙醚洗涤的主要目是___________ 。
(5)实验室用滴定法测定叠氮化钠样品中NaN3的质量分数:①将2.500g试样配成500.00mL溶液。②取50.00mL溶液置于锥形瓶中,加入50.00mL 0.1010 mol∙L−1 (NH4)2Ce(NO3)6溶液。③充分反应后,将溶液稍稀释,向溶液中加入8mL浓硫酸,滴入3滴邻菲啰啉指示液,用0.00500 mol∙L−1 (NH4)2Fe(SO4)2标准溶液滴定过量的Ce4+消耗溶液体积为29.00mL。测定过程的反应方程式为:______ ,则试样中的质量分数为___________ 。
①打开止水夹K1,关闭止水夹K2,加热装置D一段时间;
②加热装置A中的金属钠,使其熔化并充分反应后,再停止加热装置D并关闭K1;
③向装置A中b容器内充入加热介质并加热到210~220℃,打开止水夹K2,通入N2O;
④冷却,向产物中加入乙醇,减压浓缩结晶后,再过滤,并用乙醚洗涤,晾干。

回答下列问题:
(1)装置B中盛放的药品为
(2)氨气与熔化的钠反应生成NaNH2的化学方程式为
(3)步骤③中,为了使反应受热均匀,A装置里a容器的加热方式为
 在240~245℃分解制得(硝酸铵的熔点为169.6℃),则不能选择的气体发生装置是
在240~245℃分解制得(硝酸铵的熔点为169.6℃),则不能选择的气体发生装置是
(4)图中仪器a用的是铁质而不用玻璃,其主要原因是
(5)实验室用滴定法测定叠氮化钠样品中NaN3的质量分数:①将2.500g试样配成500.00mL溶液。②取50.00mL溶液置于锥形瓶中,加入50.00mL 0.1010 mol∙L−1 (NH4)2Ce(NO3)6溶液。③充分反应后,将溶液稍稀释,向溶液中加入8mL浓硫酸,滴入3滴邻菲啰啉指示液,用0.00500 mol∙L−1 (NH4)2Fe(SO4)2标准溶液滴定过量的Ce4+消耗溶液体积为29.00mL。测定过程的反应方程式为:
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐1】化学物质丰富多彩,化学反应千变万化,而常见物质之间的反应往往“隐藏着某些反应机理”。学校化学兴趣小组对过氧化钠参与的某些反应进行了初步探究。
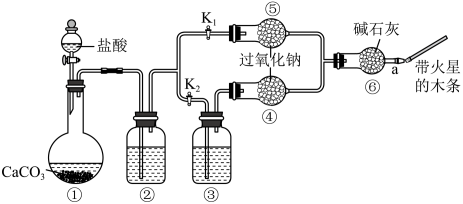
Ⅰ:甲组设计如图实验装置,验证“二氧化碳与水接触时才能和过氧化钠反应”。
步骤1:打开弹簧夹 。关闭
。关闭 ,打开分液漏斗活塞加入盐酸,将带火星的木条放在a处。
,打开分液漏斗活塞加入盐酸,将带火星的木条放在a处。
步骤2:打开弹簧夹 ,关闭
,关闭 ,打开分液漏斗活塞加入盐酸,将带火星的木条放在a处。
,打开分液漏斗活塞加入盐酸,将带火星的木条放在a处。
请回答下列问题:
(1)写出过氧化钠与二氧化碳反应的化学方程式___________ 。
(2)装置②中盛放的饱和 溶液作用
溶液作用___________ 。
(3)本实验预期现象是___________ 。
Ⅱ.乙组探究过氧化钠与亚铁盐的反应
步骤:向少量 溶液中加入足量
溶液中加入足量 ,观察到有沉淀产生。将沉淀过滤,用蒸馏水充分洗净沉淀后,加入盐酸至沉淀完全溶解,得到溶液A,再将溶液A加热蒸干并充分灼烧,得到固体B。
,观察到有沉淀产生。将沉淀过滤,用蒸馏水充分洗净沉淀后,加入盐酸至沉淀完全溶解,得到溶液A,再将溶液A加热蒸干并充分灼烧,得到固体B。
(4)写出检验A中金属阳离子的反应原理___________ (写离子方程式)。
(5)固体B的化学式为___________ 。

Ⅰ:甲组设计如图实验装置,验证“二氧化碳与水接触时才能和过氧化钠反应”。
步骤1:打开弹簧夹
 。关闭
。关闭 ,打开分液漏斗活塞加入盐酸,将带火星的木条放在a处。
,打开分液漏斗活塞加入盐酸,将带火星的木条放在a处。步骤2:打开弹簧夹
 ,关闭
,关闭 ,打开分液漏斗活塞加入盐酸,将带火星的木条放在a处。
,打开分液漏斗活塞加入盐酸,将带火星的木条放在a处。请回答下列问题:
(1)写出过氧化钠与二氧化碳反应的化学方程式
(2)装置②中盛放的饱和
 溶液作用
溶液作用(3)本实验预期现象是
Ⅱ.乙组探究过氧化钠与亚铁盐的反应
步骤:向少量
 溶液中加入足量
溶液中加入足量 ,观察到有沉淀产生。将沉淀过滤,用蒸馏水充分洗净沉淀后,加入盐酸至沉淀完全溶解,得到溶液A,再将溶液A加热蒸干并充分灼烧,得到固体B。
,观察到有沉淀产生。将沉淀过滤,用蒸馏水充分洗净沉淀后,加入盐酸至沉淀完全溶解,得到溶液A,再将溶液A加热蒸干并充分灼烧,得到固体B。(4)写出检验A中金属阳离子的反应原理
(5)固体B的化学式为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐2】化学实验小组在实验室进行含铁元素物质的实验,请回答下列问题:
(1)研究 价铁与
价铁与 价铁的转化,实验操作如图:
价铁的转化,实验操作如图:

①检验试管甲的溶液中含有 的实验方案为:取少量甲中溶液于试管中,
的实验方案为:取少量甲中溶液于试管中,________________ (叙述操作并描述现象),说明其中含有 。
。
②向试管甲中加入过量铁粉,发生反应的离子方程式为___________________ 。
③试管乙中的实验现象是_____________________ 。
④试管丙中产生白色沉淀,一段时间后部分沉淀变为红褐色,写出白色沉淀变为红褐色的化学方程式__________________________ 。
(2) 溶液在空气中易变质,利用部分变质的
溶液在空气中易变质,利用部分变质的 溶液制备
溶液制备 ,实验流程图如下.已知化合物X的焰色试验为紫色,请在“ ”内填写X和其它必要试剂的化学式或反应条件,在“☐”内填写含铁元素物质的化学式.
,实验流程图如下.已知化合物X的焰色试验为紫色,请在“ ”内填写X和其它必要试剂的化学式或反应条件,在“☐”内填写含铁元素物质的化学式.________

(3)测定某混合物中氧化铁的含量.
现有钢和氧化铁的混合物粉末共 ,将其加入到
,将其加入到 的稀硫酸溶液中,充分反应后,剩余固体的质量为
的稀硫酸溶液中,充分反应后,剩余固体的质量为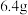 .则原混合物中氧化铁的质量分数为
.则原混合物中氧化铁的质量分数为________ %(保留小数点后一位)。
(1)研究
 价铁与
价铁与 价铁的转化,实验操作如图:
价铁的转化,实验操作如图:
①检验试管甲的溶液中含有
 的实验方案为:取少量甲中溶液于试管中,
的实验方案为:取少量甲中溶液于试管中, 。
。②向试管甲中加入过量铁粉,发生反应的离子方程式为
③试管乙中的实验现象是
④试管丙中产生白色沉淀,一段时间后部分沉淀变为红褐色,写出白色沉淀变为红褐色的化学方程式
(2)
 溶液在空气中易变质,利用部分变质的
溶液在空气中易变质,利用部分变质的 溶液制备
溶液制备 ,实验流程图如下.已知化合物X的焰色试验为紫色,请在“ ”内填写X和其它必要试剂的化学式或反应条件,在“☐”内填写含铁元素物质的化学式.
,实验流程图如下.已知化合物X的焰色试验为紫色,请在“ ”内填写X和其它必要试剂的化学式或反应条件,在“☐”内填写含铁元素物质的化学式.
(3)测定某混合物中氧化铁的含量.
现有钢和氧化铁的混合物粉末共
 ,将其加入到
,将其加入到 的稀硫酸溶液中,充分反应后,剩余固体的质量为
的稀硫酸溶液中,充分反应后,剩余固体的质量为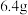 .则原混合物中氧化铁的质量分数为
.则原混合物中氧化铁的质量分数为
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
【推荐3】铁是人类较早使用的金属之一、运用所学知识,回答下列问题。
(1)鉴别 胶体和
胶体和 溶液的方法是
溶液的方法是___________ 。
(2)不仅溶液中 易被氧化成
易被氧化成 ,溶液中白色沉淀
,溶液中白色沉淀 更易被
更易被 氧化,请写出反应的化学方程式
氧化,请写出反应的化学方程式___________ ,现象为___________ 。
(3)绿矾( )是治疗缺铁性贫血药品的主要成分,也是中学化学一种常见的化学试剂。亚铁盐在空气中容易被氧化而变质。
)是治疗缺铁性贫血药品的主要成分,也是中学化学一种常见的化学试剂。亚铁盐在空气中容易被氧化而变质。
①甲同学取2mL稀硫酸酸化 溶液,加入几滴双氧水后,再加入1滴KSCN溶液,溶液变红,说明
溶液,加入几滴双氧水后,再加入1滴KSCN溶液,溶液变红,说明 可将
可将 氧化。
氧化。 溶液与双氧水反应的离子方程式为
溶液与双氧水反应的离子方程式为___________ 。
②乙同学认为甲同学的实验不够严谨,该组同学在2mL用稀 酸化的
酸化的 溶液中先加入0.5mL煤油,再于液面下依次加入几滴双氧水和1滴KSCN溶液,溶液变红,煤油的作用是
溶液中先加入0.5mL煤油,再于液面下依次加入几滴双氧水和1滴KSCN溶液,溶液变红,煤油的作用是___________ 。
(4)电子工业用 溶液腐蚀敷在绝缘板上的铜,制造印刷电路板。工程师欲从制造印刷电路板的废水中回收铜,并获得
溶液腐蚀敷在绝缘板上的铜,制造印刷电路板。工程师欲从制造印刷电路板的废水中回收铜,并获得 溶液,设计如下方案:
溶液,设计如下方案:

①滤渣C的化学式为___________ 。
②加过量D发生反应的离子方程式为___________ 。
③通入F发生反应的化学方程式为___________ 。
(1)鉴别
 胶体和
胶体和 溶液的方法是
溶液的方法是(2)不仅溶液中
 易被氧化成
易被氧化成 ,溶液中白色沉淀
,溶液中白色沉淀 更易被
更易被 氧化,请写出反应的化学方程式
氧化,请写出反应的化学方程式(3)绿矾(
 )是治疗缺铁性贫血药品的主要成分,也是中学化学一种常见的化学试剂。亚铁盐在空气中容易被氧化而变质。
)是治疗缺铁性贫血药品的主要成分,也是中学化学一种常见的化学试剂。亚铁盐在空气中容易被氧化而变质。①甲同学取2mL稀硫酸酸化
 溶液,加入几滴双氧水后,再加入1滴KSCN溶液,溶液变红,说明
溶液,加入几滴双氧水后,再加入1滴KSCN溶液,溶液变红,说明 可将
可将 氧化。
氧化。 溶液与双氧水反应的离子方程式为
溶液与双氧水反应的离子方程式为②乙同学认为甲同学的实验不够严谨,该组同学在2mL用稀
 酸化的
酸化的 溶液中先加入0.5mL煤油,再于液面下依次加入几滴双氧水和1滴KSCN溶液,溶液变红,煤油的作用是
溶液中先加入0.5mL煤油,再于液面下依次加入几滴双氧水和1滴KSCN溶液,溶液变红,煤油的作用是(4)电子工业用
 溶液腐蚀敷在绝缘板上的铜,制造印刷电路板。工程师欲从制造印刷电路板的废水中回收铜,并获得
溶液腐蚀敷在绝缘板上的铜,制造印刷电路板。工程师欲从制造印刷电路板的废水中回收铜,并获得 溶液,设计如下方案:
溶液,设计如下方案:
①滤渣C的化学式为
②加过量D发生反应的离子方程式为
③通入F发生反应的化学方程式为
您最近一年使用:0次



