Ⅰ.实验室常规检查发现标签模糊不清的两瓶试剂,只知道分别是淀粉溶液和氯化钠溶液,试用两种方法进行鉴别。
(1)___________ 。
(2)___________ 。
Ⅱ.铜器久置于空气中会和空气中的水蒸气、CO2、O2作用产生“绿锈”,“绿锈”俗称“铜绿”,又称“孔雀石”化学式为Cu2(OH)2CO3。
(3)“铜绿”的化学名称是___________ 。
(4)写出“铜绿”发生的一个氧化还原反应的化学方程___________ 。
(5)写出“铜绿”发生的一个非氧化还原反应的离子方程式___________ 。
Ⅲ.将铜和一定浓度的稀硫酸混合后在加热的情况下通入氧气,发生如下反应:2Cu+2H2SO4+O2 2CuSO4+2H2O。制得的硫酸铜溶液经过蒸发、浓缩、冷却结晶、过滤可得到胆矾。
2CuSO4+2H2O。制得的硫酸铜溶液经过蒸发、浓缩、冷却结晶、过滤可得到胆矾。
(6)请分析反应2Cu+2H2SO4+O2 2CuSO4+2H2O中,氧化剂是
2CuSO4+2H2O中,氧化剂是___________ (填化学式,下同),被氧化的物质是___________ 。
(1)
(2)
Ⅱ.铜器久置于空气中会和空气中的水蒸气、CO2、O2作用产生“绿锈”,“绿锈”俗称“铜绿”,又称“孔雀石”化学式为Cu2(OH)2CO3。
(3)“铜绿”的化学名称是
(4)写出“铜绿”发生的一个氧化还原反应的化学方程
(5)写出“铜绿”发生的一个非氧化还原反应的离子方程式
Ⅲ.将铜和一定浓度的稀硫酸混合后在加热的情况下通入氧气,发生如下反应:2Cu+2H2SO4+O2
 2CuSO4+2H2O。制得的硫酸铜溶液经过蒸发、浓缩、冷却结晶、过滤可得到胆矾。
2CuSO4+2H2O。制得的硫酸铜溶液经过蒸发、浓缩、冷却结晶、过滤可得到胆矾。(6)请分析反应2Cu+2H2SO4+O2
 2CuSO4+2H2O中,氧化剂是
2CuSO4+2H2O中,氧化剂是
更新时间:2020-10-19 14:02:44
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】回答下列问题。
I .今有 10 种物质:①Na ②盐酸 ③纯醋酸 ④NH3 ⑤空气 ⑥CO2⑦Fe(OH)3胶体 ⑧NaCl晶体 ⑨BaCO3 ⑩碘酒
(1)能导电的物质___________ 。(用序号填空 ,下同)
(2)电解质,但熔融状态下并不导电___________ 。
(3)强电解质___________ 。
(4)非电解质___________ 。
Ⅱ.请回答:
(5)区分Fe(OH)3胶体和FeCl3溶液实验方法是___________ 。
(6)配平该离子方程式并用双线桥表示电子转移:___________
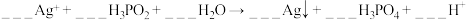
(7)H3PO2是一元弱酸,写出其与足量NaOH 溶液反应的离子方程式:___________ 。
I .今有 10 种物质:①Na ②盐酸 ③纯醋酸 ④NH3 ⑤空气 ⑥CO2⑦Fe(OH)3胶体 ⑧NaCl晶体 ⑨BaCO3 ⑩碘酒
(1)能导电的物质
(2)电解质,但熔融状态下并不导电
(3)强电解质
(4)非电解质
Ⅱ.请回答:
(5)区分Fe(OH)3胶体和FeCl3溶液实验方法是
(6)配平该离子方程式并用双线桥表示电子转移:
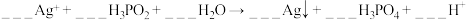
(7)H3PO2是一元弱酸,写出其与足量NaOH 溶液反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】FeCl3是中学实验室常用的试剂,可以用来制备氢氧化铁胶体。
(1)下列制备氢氧化铁胶体的操作方法正确的是____________ (填字母);
a.向饱和氯化铁溶液中滴加少量的氢氧化钠稀溶液
b.加热煮沸氯化铁饱和溶液
c. 氨水中滴加氯化铁浓溶液
氨水中滴加氯化铁浓溶液
d.在沸水中滴加饱和氯化铁溶液,煮沸至液体呈红褐色
(2)写出制备氢氧化铁胶体的离子方程式__________________________ ;
(3)下列与胶体性质无关的是_____________ (填字母);
a.河流入海口处形成沙洲
b.使用微波手术刀进行外科手术,可使开刀处的血液迅速凝固而减少失血
c.肾功能衰竭等疾病引起的血液中毒,可利用血液透析进行治疗
d.在饱和氯化铁溶液中滴加NaOH溶液,产生红褐色沉淀
e.冶金厂常用高压电除去烟尘
(4)从溶液中分离提纯Fe(OH)3胶体的方法叫_____________ 。
(1)下列制备氢氧化铁胶体的操作方法正确的是
a.向饱和氯化铁溶液中滴加少量的氢氧化钠稀溶液
b.加热煮沸氯化铁饱和溶液
c.
 氨水中滴加氯化铁浓溶液
氨水中滴加氯化铁浓溶液d.在沸水中滴加饱和氯化铁溶液,煮沸至液体呈红褐色
(2)写出制备氢氧化铁胶体的离子方程式
(3)下列与胶体性质无关的是
a.河流入海口处形成沙洲
b.使用微波手术刀进行外科手术,可使开刀处的血液迅速凝固而减少失血
c.肾功能衰竭等疾病引起的血液中毒,可利用血液透析进行治疗
d.在饱和氯化铁溶液中滴加NaOH溶液,产生红褐色沉淀
e.冶金厂常用高压电除去烟尘
(4)从溶液中分离提纯Fe(OH)3胶体的方法叫
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】对于数以千万计的化学物质和为数众多的化学反应,分类法的作用几乎是无可代替的。
I.现有物质:①H2O ②Cu ③BaCO3 ④Fe(OH)3胶体 ⑤酒精 ⑥CO2 ⑦稀硫酸
(1)以上物质中属于混合物的是_______ (填序号,下同),属于电解质的是_______ 。
(2)向④中逐滴滴加⑦,可观察到的现象是_______ 。
II.某白色粉末中可能含有 、
、 、
、 ,现进行以下实验:
,现进行以下实验:
i.将部分粉末加入水中,振荡,有白色沉淀生成;
ii.向i的悬浊液中加入过量稀硝酸,白色沉淀消失,并有气泡产生;
iii.取少量ii的溶液滴入 溶液,有白色沉淀生成。
溶液,有白色沉淀生成。
(3)根据上述实验现象,判断原白色粉末中肯定含有_______ ,可能含有_______ ,并写出有关反应的离子方程式_______ 。(写两个即可)
I.现有物质:①H2O ②Cu ③BaCO3 ④Fe(OH)3胶体 ⑤酒精 ⑥CO2 ⑦稀硫酸
(1)以上物质中属于混合物的是
(2)向④中逐滴滴加⑦,可观察到的现象是
II.某白色粉末中可能含有
 、
、 、
、 ,现进行以下实验:
,现进行以下实验:i.将部分粉末加入水中,振荡,有白色沉淀生成;
ii.向i的悬浊液中加入过量稀硝酸,白色沉淀消失,并有气泡产生;
iii.取少量ii的溶液滴入
 溶液,有白色沉淀生成。
溶液,有白色沉淀生成。(3)根据上述实验现象,判断原白色粉末中肯定含有
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】根据有关铁及其化合物的性质,回答下列问题:
(1)电子工业常用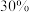 的
的 溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板,写出该反应的离子方程式:
溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板,写出该反应的离子方程式:_______ 。
(2)工业盐的主要成分是 ,以前有许多起因误食
,以前有许多起因误食 而中毒的事件,其原因是
而中毒的事件,其原因是 把人体内的
把人体内的 转化为
转化为 而失去与
而失去与 结合的能力,这说明
结合的能力,这说明 具有
具有_______ (填“氧化”或“还原”)性。下列也能实现这种转化的物质是_______ (填字母序号)。
A. B.
B. C.
C. 溶液 D.酸性
溶液 D.酸性 溶液
溶液
工业盐中毒后,可服用维生素C来缓解中毒状况,这说明维生素C具有_______ (填“氧化”或“还原”)性。
(3)在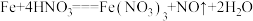 的反应中,每有
的反应中,每有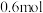 电子发生转移时,被还原的
电子发生转移时,被还原的 为
为_______  。
。
(4)某容器中发生一个化学反应,反应过程中存在 、
、 、
、 、
、 、
、 和
和 六种粒子,在反应过程中测得
六种粒子,在反应过程中测得 、
、 的物质的量随时间变化的曲线如图所示,该反应的离子方程式为
的物质的量随时间变化的曲线如图所示,该反应的离子方程式为_______ 。

(1)电子工业常用
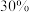 的
的 溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板,写出该反应的离子方程式:
溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板,写出该反应的离子方程式:(2)工业盐的主要成分是
 ,以前有许多起因误食
,以前有许多起因误食 而中毒的事件,其原因是
而中毒的事件,其原因是 把人体内的
把人体内的 转化为
转化为 而失去与
而失去与 结合的能力,这说明
结合的能力,这说明 具有
具有A.
 B.
B. C.
C. 溶液 D.酸性
溶液 D.酸性 溶液
溶液工业盐中毒后,可服用维生素C来缓解中毒状况,这说明维生素C具有
(3)在
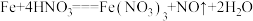 的反应中,每有
的反应中,每有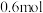 电子发生转移时,被还原的
电子发生转移时,被还原的 为
为 。
。(4)某容器中发生一个化学反应,反应过程中存在
 、
、 、
、 、
、 、
、 和
和 六种粒子,在反应过程中测得
六种粒子,在反应过程中测得 、
、 的物质的量随时间变化的曲线如图所示,该反应的离子方程式为
的物质的量随时间变化的曲线如图所示,该反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】钠和铝是两种重要的金属。请回答下列问题:
(1)一小块金属钠长时间放置在空气中,可能有下列现象,这些现象出现的先后顺序是______________________ (填序号);
①变成白色粉末 ②变暗 ③变成白色固体 ④变成液体
若金属钠长时间在潮湿的空气中放置,最后生成的物质是_________ (填名称)。
(2)将一小块金属钠投入水中,观察到的实验现象是________ (填序号),发生反应的离子方程式为:__________________ 。
A.钠沉到水底 B.钠熔成小球 C.小球四处游动
(3)铝与稀硝酸反应的化学方程式为:Al+4HNO3=Al(NO3)3+NO↑+2H2O,该反应的氧化剂是_______ (填化学式),还原剂与氧化剂的物质的量之比是________ ,当有5.4gAl发生反应时,转移的电子数为________ 。
(1)一小块金属钠长时间放置在空气中,可能有下列现象,这些现象出现的先后顺序是
①变成白色粉末 ②变暗 ③变成白色固体 ④变成液体
若金属钠长时间在潮湿的空气中放置,最后生成的物质是
(2)将一小块金属钠投入水中,观察到的实验现象是
A.钠沉到水底 B.钠熔成小球 C.小球四处游动
(3)铝与稀硝酸反应的化学方程式为:Al+4HNO3=Al(NO3)3+NO↑+2H2O,该反应的氧化剂是
您最近一年使用:0次
【推荐3】按要求填空:
(1)在S2-、Fe2+、Mg2+、S、I- 、H+ 中,既有氧化性又有还原性的是___________ 。
(2)某同学写出以下三个化学方程式(未配平):
①NO +HNO3 →N2O3+ H2O;②NH3 +NO→HNO2+ H2O;③N2O4 +H2O→HNO3 + HNO2
其中你认为一定不可能实现的是___________ 。
(3)用双线桥标出方程式6HCl+KClO3=KCl+3Cl2↑+3H2O 中电子转移的方向和数目___________ ,该反应中若生成 426g Cl2,则被氧化的HCl的有多少___________ g。
(4)As2O3、Zn、AsH3 (气态)、ZnSO4、H2SO4、H2O组成的一个氧化还原反应体系中,已知As2O3作氧化剂, ZnSO4 作氧化产物。该反应的化学反应方程式为:___________ 。
(5)已知氧化性:Cl2 > Br2 > Fe3+ > I2,写出下列离子方程式:
a.少量氯气与FeI2溶液反应:___________ 。
b.氯气与FeBr2溶液以按个数比 1∶1 反应:___________ 。
(6)新型纳米材料氧缺位铁酸盐(MFe2Ox,3 < x < 4,M=Mn,Zn,Ni且均为+2 价,下同)是由铁酸盐 MFe2O4 经过高温反应得到的。将纳米材料氧缺位铁酸盐分散在蒸馏水中,所形成的分散系属于___________ ,铁酸盐MFe2O4经过高温反应得到 MFe2Ox的反应属于___________ (填“氧化还原”或“非氧化还原”)反应。
(7)在酸性条件下。 容易转化为 Fe2+,某反应体系中共存在下列 6 种粒子,
容易转化为 Fe2+,某反应体系中共存在下列 6 种粒子, 、Fe2+、H+、H2O、Cu2O、Cu2+,则该反应中的还原剂是
、Fe2+、H+、H2O、Cu2O、Cu2+,则该反应中的还原剂是___________ 。
(1)在S2-、Fe2+、Mg2+、S、I- 、H+ 中,既有氧化性又有还原性的是
(2)某同学写出以下三个化学方程式(未配平):
①NO +HNO3 →N2O3+ H2O;②NH3 +NO→HNO2+ H2O;③N2O4 +H2O→HNO3 + HNO2
其中你认为一定不可能实现的是
(3)用双线桥标出方程式6HCl+KClO3=KCl+3Cl2↑+3H2O 中电子转移的方向和数目
(4)As2O3、Zn、AsH3 (气态)、ZnSO4、H2SO4、H2O组成的一个氧化还原反应体系中,已知As2O3作氧化剂, ZnSO4 作氧化产物。该反应的化学反应方程式为:
(5)已知氧化性:Cl2 > Br2 > Fe3+ > I2,写出下列离子方程式:
a.少量氯气与FeI2溶液反应:
b.氯气与FeBr2溶液以按个数比 1∶1 反应:
(6)新型纳米材料氧缺位铁酸盐(MFe2Ox,3 < x < 4,M=Mn,Zn,Ni且均为+2 价,下同)是由铁酸盐 MFe2O4 经过高温反应得到的。将纳米材料氧缺位铁酸盐分散在蒸馏水中,所形成的分散系属于
(7)在酸性条件下。
 容易转化为 Fe2+,某反应体系中共存在下列 6 种粒子,
容易转化为 Fe2+,某反应体系中共存在下列 6 种粒子, 、Fe2+、H+、H2O、Cu2O、Cu2+,则该反应中的还原剂是
、Fe2+、H+、H2O、Cu2O、Cu2+,则该反应中的还原剂是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】物质的分类是学习化学的一种重要方法,科学合理的分类对于提高学习效率、解决问题都有着重要的意义。请回答下列问题:
I.纯净物根据其组成和性质有如图分类形式

(1)图中所示所属的分类方法为_______
(2)下列物质能导电的是_______ (填数字序号,下同),属于混合物的有_______ ,属于电解质的是_______ 。
①NaCl晶体 ②CO2 ③K2CO3溶液 ④铜 ⑤CaCO3固体 ⑥乙醇 ⑦氨水 ⑧稀硫酸 ⑨熔化的NaHSO4
(3)写出NaHSO4在水溶液中的电离方程式_______ 。
(4)写出③和⑧反应的离子方程式_______ 。
II.我们可以从不同角度认识化学反应,四种基本反应类型与氧化还原反应的关系如图所示。

(5)下列化学反应属于阴影区域的是_______
A. SO2+H2O2=H2SO4
B. 3CO+Fe2O3 2Fe+3CO2
2Fe+3CO2
C. 2Na2O2+2H2O=4NaOH+O2↑
D.Br2+2KI=I2+2KBr
E. 2Fe(OH)3 Fe2O3+3H2O
Fe2O3+3H2O
I.纯净物根据其组成和性质有如图分类形式

(1)图中所示所属的分类方法为
(2)下列物质能导电的是
①NaCl晶体 ②CO2 ③K2CO3溶液 ④铜 ⑤CaCO3固体 ⑥乙醇 ⑦氨水 ⑧稀硫酸 ⑨熔化的NaHSO4
(3)写出NaHSO4在水溶液中的电离方程式
(4)写出③和⑧反应的离子方程式
II.我们可以从不同角度认识化学反应,四种基本反应类型与氧化还原反应的关系如图所示。

(5)下列化学反应属于阴影区域的是
A. SO2+H2O2=H2SO4
B. 3CO+Fe2O3
 2Fe+3CO2
2Fe+3CO2C. 2Na2O2+2H2O=4NaOH+O2↑
D.Br2+2KI=I2+2KBr
E. 2Fe(OH)3
 Fe2O3+3H2O
Fe2O3+3H2O
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】用双线桥法标出下列反应的电子转移情况和化合价升降情况
Fe+H2SO4=FeSO4+H2↑_____________________________________
Fe+H2SO4=FeSO4+H2↑
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】化学反应按照不同的分类方法,可以分为化合反应、分解反应、置换反应、复分解反应,也可分为氧化还原反应和非氧化还原反应。有下列反应:①CO2+C 2CO②Cu2(OH)2CO3
2CO②Cu2(OH)2CO3 2CuO+H2O+CO2↑③2NaOH+Cl2=NaCl+NaClO+H2O④2CO+O2
2CuO+H2O+CO2↑③2NaOH+Cl2=NaCl+NaClO+H2O④2CO+O2 2CO2⑤3Fe+4H2O(g)
2CO2⑤3Fe+4H2O(g)  Fe3O4+4H2⑥CuO+CO
Fe3O4+4H2⑥CuO+CO Cu+CO2⑦2H2O
Cu+CO2⑦2H2O 2H2↑+O2↑⑧CO2+H2O=H2CO3
2H2↑+O2↑⑧CO2+H2O=H2CO3
(1)其中属于化合反应的有___________ (填序号,下同),属于置换反应的有___________ 。
(2)在化学反应前后元素的化合价没有变化的是___________ 。
(3)上述反应中,既是分解反应,又是氧化还原反应的是___________ 。
(4)上述反应中,既是溶液中的离子反应,又是氧化还原反应的是___________ 。
(5)根据你的理解,氧化还原反应的实质是___________ 。
(6)用双线桥法表示⑥反应的电子转移情况,并指出氧化产物和还原产物_________________________________ 。
(7)用单线桥法表示⑤ 反应的电子转移情况,并指出氧化剂和还原剂_________________________________ 。
 2CO②Cu2(OH)2CO3
2CO②Cu2(OH)2CO3 2CuO+H2O+CO2↑③2NaOH+Cl2=NaCl+NaClO+H2O④2CO+O2
2CuO+H2O+CO2↑③2NaOH+Cl2=NaCl+NaClO+H2O④2CO+O2 2CO2⑤3Fe+4H2O(g)
2CO2⑤3Fe+4H2O(g)  Fe3O4+4H2⑥CuO+CO
Fe3O4+4H2⑥CuO+CO Cu+CO2⑦2H2O
Cu+CO2⑦2H2O 2H2↑+O2↑⑧CO2+H2O=H2CO3
2H2↑+O2↑⑧CO2+H2O=H2CO3(1)其中属于化合反应的有
(2)在化学反应前后元素的化合价没有变化的是
(3)上述反应中,既是分解反应,又是氧化还原反应的是
(4)上述反应中,既是溶液中的离子反应,又是氧化还原反应的是
(5)根据你的理解,氧化还原反应的实质是
(6)用双线桥法表示⑥反应的电子转移情况,并指出氧化产物和还原产物
(7)用单线桥法表示⑤ 反应的电子转移情况,并指出氧化剂和还原剂
您最近一年使用:0次



