化学反应按照不同的分类方法,可以分为化合反应、分解反应、置换反应、复分解反应,也可分为氧化还原反应和非氧化还原反应。有下列反应:①CO2+C 2CO②Cu2(OH)2CO3
2CO②Cu2(OH)2CO3 2CuO+H2O+CO2↑③2NaOH+Cl2=NaCl+NaClO+H2O④2CO+O2
2CuO+H2O+CO2↑③2NaOH+Cl2=NaCl+NaClO+H2O④2CO+O2 2CO2⑤3Fe+4H2O(g)
2CO2⑤3Fe+4H2O(g)  Fe3O4+4H2⑥CuO+CO
Fe3O4+4H2⑥CuO+CO Cu+CO2⑦2H2O
Cu+CO2⑦2H2O 2H2↑+O2↑⑧CO2+H2O=H2CO3
2H2↑+O2↑⑧CO2+H2O=H2CO3
(1)其中属于化合反应的有___________ (填序号,下同),属于置换反应的有___________ 。
(2)在化学反应前后元素的化合价没有变化的是___________ 。
(3)上述反应中,既是分解反应,又是氧化还原反应的是___________ 。
(4)上述反应中,既是溶液中的离子反应,又是氧化还原反应的是___________ 。
(5)根据你的理解,氧化还原反应的实质是___________ 。
(6)用双线桥法表示⑥反应的电子转移情况,并指出氧化产物和还原产物_________________________________ 。
(7)用单线桥法表示⑤ 反应的电子转移情况,并指出氧化剂和还原剂_________________________________ 。
 2CO②Cu2(OH)2CO3
2CO②Cu2(OH)2CO3 2CuO+H2O+CO2↑③2NaOH+Cl2=NaCl+NaClO+H2O④2CO+O2
2CuO+H2O+CO2↑③2NaOH+Cl2=NaCl+NaClO+H2O④2CO+O2 2CO2⑤3Fe+4H2O(g)
2CO2⑤3Fe+4H2O(g)  Fe3O4+4H2⑥CuO+CO
Fe3O4+4H2⑥CuO+CO Cu+CO2⑦2H2O
Cu+CO2⑦2H2O 2H2↑+O2↑⑧CO2+H2O=H2CO3
2H2↑+O2↑⑧CO2+H2O=H2CO3(1)其中属于化合反应的有
(2)在化学反应前后元素的化合价没有变化的是
(3)上述反应中,既是分解反应,又是氧化还原反应的是
(4)上述反应中,既是溶液中的离子反应,又是氧化还原反应的是
(5)根据你的理解,氧化还原反应的实质是
(6)用双线桥法表示⑥反应的电子转移情况,并指出氧化产物和还原产物
(7)用单线桥法表示⑤ 反应的电子转移情况,并指出氧化剂和还原剂
更新时间:2022-12-02 17:36:30
|
相似题推荐
【推荐1】I.在肉制品加工中,使用的护色剂——亚硝酸钠(NaNO2)必须严格控制用量,以确保食用安全。已知:
(1)配平并标出上述反应电子转移的方向和数目:___________
(2)该反应中的氧化剂是___________ 。
(3)若有1mol氧化产物生成,则转移的电子数目是___________ mol。
(4)若误食亚硝酸钠会导致血红蛋白中亚铁离子转化为铁离子而中毒,服用维生素C可解除亚硝酸钠的中毒,下列关于上述中毒。解毒过程的说法中,正确的是___________。
II.已知:Cl2是一种有毒气体,如果泄漏会造成严重的危害。
(5)实验室常用烧碱溶液吸收Cl2。若将Cl2通入热的烧碱溶液中,可以得到NaCl、NaClO和NaClO3的混合液。当NaCl和NaClO3的物质的量之比为8∶1时,混合液中NaClO和NaClO3的物质的量之比为___________ 。
(6)某同学把新制的氯水(主要成分Cl2)加到NaNO2溶液中,观察到氯水褪色,同时生成NaNO3和HCl,请写出反应的离子方程式:___________ 。

(1)配平并标出上述反应电子转移的方向和数目:
(2)该反应中的氧化剂是
(3)若有1mol氧化产物生成,则转移的电子数目是
(4)若误食亚硝酸钠会导致血红蛋白中亚铁离子转化为铁离子而中毒,服用维生素C可解除亚硝酸钠的中毒,下列关于上述中毒。解毒过程的说法中,正确的是___________。
| A.亚硝酸钠是还原剂 | B.维生素C是氧化剂 |
| C.维生素C能把铁离子还原成为亚铁离子 | D.亚硝酸钠被氧化 |
II.已知:Cl2是一种有毒气体,如果泄漏会造成严重的危害。
(5)实验室常用烧碱溶液吸收Cl2。若将Cl2通入热的烧碱溶液中,可以得到NaCl、NaClO和NaClO3的混合液。当NaCl和NaClO3的物质的量之比为8∶1时,混合液中NaClO和NaClO3的物质的量之比为
(6)某同学把新制的氯水(主要成分Cl2)加到NaNO2溶液中,观察到氯水褪色,同时生成NaNO3和HCl,请写出反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】储氢纳米碳管的研究成功体现了科技的进步,但用电弧法合成的碳纳米管常伴有大量的杂质——碳纳米颗粒,这种碳纳米颗粒可用氧化气化法提纯其反应式为 (未配平)。
(未配平)。
(1)配平上述方程式:_______ 。
(2)上述反应中氧化剂是_______ (填化学式),氧化产物是_______ (填化学式)。
(3) 在上述反应中表现出来的性质是
在上述反应中表现出来的性质是_______ (填序号)。
a.氧化性 b.氧化性和酸性 c.酸性 d.还原性和酸性
(4)若反应中电子转移了 ,则产生的气体在标准状况下的体积为
,则产生的气体在标准状况下的体积为_______ L。
(5)要使
 的
的 溶液被还原,至少要加入
溶液被还原,至少要加入_______ 
 的
的 溶液。
溶液。
 (未配平)。
(未配平)。(1)配平上述方程式:
(2)上述反应中氧化剂是
(3)
 在上述反应中表现出来的性质是
在上述反应中表现出来的性质是a.氧化性 b.氧化性和酸性 c.酸性 d.还原性和酸性
(4)若反应中电子转移了
 ,则产生的气体在标准状况下的体积为
,则产生的气体在标准状况下的体积为(5)要使

 的
的 溶液被还原,至少要加入
溶液被还原,至少要加入
 的
的 溶液。
溶液。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】氧化还原反应原理在生产生活和科学研究中应用广泛。
(1)下列表述中没有氧化还原反应发生的是_____ 。
a.滴水成冰 b.蜡炬成灰 c.百炼成钢
(2)NH3和Cl2反应的方程式为:NH3+Cl2—N2+HCl
①该反应中被氧化的元素是___ (填元素名称),氧化剂是__ (填化学式)。
②配平该方程式:____ NH3+ ____ Cl2—____ N2+____ HCl
③工业生产中常用喷洒氨水的方法来检查是否有Cl2泄漏,若Cl2有泄漏,可以观察到的现象是______ ,产生该现象的反应方程式为___ 。
(3)“地康法”制氯气的反应原理图示如下:
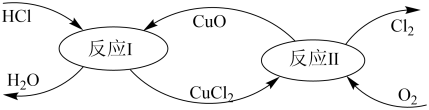
①反应I的化学方程式为____ 。
②若要制得标准状况下氯气11.2L,则整个反应中转移电子的物质的量为____ 。
(1)下列表述中没有氧化还原反应发生的是
a.滴水成冰 b.蜡炬成灰 c.百炼成钢
(2)NH3和Cl2反应的方程式为:NH3+Cl2—N2+HCl
①该反应中被氧化的元素是
②配平该方程式:
③工业生产中常用喷洒氨水的方法来检查是否有Cl2泄漏,若Cl2有泄漏,可以观察到的现象是
(3)“地康法”制氯气的反应原理图示如下:

①反应I的化学方程式为
②若要制得标准状况下氯气11.2L,则整个反应中转移电子的物质的量为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】为解决能源与环境问题,有学者提出如图所示的含碳物质转化的技术路线:

回答下列问题:
(1)上述涉及物质中属于氧化物的是___________ (填化学式)。
(2) 既属于钾盐,也属于碳酸盐,该分类方法属于
既属于钾盐,也属于碳酸盐,该分类方法属于___________ 。
(3)上述反应中,属于氧化还原反应的是___________(填字母)。
(4)应②的化学方程式为___________ ,属于___________ (填基本反应类型)。
(5)反应③中,参加反应的 和生成的
和生成的 的分子数目之比为
的分子数目之比为___________ ,每生成1个 ,转移
,转移___________ 个电子。

回答下列问题:
(1)上述涉及物质中属于氧化物的是
(2)
 既属于钾盐,也属于碳酸盐,该分类方法属于
既属于钾盐,也属于碳酸盐,该分类方法属于(3)上述反应中,属于氧化还原反应的是___________(填字母)。
| A.反应① | B.反应② | C.反应③ | D.反应④ |
(5)反应③中,参加反应的
 和生成的
和生成的 的分子数目之比为
的分子数目之比为 ,转移
,转移
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】回答下列问题:
(1)已知CuO具有氧化性,能够和氨气反应,产物中合有两种单质,请写出在加热条件下CuO和NH3反应的化学方程式___________ 。
(2)在一定条件下,R2+和O2可发生如下反应: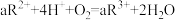 ,由以上反应可知在上述过程中R2+被
,由以上反应可知在上述过程中R2+被___________ (填“氧化”或“还原”),a的值为___________ 。
(3)一个完整的氧化还原反应方程式可以拆开写成两个“半反应式”,一个是“氧化反应”式,一个是“还原反应”式。如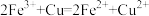 的拆写结果是:氧化反应为:
的拆写结果是:氧化反应为: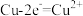 ;还原反应为:
;还原反应为: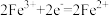 。请据此将反应:
。请据此将反应: 拆写成两个“半反应式”;氧化反应为
拆写成两个“半反应式”;氧化反应为___________ 。
(4) 、
、 、
、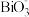 、
、 、
、 、
、 组成的一个氧化还原反应体系中,发生
组成的一个氧化还原反应体系中,发生 的反应过程,将以上物质组成一个正确的离子方程式,并用单线桥标出电子转移方向和数目
的反应过程,将以上物质组成一个正确的离子方程式,并用单线桥标出电子转移方向和数目___________ 。
(5)在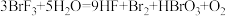 中,若有
中,若有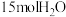 分子参加反应,则被水还原的溴原子的个数为
分子参加反应,则被水还原的溴原子的个数为___________ 。
(1)已知CuO具有氧化性,能够和氨气反应,产物中合有两种单质,请写出在加热条件下CuO和NH3反应的化学方程式
(2)在一定条件下,R2+和O2可发生如下反应:
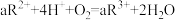 ,由以上反应可知在上述过程中R2+被
,由以上反应可知在上述过程中R2+被(3)一个完整的氧化还原反应方程式可以拆开写成两个“半反应式”,一个是“氧化反应”式,一个是“还原反应”式。如
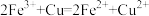 的拆写结果是:氧化反应为:
的拆写结果是:氧化反应为: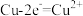 ;还原反应为:
;还原反应为: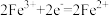 。请据此将反应:
。请据此将反应: 拆写成两个“半反应式”;氧化反应为
拆写成两个“半反应式”;氧化反应为(4)
 、
、 、
、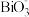 、
、 、
、 、
、 组成的一个氧化还原反应体系中,发生
组成的一个氧化还原反应体系中,发生 的反应过程,将以上物质组成一个正确的离子方程式,并用单线桥标出电子转移方向和数目
的反应过程,将以上物质组成一个正确的离子方程式,并用单线桥标出电子转移方向和数目(5)在
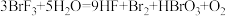 中,若有
中,若有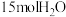 分子参加反应,则被水还原的溴原子的个数为
分子参加反应,则被水还原的溴原子的个数为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】已知反应:
①SO3+H2O=H2SO4
②3NO2+H2O=2HNO3+NO
③2F2+2H2O=4HF+O2
④2Na+2H2O=2NaOH+H2↑
⑤Na2O+2HCl=2NaCl+H2O
⑥Al2O3+2NaOH=2NaAlO2+H2O
(1)上述反应不属于氧化还原反应的有___________ (填序号,下同)。H2O被氧化的是___________ ,H2O被还原的是___________ 。
(2)用双线桥法表示反应②的电子转移方向和数目:___________ 。
(3)用单线桥法表示反应③的电子转移方___________ 。
(4)写出反应④的离子方程式:___________ 。
①SO3+H2O=H2SO4
②3NO2+H2O=2HNO3+NO
③2F2+2H2O=4HF+O2
④2Na+2H2O=2NaOH+H2↑
⑤Na2O+2HCl=2NaCl+H2O
⑥Al2O3+2NaOH=2NaAlO2+H2O
(1)上述反应不属于氧化还原反应的有
(2)用双线桥法表示反应②的电子转移方向和数目:
(3)用单线桥法表示反应③的电子转移方
(4)写出反应④的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】对于数以千万计的化学物质和为数众多的化学反应,分类法的作用几乎是无可代替的。
Ⅰ.现有以下物质:①H2O ②Cu ③BaCO3 ④Fe(OH)3胶体 ⑤NaHSO4溶液 ⑥干冰 ⑦稀硫酸⑧四氯化碳⑨氢氧化钡
(1)以上物质中属于混合物的是___________ (填序号,下同),属于电解质的是___________ 。
(2)向④中逐滴滴加⑦,可观察到的现是___________ 。
Ⅱ.虽然分类的方法不同,但四种基本反应类型和离子反应、氧化还原反应之间也存在着一定的关系。
(3)如图为离子反应、氧化还原反应和置换反应三者之间的关系,其中表示离子反应的是___________ (填字母)。
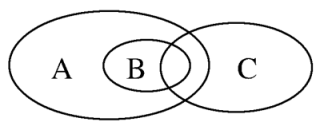
(4)有同学认为所有酸碱中和反应均可表示为H++OH-=H2O。请举个例子反驳上述观点(用离子方程式表示)___________ 。
(5)写出物质⑤和⑨的水溶液混合反应成中性时的离子方程式:___________ 。
Ⅰ.现有以下物质:①H2O ②Cu ③BaCO3 ④Fe(OH)3胶体 ⑤NaHSO4溶液 ⑥干冰 ⑦稀硫酸⑧四氯化碳⑨氢氧化钡
(1)以上物质中属于混合物的是
(2)向④中逐滴滴加⑦,可观察到的现是
Ⅱ.虽然分类的方法不同,但四种基本反应类型和离子反应、氧化还原反应之间也存在着一定的关系。
(3)如图为离子反应、氧化还原反应和置换反应三者之间的关系,其中表示离子反应的是

(4)有同学认为所有酸碱中和反应均可表示为H++OH-=H2O。请举个例子反驳上述观点(用离子方程式表示)
(5)写出物质⑤和⑨的水溶液混合反应成中性时的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】现有以下物质:①熔融态NaOH ②Cu③BaCO3④Fe(OH)3胶体 ⑤酒精⑥CO2 ⑦硫酸 ⑧盐酸
(1)以上物质中属于混合物的是_____ (填序号,下同),
能导电的是_____ .
属于电解质的是_____ .
(2)向④中逐滴滴加⑧,可观察到的现象是_____ .
(3)虽然分类的方法不同,但四种基本反应类型和离子反应、氧化还原反应之间也存在着一定的关系. 图为离子反应、氧化还原反应和置换反应三者之间的关系,其中表示离子反应的是_____ (填字母).

(4)有同学认为所有酸碱中和反应均可表示为:H++OH﹣=H2O.请举个例子反驳上述观点(用离子方程式表示)_____ .
( 5) 宋代著名法医学家宋慈的《洗冤集录》中有“ 银针验毒” 的记载,“ 银针验毒” 的原理是:
4Ag+2H2S+O2═2X+2H2O.则 X 的化学式为_____ .其中 H2S 是该反应的_____ (填序号).
A.氧化剂 B.还原剂
C.既是氧化剂又是还原剂 D.既不是氧化剂又不是还原剂.
(1)以上物质中属于混合物的是
能导电的是
属于电解质的是
(2)向④中逐滴滴加⑧,可观察到的现象是
(3)虽然分类的方法不同,但四种基本反应类型和离子反应、氧化还原反应之间也存在着一定的关系. 图为离子反应、氧化还原反应和置换反应三者之间的关系,其中表示离子反应的是

(4)有同学认为所有酸碱中和反应均可表示为:H++OH﹣=H2O.请举个例子反驳上述观点(用离子方程式表示)
( 5) 宋代著名法医学家宋慈的《洗冤集录》中有“ 银针验毒” 的记载,“ 银针验毒” 的原理是:
4Ag+2H2S+O2═2X+2H2O.则 X 的化学式为
A.氧化剂 B.还原剂
C.既是氧化剂又是还原剂 D.既不是氧化剂又不是还原剂.
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】已知反应:①SO3+H2O=H2SO4 ②3NO2+H2O=2HNO3+NO ③2F2+2H2O=4HF+O2 ④2Na+2H2O=2NaOH+H2↑ ⑤Na2O+2HCl=2NaCl+H2O ⑥SiO2+2NaOH=Na2SiO3+H2O
(1)上述反应中不属于氧化还原反应的有_______ (填序号,下同)。H2O被氧化的是_______ ,H2O被还原的是_______ ,属于氧化还原反应,但其中的H2O既不被氧化又不被还原的是_______ 。
(2)用双线桥表示反应②的电子转移方向和数目:_______ 。
3NO2+H2O=2HNO3+NO
(3)用单线桥标出反应③的电子转移方向和数目:_______ 。
2F2+2H2O=4HF+O2
(4)写出反应④的离子方程式:_______ 。
(1)上述反应中不属于氧化还原反应的有
(2)用双线桥表示反应②的电子转移方向和数目:
3NO2+H2O=2HNO3+NO
(3)用单线桥标出反应③的电子转移方向和数目:
2F2+2H2O=4HF+O2
(4)写出反应④的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】现有下列10种物质:① ②
② ③
③ 固体 ④
固体 ④ 固体
固体
⑤葡萄糖 ⑥石墨 ⑦ 溶液 ⑧
溶液 ⑧ 气体 ⑨熔融氯化钾 ⑩生理盐水
气体 ⑨熔融氯化钾 ⑩生理盐水
请回答下列问题:
(1)与⑥互为同素异形体的一种物质是___________ (填物质的名称)。
(2)以上物质属盐的有___________ (填序号,下同)。
(3)以上物质属于电解质的有______________________ 。
(4)上述状态下能够导电的物质是______________________ 。
(5)小苏打治疗胃酸过多的离子反应方程式___________________ 。
(6)稀硫酸和澄清石灰水反应的离子反应方程式_________________ 。
(7)配平该离子反应方程式并用双线桥表示电子转移方向和数目__________ 。
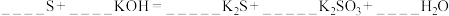
 ②
② ③
③ 固体 ④
固体 ④ 固体
固体⑤葡萄糖 ⑥石墨 ⑦
 溶液 ⑧
溶液 ⑧ 气体 ⑨熔融氯化钾 ⑩生理盐水
气体 ⑨熔融氯化钾 ⑩生理盐水请回答下列问题:
(1)与⑥互为同素异形体的一种物质是
(2)以上物质属盐的有
(3)以上物质属于电解质的有
(4)上述状态下能够导电的物质是
(5)小苏打治疗胃酸过多的离子反应方程式
(6)稀硫酸和澄清石灰水反应的离子反应方程式
(7)配平该离子反应方程式并用双线桥表示电子转移方向和数目
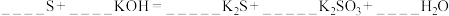
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】高铁酸钾( ,极易溶于水)是常见的水处理剂,其原理如图所示。
,极易溶于水)是常见的水处理剂,其原理如图所示。
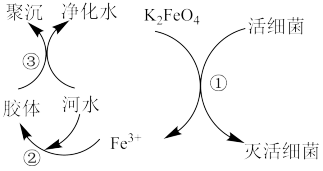
【查阅资料】向胶体中加入电解质后,胶体因失去稳定性而发生离子的聚集以至沉淀,称为电解质对胶体的聚沉作用,简称胶体的聚沉。
请回答下列问题:
(1) 中铁元素的化合价为
中铁元素的化合价为_______ 价。
(2)过程①中活性菌表现了_______ (填“氧化”或“还原”)性,该过程的还原产物是_______ (填离子符号);过程③属于_______ (填“物理”或“化学”)变化。
(3)根据上述原理分析,作水处理剂时, 的作用有
的作用有_______ (填两个)。
(4)制备高铁酸钾常用的反应原理为 (反应未配平)。
(反应未配平)。
①该反应中,Cl元素的化合价由_______ 价变为_______ 价;通过该反应说明:在碱性条件下,氧化性
_______ (填“>”、“=”或“<”) 。
。
②配平该反应的化学方程式,并用双线桥法表示电子转移的方向和数目:_______ ,将该反应改写为离子方程式:_______ 。
 ,极易溶于水)是常见的水处理剂,其原理如图所示。
,极易溶于水)是常见的水处理剂,其原理如图所示。
【查阅资料】向胶体中加入电解质后,胶体因失去稳定性而发生离子的聚集以至沉淀,称为电解质对胶体的聚沉作用,简称胶体的聚沉。
请回答下列问题:
(1)
 中铁元素的化合价为
中铁元素的化合价为(2)过程①中活性菌表现了
(3)根据上述原理分析,作水处理剂时,
 的作用有
的作用有(4)制备高铁酸钾常用的反应原理为
 (反应未配平)。
(反应未配平)。①该反应中,Cl元素的化合价由

 。
。②配平该反应的化学方程式,并用双线桥法表示电子转移的方向和数目:
您最近一年使用:0次


 ____NO+____H2O
____NO+____H2O

