回答下列问题:
(1)虽然分类的方法不同,但四种基本反应和离子反应、氧化还原反应之间也存在着一定的关系。如图为离子反应、氧化还原反应和置换反应三者之间的关系,其中表示离子反应的是___ (填字母)。

(2)利用氧化还原反应原理配平如下方程式:___
____NH3+____O2 ____NO+____H2O
____NO+____H2O
(3)用单线桥法标出如下反应的电子转移的方向和数目:___ 。
Cl2+SO2+2H2O=H2SO4+2HCl
(1)虽然分类的方法不同,但四种基本反应和离子反应、氧化还原反应之间也存在着一定的关系。如图为离子反应、氧化还原反应和置换反应三者之间的关系,其中表示离子反应的是

(2)利用氧化还原反应原理配平如下方程式:
____NH3+____O2
 ____NO+____H2O
____NO+____H2O(3)用单线桥法标出如下反应的电子转移的方向和数目:
Cl2+SO2+2H2O=H2SO4+2HCl
更新时间:2021-10-22 11:11:01
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】回答下列问题:
(1)某反应化学方程式为:10Al+6NaNO3+4NaOH=10NaAlO2+3N2+2H2O。其中被还原的元素是______ (填元素符号,下同),被氧化的元素是______ ,氧化剂是______ (填化学式,下同),还原剂是______ ,氧化产物是______ ,还原产物是______ 。
(2)储氢纳米碳管的研制成功体现了科技的进步。用电弧法合成的碳纳米管常伴有大量的杂质-碳纳米颗粒。这种碳纳米颗粒可用氧化气化法提纯。其反应中的反应物和生成物有C、CO2、H2SO4、K2Cr2O7、K2SO4、Cr2(SO4)3和H2O七种。
①用上述物质填空并配平:______ 。
( )C+( )______+( )H2SO4=( )______+( )K2SO4+( )Cr2(SO4)3+( )H2O
②H2SO4在该反应中表现出来的性质是______ (填选项序号)。
A.氧化性 B.氧化性和酸性 C.酸性 D.还原性和酸性
(3)我国发射的探月卫星燃料之一是铝粉与高氯酸铵(NH4ClO4)固体混合物,点燃时铝粉被氧化放大量热,引发高氯酸铵发生反应:2NH4ClO4=N2↑+4H2O+Cl2+2O2↑,对该反应类型判断正确的是______ 。
A.氧化还原反应 B.复分解反应 C.置换反应 D.分解反应 E.化合反应
反应中氧化产物与还原产物的质量比为______ 。
(4)KClO3与浓盐酸在一定温度下反应会生成黄绿色的易爆物质二氧化氯,其变化为:KClO3+HCl(浓)→KCl+ClO2+Cl2+H2O,若产生7.1gCl2,则生成ClO2的质量为______ g。
(1)某反应化学方程式为:10Al+6NaNO3+4NaOH=10NaAlO2+3N2+2H2O。其中被还原的元素是
(2)储氢纳米碳管的研制成功体现了科技的进步。用电弧法合成的碳纳米管常伴有大量的杂质-碳纳米颗粒。这种碳纳米颗粒可用氧化气化法提纯。其反应中的反应物和生成物有C、CO2、H2SO4、K2Cr2O7、K2SO4、Cr2(SO4)3和H2O七种。
①用上述物质填空并配平:
( )C+( )______+( )H2SO4=( )______+( )K2SO4+( )Cr2(SO4)3+( )H2O
②H2SO4在该反应中表现出来的性质是
A.氧化性 B.氧化性和酸性 C.酸性 D.还原性和酸性
(3)我国发射的探月卫星燃料之一是铝粉与高氯酸铵(NH4ClO4)固体混合物,点燃时铝粉被氧化放大量热,引发高氯酸铵发生反应:2NH4ClO4=N2↑+4H2O+Cl2+2O2↑,对该反应类型判断正确的是
A.氧化还原反应 B.复分解反应 C.置换反应 D.分解反应 E.化合反应
反应中氧化产物与还原产物的质量比为
(4)KClO3与浓盐酸在一定温度下反应会生成黄绿色的易爆物质二氧化氯,其变化为:KClO3+HCl(浓)→KCl+ClO2+Cl2+H2O,若产生7.1gCl2,则生成ClO2的质量为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】利用所学化学知识,分析并回答下列各小题。
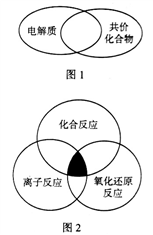
(1)下列物质属于图1所示化学概念交叉部分的有______ (填标号)。
a.氨气 b.硝酸 c.乙醇 d.醋酸钠
(2)下列各反应属于图2中阴影部分所示关系的有_______ (填标号)。
a.氨气与浓硝酸
b.氢气与氧气
c.氯气与氯化亚铁溶液
d.铜与氯化铁溶液
(3)下列有关说法正确的是_____ (填标号)。
a.核电站把核能转化为电能
b.常温下铜与浓硫酸发生钝化。反应很快停止
c.海水中提取化学物质均涉及到氧化还原反应
d.电解法得到某元素单质,则该元素可能被还原,也可能被氧化
(4)下列各实验过程中,需要检查所用某些仪器是否漏水的有_______ (填标号)。
a.氢气还原氧化铜
b.水与煤油混合物分离
c.氯化钠溶液与泥沙分离
d.配制100mL 10mol·L-1碳酸钠溶液
(5)下列关于试剂保存的叙述正确的是_________ (填标号)。
a.氢氟酸保存在玻璃瓶中
b.KOH溶液保存在带玻璃塞的细口瓶中
c.溴水保存在带橡胶塞的棕色瓶中
d.KMnO4与乙醇不能放在同一药品厨中

(1)下列物质属于图1所示化学概念交叉部分的有
a.氨气 b.硝酸 c.乙醇 d.醋酸钠
(2)下列各反应属于图2中阴影部分所示关系的有
a.氨气与浓硝酸
b.氢气与氧气
c.氯气与氯化亚铁溶液
d.铜与氯化铁溶液
(3)下列有关说法正确的是
a.核电站把核能转化为电能
b.常温下铜与浓硫酸发生钝化。反应很快停止
c.海水中提取化学物质均涉及到氧化还原反应
d.电解法得到某元素单质,则该元素可能被还原,也可能被氧化
(4)下列各实验过程中,需要检查所用某些仪器是否漏水的有
a.氢气还原氧化铜
b.水与煤油混合物分离
c.氯化钠溶液与泥沙分离
d.配制100mL 10mol·L-1碳酸钠溶液
(5)下列关于试剂保存的叙述正确的是
a.氢氟酸保存在玻璃瓶中
b.KOH溶液保存在带玻璃塞的细口瓶中
c.溴水保存在带橡胶塞的棕色瓶中
d.KMnO4与乙醇不能放在同一药品厨中
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】现有以下物质:①熔融态NaOH ②Cu③BaCO3④Fe(OH)3胶体 ⑤酒精⑥CO2 ⑦硫酸 ⑧盐酸
(1)以上物质中属于混合物的是_____ (填序号,下同),
能导电的是_____ .
属于电解质的是_____ .
(2)向④中逐滴滴加⑧,可观察到的现象是_____ .
(3)虽然分类的方法不同,但四种基本反应类型和离子反应、氧化还原反应之间也存在着一定的关系. 图为离子反应、氧化还原反应和置换反应三者之间的关系,其中表示离子反应的是_____ (填字母).

(4)有同学认为所有酸碱中和反应均可表示为:H++OH﹣=H2O.请举个例子反驳上述观点(用离子方程式表示)_____ .
( 5) 宋代著名法医学家宋慈的《洗冤集录》中有“ 银针验毒” 的记载,“ 银针验毒” 的原理是:
4Ag+2H2S+O2═2X+2H2O.则 X 的化学式为_____ .其中 H2S 是该反应的_____ (填序号).
A.氧化剂 B.还原剂
C.既是氧化剂又是还原剂 D.既不是氧化剂又不是还原剂.
(1)以上物质中属于混合物的是
能导电的是
属于电解质的是
(2)向④中逐滴滴加⑧,可观察到的现象是
(3)虽然分类的方法不同,但四种基本反应类型和离子反应、氧化还原反应之间也存在着一定的关系. 图为离子反应、氧化还原反应和置换反应三者之间的关系,其中表示离子反应的是

(4)有同学认为所有酸碱中和反应均可表示为:H++OH﹣=H2O.请举个例子反驳上述观点(用离子方程式表示)
( 5) 宋代著名法医学家宋慈的《洗冤集录》中有“ 银针验毒” 的记载,“ 银针验毒” 的原理是:
4Ag+2H2S+O2═2X+2H2O.则 X 的化学式为
A.氧化剂 B.还原剂
C.既是氧化剂又是还原剂 D.既不是氧化剂又不是还原剂.
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】现有下列反应:
①2H2O+Cl2+SO2=H2SO4+2HCl
②2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O
针对上述两个反应回答:
(1)用单线桥标出①中电子转移的方向和数目_____ ;
(2)写出②的离子化学方程式____ ;
(3)Cl2、SO2和KMnO4的氧化性由强到弱的顺序为____ ;
(4)反应②中氯化氢表现出的性质是____ 。
a.还原性 b.酸性 c.氧化性
①2H2O+Cl2+SO2=H2SO4+2HCl
②2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O
针对上述两个反应回答:
(1)用单线桥标出①中电子转移的方向和数目
(2)写出②的离子化学方程式
(3)Cl2、SO2和KMnO4的氧化性由强到弱的顺序为
(4)反应②中氯化氢表现出的性质是
a.还原性 b.酸性 c.氧化性
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】二氧化硒(SeO2)是一种氧化剂,其被还原后的单质硒可能成为环境污染物,通过与浓 或浓
或浓 反应生成
反应生成 以回收
以回收 。完成下列填空:
。完成下列填空:
(1) 和浓
和浓 反应的还原产物为
反应的还原产物为 和
和 ,且
,且 和
和 的物质的量之比为1:1,写出
的物质的量之比为1:1,写出 和浓
和浓 的化学反应方程式
的化学反应方程式___________
(2)已知: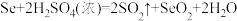
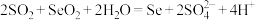
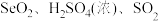 的氧化性由强到弱的顺序是
的氧化性由强到弱的顺序是___________
(3)回收得到的 的含量。可以通过下面的方法测定:
的含量。可以通过下面的方法测定:
①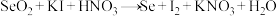
②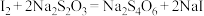
配平方程式①,并用双线桥标出电子转移的方向和数目___________
(4)上述②方程式中每生成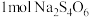 转移电子数的物质的量为:
转移电子数的物质的量为:___________
 或浓
或浓 反应生成
反应生成 以回收
以回收 。完成下列填空:
。完成下列填空:(1)
 和浓
和浓 反应的还原产物为
反应的还原产物为 和
和 ,且
,且 和
和 的物质的量之比为1:1,写出
的物质的量之比为1:1,写出 和浓
和浓 的化学反应方程式
的化学反应方程式(2)已知:
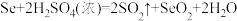
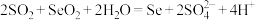
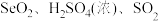 的氧化性由强到弱的顺序是
的氧化性由强到弱的顺序是(3)回收得到的
 的含量。可以通过下面的方法测定:
的含量。可以通过下面的方法测定:①
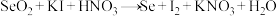
②
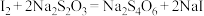
配平方程式①,并用双线桥标出电子转移的方向和数目
(4)上述②方程式中每生成
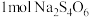 转移电子数的物质的量为:
转移电子数的物质的量为:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】研究物质性质及物质转化具有重要的价值,根据所学知识回答下列问题:
(1)火药是中国的四大发明之一,永远值得华夏儿女骄傲。黑火药在发生爆炸时,发生如下反应: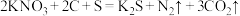 。其中作氧化剂的是
。其中作氧化剂的是_______ (填化学式)。
(2)中国古代著作中有“银针验毒”的记录,其原理为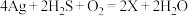 ,则X的化学式是
,则X的化学式是_______ ,其中 在该反应中
在该反应中_______ (填标号)。
A.作氧化剂 B.作还原剂
C.既是氧化剂又是还原剂 D.既不是氧化剂又不是还原剂
(3)按如图所示操作,充分反应后:

①Ⅱ中铜丝上观察到的现象是_______ 。
②结合Ⅰ、Ⅱ实验现象可知 、
、 、
、 的氧化性由强到弱的顺序为
的氧化性由强到弱的顺序为_______ 。
(4)已知 可发生反应:
可发生反应: 。
。
①该反应中氧化剂是_______ (填化学式,下同),还原剂是_______ 。
②用双线桥法标出电子转移的数目和方向:_______ 。
(1)火药是中国的四大发明之一,永远值得华夏儿女骄傲。黑火药在发生爆炸时,发生如下反应:
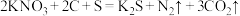 。其中作氧化剂的是
。其中作氧化剂的是(2)中国古代著作中有“银针验毒”的记录,其原理为
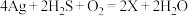 ,则X的化学式是
,则X的化学式是 在该反应中
在该反应中A.作氧化剂 B.作还原剂
C.既是氧化剂又是还原剂 D.既不是氧化剂又不是还原剂
(3)按如图所示操作,充分反应后:

①Ⅱ中铜丝上观察到的现象是
②结合Ⅰ、Ⅱ实验现象可知
 、
、 、
、 的氧化性由强到弱的顺序为
的氧化性由强到弱的顺序为(4)已知
 可发生反应:
可发生反应: 。
。①该反应中氧化剂是
②用双线桥法标出电子转移的数目和方向:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】置换反应的通式可表示为:

单质甲、乙和化合物A、B为中学常见物质,请回答下列问题:
(1)若A为两种元素形成常温下呈液态的化合物,化合物B的焰色反应呈黄色,则该反应的化学方程式为:_________________________________ 。
(2)若甲是一种金属单质,在高温条件下,本反应常用于焊接钢轨。则该反应的化学方程式为:____________________________________ 。
(3)若单质乙是黑色非金属固体单质,化合物B是一种白色金属氧化物,则该反应的化学方程式为:_____________________________________ 。

单质甲、乙和化合物A、B为中学常见物质,请回答下列问题:
(1)若A为两种元素形成常温下呈液态的化合物,化合物B的焰色反应呈黄色,则该反应的化学方程式为:
(2)若甲是一种金属单质,在高温条件下,本反应常用于焊接钢轨。则该反应的化学方程式为:
(3)若单质乙是黑色非金属固体单质,化合物B是一种白色金属氧化物,则该反应的化学方程式为:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】水具有很高的热稳定性,即使加热到1727°C 也只有0.588%的水分解成氢气和氧气。科学家已经找到了一种方法, 分三步可使水在500°C以下分解:首先在500°C下 加热FeCl2水溶液,将生成的Fe3O4在HCl介质中与Cl2在100°C 时反应,最后将生成们固体物质在300°C时加热分解。根据以上信息,请补全第二个反应的化学方程式:
①3FeCl2+4H2O Fe3O4+6HCl+H2:
Fe3O4+6HCl+H2:
②____________________ ;
③3FeCl3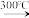 3FeCl2+3/2C12
3FeCl2+3/2C12
①3FeCl2+4H2O
 Fe3O4+6HCl+H2:
Fe3O4+6HCl+H2:②
③3FeCl3
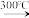 3FeCl2+3/2C12
3FeCl2+3/2C12
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】1797年,法国化学家Vauquelin发现了一种新元素。由于包含这种元素的矿物呈现出多种颜色,因此称之为Chromium,元素符号为Cr。一些含Cr元素的物质或微粒的性质如表。
(1)取少量Cr(OH)3于试管中,逐滴加入稀硫酸,直至过量,可观察到的现象为___________ 。
(2)请结合平衡移动原理,解释(1)中现象___________ 。
(3)将Cr(OH)3加热可得到Cr2O3固体,将稍过量的Cr2O3固体与Na2CO3固体混合均匀,在空气中高温煅烧,可得到黄色的Na2CrO4固体,请写出该反应的化学方程式___________ 。
(4)Na2CrO4部分水合物溶解度如图1。
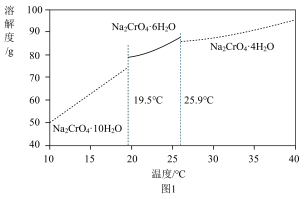
将(3)中所得固体溶解于水中,过滤,得到Na2CrO4溶液。从该溶液中获得Na2CrO4•6H2O的方法为___________ 。
(5)向0.1mol/LNa2CrO4溶液滴加浓硫酸(忽略溶液体积变化),不同pH下,溶液中含+6价Cr元素的微粒浓度变化如图2所示。
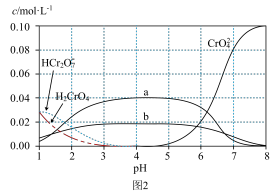
①a代表的微粒是___________ 。
②溶液由pH4.5向pH3.5转化过程中,溶液颜色几乎不变,请结合化学用语解释其原因_______ 。
| 物质 | Cr(OH)3 | H2CrO4 | H2Cr2O7 | |||||
| 性质 | 灰蓝色固体,难溶于水两性氢氧化物 | 红色固体,水溶液为黄色中强酸 | 无纯净物,只存在于水溶液中,强酸 | |||||
| 微粒 | Cr3+ | Cr(OH) |  、HCrO 、HCrO |  、HCr2O 、HCr2O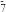 | ||||
| 颜色 | 蓝紫色 | 绿色 | 黄色 | 橙红色 | ||||
(1)取少量Cr(OH)3于试管中,逐滴加入稀硫酸,直至过量,可观察到的现象为
(2)请结合平衡移动原理,解释(1)中现象
(3)将Cr(OH)3加热可得到Cr2O3固体,将稍过量的Cr2O3固体与Na2CO3固体混合均匀,在空气中高温煅烧,可得到黄色的Na2CrO4固体,请写出该反应的化学方程式
(4)Na2CrO4部分水合物溶解度如图1。

将(3)中所得固体溶解于水中,过滤,得到Na2CrO4溶液。从该溶液中获得Na2CrO4•6H2O的方法为
(5)向0.1mol/LNa2CrO4溶液滴加浓硫酸(忽略溶液体积变化),不同pH下,溶液中含+6价Cr元素的微粒浓度变化如图2所示。

①a代表的微粒是
②溶液由pH4.5向pH3.5转化过程中,溶液颜色几乎不变,请结合化学用语解释其原因
您最近一年使用:0次



