X、Y、Z、W是短周期主族元素,X原子最外层电子数是其内层电子数的2倍;Y是短周期元素中原子半径最大的;Z的单质多出现在火山口附近,且为淡黄色晶体;W的单质常温下为黄绿色气体。下列叙述正确的是
| A.简单离子半径的大小:W>Z>Y |
| B.X的单质只有两种同素异形体 |
| C.Y的最高价氧化物对应水化物的碱性在同周期中最强 |
| D.Z的氢化物的稳定性比W的氢化物的稳定性强 |
更新时间:2020-11-02 16:50:35
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】X、Y、Z、W是原子序数依次增大的四种短周期元素,甲、乙、丙、丁、戊是由其中两种或三种元素组成的化合物,己是Z元素形成的单质。已知:甲+乙→丁+己,甲+丙→戊+己;25℃时,0.1 mol·L-1的丁溶液pH=13.下列说法错误的是
| A.1 mol甲与足量乙反应转移2 mol电子 |
| B.离子半径Z>W |
| C.甲与丙反应时,既有离子键、共价键的断裂,又有离子键、共价键的形成 |
| D.四种元素可以组成化合物WXY2Z4 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】已知a、b、c、d、e是原子序数依次增大的短周期元素,其中a的一种核素常用来鉴定文物;c元素所组成的单质和氢化物中各有一种可以用来做消毒剂和漂白剂;d元素的简单离子半径是第三周期中最小的;e的最外层电子数是最内层电子数的3倍。下列判断正确的是
| A.a、b、c三种元素分别形成的单质均只有一种 |
| B.d的氧化物能溶于过量氨水 |
| C.e在过量的氧气中燃烧得到eO3 |
| D.a、b、d、e的单质都能与c的单质发生氧化还原反应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】X、Y、Z、W四种短周期元素在周期表中的相对位置如图所示, 这四种元素的最外层电子数之和为22,下列说法不正确的是
| Y | Z | ||
| W | X |
| A.Z与W可形成化合物WZ4 |
| B.Z、Y无最高正价 |
| C.Z的非金属性比Y强,所以Z的氢化物沸点比Y高 |
| D.WY2与 WZ4的化学键类型相同 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】A、B、C、D为四种原子序数递增的短周期主族元素,A和C同族但不相邻;B和D同族,D 元素原子最外层电子数是B元素原子次外层电子数的3倍。下列说法正确的是
| A.气态氢化物的稳定性:D>B |
| B.原子半径:D>C>B>A |
| C.A与B、C、D均可以形成二元共价化合物 |
| D.A、B、D三种元素形成的化合物A2DBn,n值越大酸性越强 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】被誉为“矿石熊猫”的香花石,由我国地质学家首次发现,它由前20号元素中的6种组成,其化学式为Y2X3(ZWR4)3T2,其中X、Y、Z为金属元素,Z的最外层电子数与次外层电子数相等,X、Z位于同族,Y、Z、R、T位于同周期,R最外层电子数是次外层的3倍,T无正价,X与R原子序数之和是W的2倍。下列说法错误的是
| A.原子半径:Y>Z>R>T |
| B.气态氢化物的稳定性:W<R<T |
| C.第一电离能:X>Z |
| D.XR2、WR2两种化合物中R的化合价不相同 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
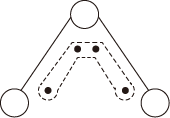
【推荐1】1949年度诺贝尔化学奖授予为研究臭氧做出贡献的化学家。臭氧能吸收有害紫外线,保护人类赖以生存的空间。O3分子的结构如图:呈V形,键角116.5°。三个原子以一个O原子为中心,与另外两个O原子分别构成一个极性共价键;中间O原子提供2个电子,旁边两个O原子提供1个电子,构成一个特殊的化学键(虚线内部分)——三个O原子均等的享有着4个电子。下列说法不正确的是
| A.题中极性共价键是σ键,特殊的化学键是π键 |
| B.臭氧与氧气是同素异形体 |
| C.SO2分子与O3分子的结构相似 |
| D.O3分子有4对孤电子对 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】关于物质的分类,下列说法正确的是
| A.溶于水能电离出H+的化合物称为酸 |
| B.H2、D2、T2互为同素异形体 |
| C.只由一种元素构成的物质一定是纯净物 |
| D.碱性氧化物一定是金属氧化物 |
您最近一年使用:0次




